Презентация - Глюкоза (строение, свойства, применение)
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 100%
- Слайдов: 39
- Просмотров: 4167
- Скачиваний: 1749
- Размер: 2.77 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы
Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы Урок алгебры по теме «Функция y=ax², её график и свойства» с применение системы учебных заданий как средства достижения планируемых результатов ФГОС. 9-й класс
Урок алгебры по теме «Функция y=ax², её график и свойства» с применение системы учебных заданий как средства достижения планируемых результатов ФГОС. 9-й класс Опорно-двигательная система - Строение, состав и свойства костей
Опорно-двигательная система - Строение, состав и свойства костей Строение и свойства биогеоценоза
Строение и свойства биогеоценоза Тема урока «Форма, строение, состав и свойства костей, рост костей. Типы соединения костей»
Тема урока «Форма, строение, состав и свойства костей, рост костей. Типы соединения костей» Практическое применение метода дма для исследования, анализа и диагностики свойств ПКМ
Практическое применение метода дма для исследования, анализа и диагностики свойств ПКМ Строение, свойства костей. Типы их соединения
Строение, свойства костей. Типы их соединения
Слайды и текст этой онлайн презентации
Слайд 1

УГЛЕВОДЫ.
Глюкоза. Строение. Свойства.
Применение.
Слайд 2

“Химик не такой должен быть, который дальше дыму и пеплу ничего не видит, а такой, который на основании опытных данных может делать теоретические выводы”
М.В.Ломоносов
Слайд 3

Цель урока:
Сделать вывод о природе неизвестного вещества на основании проведённого эксперимента и изучить его свойства.
Сделать вывод о природе неизвестного вещества на основании проведённого эксперимента и изучить его свойства.
Слайд 4
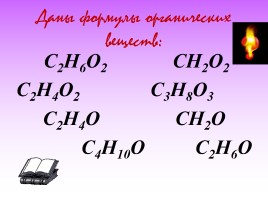
Даны формулы органических веществ:
C2H6O2 CH2O2 C2H4O2 C3H8O3 C2H4O CH2O C4H10O C2H6O
C2H6O2 CH2O2 C2H4O2 C3H8O3 C2H4O CH2O C4H10O C2H6O
Слайд 5
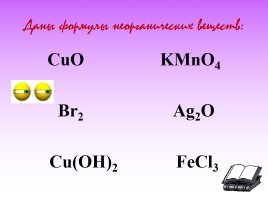
Даны формулы неорганических веществ:
CuO KMnO4 Br2 Ag2O Cu(OH)2 FeCl3
CuO KMnO4 Br2 Ag2O Cu(OH)2 FeCl3
Слайд 6

Углеводы – органические соединения, состоящие из углерода, водорода и кислорода, причем водород и кислород входят в соотношении (2:1) как в воде, отсюда и название. На основе этой аналогии русский химик К. Шмидт в 1844 г. предложил термин углевода (углерод и вода), а общая формула углеводов Сn(Н2 О)m .
Слайд 7

УГЛЕВОДЫ
Называют сахаристыми веществами или сахарами; Могут быть безвкусными, сладкими и горькими; Если сладость раствора сахарозы принять за 100 %, то сладость фруктозы – 173 %, глюкозы – 81 %, мальтозы и галактозы – 32 %, лактозы – 16 %.
Называют сахаристыми веществами или сахарами; Могут быть безвкусными, сладкими и горькими; Если сладость раствора сахарозы принять за 100 %, то сладость фруктозы – 173 %, глюкозы – 81 %, мальтозы и галактозы – 32 %, лактозы – 16 %.
Слайд 8

Слайд 9
моносахариды
дисахариды
полисахариды
УГЛЕВОДЫ
дисахариды
полисахариды
УГЛЕВОДЫ
Слайд 10
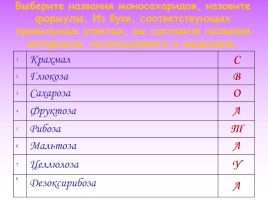
Выберите названия моносахаридов, назовите формулы. Из букв, соответствующих правильным ответам, вы составите название материала, используемого в медицине.
1 Крахмал С
2 Глюкоза В
3 Сахароза О
4 Фруктоза А
5 Рибоза Т
6 Мальтоза Л
7 Целлюлоза У
8 Дезоксирибоза А
1 Крахмал С
2 Глюкоза В
3 Сахароза О
4 Фруктоза А
5 Рибоза Т
6 Мальтоза Л
7 Целлюлоза У
8 Дезоксирибоза А
Слайд 11
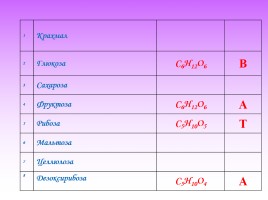
1 Крахмал
2 Глюкоза С6Н12О6 В
3 Сахароза
4 Фруктоза С6Н12О6 А
5 Рибоза С5Н10О5 Т
6 Мальтоза
7 Целлюлоза
8 Дезоксирибоза С5Н10О4 А
2 Глюкоза С6Н12О6 В
3 Сахароза
4 Фруктоза С6Н12О6 А
5 Рибоза С5Н10О5 Т
6 Мальтоза
7 Целлюлоза
8 Дезоксирибоза С5Н10О4 А
Слайд 12

Знаете ли вы что…
Углеводы используются с глубокой древности – самым первым углеводом (точнее смесью углеводов), с которым познакомился человек, был мед. Родиной сахарного тростника является северо-западная Индия-Бенгалия. Европейцы познакомились с тростниковым сахаром благодаря походам Александра Македонского в 327г. до н.э. Свекловичный сахар в чистом виде был открыт лишь в 1747 г. Немецким химиком А. Марггафом. Крахмал был известен еще древним грекам. Целлюлоза, как составная часть древесины, используется с глубокой древности.
Углеводы используются с глубокой древности – самым первым углеводом (точнее смесью углеводов), с которым познакомился человек, был мед. Родиной сахарного тростника является северо-западная Индия-Бенгалия. Европейцы познакомились с тростниковым сахаром благодаря походам Александра Македонского в 327г. до н.э. Свекловичный сахар в чистом виде был открыт лишь в 1747 г. Немецким химиком А. Марггафом. Крахмал был известен еще древним грекам. Целлюлоза, как составная часть древесины, используется с глубокой древности.
Слайд 13

Экспериментальная задача
Под номерами даны растворы альдегида, многоатомного спирта и неизвестного вещества. Необходимо, обнаружить в какой пробирке находится неизвестное вещество, зная качественные реакции на альдегид и многоатомный спирт.
Под номерами даны растворы альдегида, многоатомного спирта и неизвестного вещества. Необходимо, обнаружить в какой пробирке находится неизвестное вещество, зная качественные реакции на альдегид и многоатомный спирт.
Слайд 14
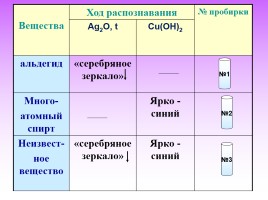
Вещества Ход распознавания Ход распознавания № пробирки
Вещества Ag2O, t Cu(OH)2 № пробирки
альдегид «серебряное зеркало»
Много- атомный спирт Ярко - синий
Неизвест- ное вещество «серебряное зеркало» Ярко - синий
№2
№1
№3
Вещества Ag2O, t Cu(OH)2 № пробирки
альдегид «серебряное зеркало»
Много- атомный спирт Ярко - синий
Неизвест- ное вещество «серебряное зеркало» Ярко - синий
№2
№1
№3
Слайд 15

ЗАДАЧА
Вещество в пробирке №3 имеет следующий качественный состав: W(C) = 40% W (H) = 6,7 % W (O) = 53,3 % Молекулярная масса неизвестного вещества 180 г/моль. Найдите формулу неизвестного вещества.
Вещество в пробирке №3 имеет следующий качественный состав: W(C) = 40% W (H) = 6,7 % W (O) = 53,3 % Молекулярная масса неизвестного вещества 180 г/моль. Найдите формулу неизвестного вещества.
Слайд 16

Строение молекулы глюкозы
C
H
O
O
H
H
H
H
O
O
H
H
O
H
H
C
H
2
O
H
=
5
C
H
O
O
H
H
H
H
O
O
H
H
O
H
H
C
H
2
O
H
=
5
Слайд 17
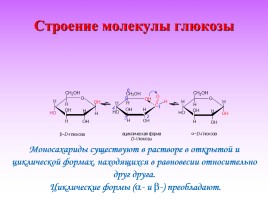
Строение молекулы глюкозы
O
H
C
O
H
H
O
O
H
O
H
H
H
H
H
2
1
3
4
6
5
C
H
2
O
H
C
H
2
O
H
H
H
O
O
H
O
H
O
H
H
H
H
H
O
C
H
2
O
H
H
H
O
O
H
O
H
O
H
H
H
H
H
O
а
ц
и
к
л
и
ч
е
с
к
а
я
ф
о
р
м
а
D
-
г
л
ю
к
о
з
ы
b
-
D
-
г
л
ю
к
о
з
а
a
-
D
-
г
л
ю
к
о
з
а
Моносахариды существуют в растворе в открытой и циклической формах, находящихся в равновесии относительно друг друга. Циклические формы (- и -) преобладают.
O
H
C
O
H
H
O
O
H
O
H
H
H
H
H
2
1
3
4
6
5
C
H
2
O
H
C
H
2
O
H
H
H
O
O
H
O
H
O
H
H
H
H
H
O
C
H
2
O
H
H
H
O
O
H
O
H
O
H
H
H
H
H
O
а
ц
и
к
л
и
ч
е
с
к
а
я
ф
о
р
м
а
D
-
г
л
ю
к
о
з
ы
b
-
D
-
г
л
ю
к
о
з
а
a
-
D
-
г
л
ю
к
о
з
а
Моносахариды существуют в растворе в открытой и циклической формах, находящихся в равновесии относительно друг друга. Циклические формы (- и -) преобладают.
Слайд 18

Физические свойства глюкозы
Белое кристаллическое вещество сладкого вкуса, хорошо растворимое в воде, температура плавления 146 С.
«виноградный сахар»
Белое кристаллическое вещество сладкого вкуса, хорошо растворимое в воде, температура плавления 146 С.
«виноградный сахар»
Слайд 19

Знаете ли вы что глюкоза --
Один из ключевых продуктов обмена веществ, обеспечивающих живые клетки энергией (в процессах дыхания, брожения, гликолиза); Служит исходным продуктом биосинтеза многих веществ; У человека и животных постоянный уровень глюкозы в крови поддерживается путем синтеза и распада гликогена; В организме человека глюкоза содержится в мышцах, в крови и в небольших количествах во всех клетках.
Один из ключевых продуктов обмена веществ, обеспечивающих живые клетки энергией (в процессах дыхания, брожения, гликолиза); Служит исходным продуктом биосинтеза многих веществ; У человека и животных постоянный уровень глюкозы в крови поддерживается путем синтеза и распада гликогена; В организме человека глюкоза содержится в мышцах, в крови и в небольших количествах во всех клетках.
Слайд 20

Химические свойства глюкозы
Свойства альдегида 1. Восстановление. Альдегидная группа глюкозы может восстанавливаться до спиртовой с образованием шестиатомного спирта сорбита.
сорбит
Свойства альдегида 1. Восстановление. Альдегидная группа глюкозы может восстанавливаться до спиртовой с образованием шестиатомного спирта сорбита.
сорбит
Слайд 21

2. Окисление
а) Глюкоза окисляется раствором гидроксида меди (II) при нагревании
HOCH2 (CHOH)4 CHO + 2Сu(OH)2
глюкоза
HOCH2 (CHOH)4 COOH + Cu2O + 2H2O
глюконовая кислота
б) Глюкоза окисляется аммиачным раствором оксида серебра (I) при нагревании
HOCH2 (CHOH)4 CHO + Ag2O
глюкоза
HOCH2 (CHOH)4 COOH + 2Ag↓
глюконовая кислота
Слайд 22

Образование сахаратов ( с гидроксидом меди (II) без нагревания)
C
u
(
O
H
)
2
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
O
H
H
O
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
H
O
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
O
H
C
u
O
O
2
-
2
H
2
O
Свойства спиртов
C
u
(
O
H
)
2
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
O
H
H
O
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
H
O
C
H
H
2
C
C
H
C
H
C
H
C
O
H
O
H
O
H
O
H
O
H
C
u
O
O
2
-
2
H
2
O
Свойства спиртов
Слайд 23
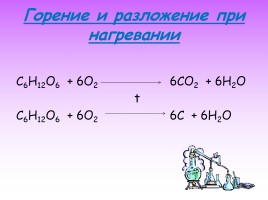
Горение и разложение при нагревании
C6H12O6 + 6O2 6CO2 + 6H2O t C6H12O6 + 6O2 6C + 6H2O
C6H12O6 + 6O2 6CO2 + 6H2O t C6H12O6 + 6O2 6C + 6H2O
Слайд 24

Брожение – процесс разложения глюкозы под действием микроорганизмов или ферментов, сопровождающийся расщеплением углеродных связей.
Различают спиртовое, молочнокислое и маслянокислое брожение: 1. Спиртовое брожение глюкозы осуществляется под действием дрожжевых ферментов C6H12O6 2C2H5OH + 2CO2 2. Молочнокислое брожение глюкозы с образованием молочной кислоты происходит под влиянием ферментов молочнокислых бактерий и используется в пищевой промышленности: C6H12O6 CH3 CH COOH OH 3. Маслянокислое брожение глюкозы приводит к образованию масляной кислоты: C6H12O6 C3H7COOH + 2CO2 + 2H2
Различают спиртовое, молочнокислое и маслянокислое брожение: 1. Спиртовое брожение глюкозы осуществляется под действием дрожжевых ферментов C6H12O6 2C2H5OH + 2CO2 2. Молочнокислое брожение глюкозы с образованием молочной кислоты происходит под влиянием ферментов молочнокислых бактерий и используется в пищевой промышленности: C6H12O6 CH3 CH COOH OH 3. Маслянокислое брожение глюкозы приводит к образованию масляной кислоты: C6H12O6 C3H7COOH + 2CO2 + 2H2
Слайд 25
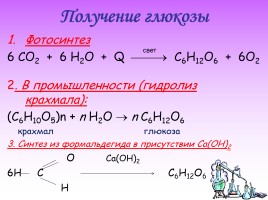
Получение глюкозы
Фотосинтез 6 СO2 + 6 H2O + Q C6H12O6 + 6O2 2. В промышленности (гидролиз крахмала): (C6H10O5)n + n H2O n C6H12O6 крахмал глюкоза 3. Синтез из формальдегида в присутствии Ca(OH)2 O Ca(OH)2 6H C C6H12O6 H
свет
Фотосинтез 6 СO2 + 6 H2O + Q C6H12O6 + 6O2 2. В промышленности (гидролиз крахмала): (C6H10O5)n + n H2O n C6H12O6 крахмал глюкоза 3. Синтез из формальдегида в присутствии Ca(OH)2 O Ca(OH)2 6H C C6H12O6 H
свет
Слайд 26

Применение
В медицине (консервирование крови, внутривенное вливание, для приготовления лечебных препаратов) Кондитерское производство Крашение и апперетирование тканей и кожи Производство зеркал и игрушек
В медицине (консервирование крови, внутривенное вливание, для приготовления лечебных препаратов) Кондитерское производство Крашение и апперетирование тканей и кожи Производство зеркал и игрушек
Слайд 27

ГЛЮКОЗА В
ВОЕННОМ ДЕЛЕ
Слайд 28

ГЛЮКОЗА ЯВЛЯЕТСЯ
АНТИДОТОМ
ПРИ ОТРАВЛЕНИИ
ЦИАНИДАМИ
Слайд 29
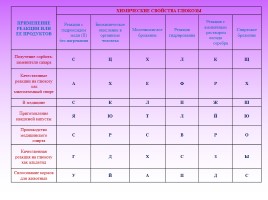
ПРИМЕНЕНИЕ
РЕАКЦИИ ИЛИ
ЕЕ ПРОДУКТОВ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ
ПРИМЕНЕНИЕ РЕАКЦИИ ИЛИ ЕЕ ПРОДУКТОВ Реакции с гидроксидом меди (II) без нагревания Биохимическое окисление в организме человека Молочнокислое брожение Реакция гидрирования Реакция с аммиачным раствором оксида серебра Спиртовое брожение
Получение сорбита- заменителя сахара С Ц Х Л К Щ
Качественные реакции на глюкозу как многоатомный спирт А Х Е Ф Р Х
В медицине С К Л П Ж Ш
Приготовление квашеной капусты Я Ю Т Л Й Ю
Производство медицинского спирта С Р С В Р О
Качественная реакция на глюкозу как альдегид Г Д Х С З Ы
Силосование кормов для животных У Й А П Д С
ПРИМЕНЕНИЕ РЕАКЦИИ ИЛИ ЕЕ ПРОДУКТОВ Реакции с гидроксидом меди (II) без нагревания Биохимическое окисление в организме человека Молочнокислое брожение Реакция гидрирования Реакция с аммиачным раствором оксида серебра Спиртовое брожение
Получение сорбита- заменителя сахара С Ц Х Л К Щ
Качественные реакции на глюкозу как многоатомный спирт А Х Е Ф Р Х
В медицине С К Л П Ж Ш
Приготовление квашеной капусты Я Ю Т Л Й Ю
Производство медицинского спирта С Р С В Р О
Качественная реакция на глюкозу как альдегид Г Д Х С З Ы
Силосование кормов для животных У Й А П Д С
Слайд 30
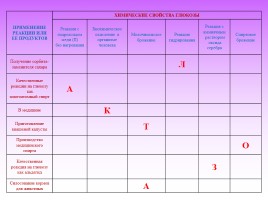
ПРИМЕНЕНИЕ
РЕАКЦИИ ИЛИ
ЕЕ ПРОДУКТОВ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ ХИМИЧЕСКИЕ СВОЙСТВА ГЛЮКОЗЫ
ПРИМЕНЕНИЕ РЕАКЦИИ ИЛИ ЕЕ ПРОДУКТОВ Реакции с гидроксидом меди (II) без нагревания Биохимическое окисление в организме человека Молочнокислое брожение Реакция гидрирования Реакция с аммиачным раствором оксида серебра Спиртовое брожение
Получение сорбита- заменителя сахара Л
Качественные реакции на глюкозу как многоатомный спирт А
В медицине К
Приготовление квашеной капусты Т
Производство медицинского спирта О
Качественная реакция на глюкозу как альдегид З
Силосование кормов для животных А
ПРИМЕНЕНИЕ РЕАКЦИИ ИЛИ ЕЕ ПРОДУКТОВ Реакции с гидроксидом меди (II) без нагревания Биохимическое окисление в организме человека Молочнокислое брожение Реакция гидрирования Реакция с аммиачным раствором оксида серебра Спиртовое брожение
Получение сорбита- заменителя сахара Л
Качественные реакции на глюкозу как многоатомный спирт А
В медицине К
Приготовление квашеной капусты Т
Производство медицинского спирта О
Качественная реакция на глюкозу как альдегид З
Силосование кормов для животных А
Слайд 31

Лактоза С12Н22О11 — углевод группы дисахаридов, содержится в молоке и молочных продуктах. Молекула лактозы состоит из остатков молекул глюкозы и галактозы. Лактозу иногда называют молочным сахаром. Лактоза является основным углеводом женского молока, хотя в нем присутствуют в небольших количествах также и галактоза, фруктоза и другие олигосахариды. Этот сахар присущ только молоку, и женское молоко содержит наивысшие его концентрации (в среднем 4% в молозиве, возрастая до 7% в зрелом молоке). Лактоза является специфическим продуктом питания в младенчестве. Лактоза присуща европейцам и некоторым другим народам, но у большинства людей лактоза не усваивается, начиная с середины детского возраста; поэтому пища, содержащая лактозу может вызвать нарушения пищеварения.
Слайд 32
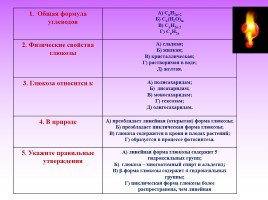
1. Общая формула углеводов А) СnH2n+2
Б) Cn(H2O)m
В) СnH2n-2
Г) СnH2n
2. Физические свойства глюкозы А) сладкая; Б) жидкая; В) кристаллическая; Г) растворимая в воде; Д) желтая.
3. Глюкоза относится к А) полисахаридам; Б) дисахаридам; В) моносахаридам; Г) гексозам; Д) олигосахаридам.
4. В природе А) преобладает линейная (открытая) форма глюкозы; Б) преобладает циклическая форма глюкозы; В) глюкоза содержится в крови и плодах растений; Г) образуется в процессе фотосинтеза.
5. Укажите правильные утверждения А) линейная форма глюкозы содержит 5 гидроксильных групп; Б) глюкоза – многоатомный спирт и альдегид; В) β-форма глюкозы содержит 4 гидроксильных группы; Г) циклическая форма глюкозы более распространена, чем линейная
2. Физические свойства глюкозы А) сладкая; Б) жидкая; В) кристаллическая; Г) растворимая в воде; Д) желтая.
3. Глюкоза относится к А) полисахаридам; Б) дисахаридам; В) моносахаридам; Г) гексозам; Д) олигосахаридам.
4. В природе А) преобладает линейная (открытая) форма глюкозы; Б) преобладает циклическая форма глюкозы; В) глюкоза содержится в крови и плодах растений; Г) образуется в процессе фотосинтеза.
5. Укажите правильные утверждения А) линейная форма глюкозы содержит 5 гидроксильных групп; Б) глюкоза – многоатомный спирт и альдегид; В) β-форма глюкозы содержит 4 гидроксильных группы; Г) циклическая форма глюкозы более распространена, чем линейная
Слайд 33

КАК ЛЯГУШКИ УХИТРЯЮТСЯ
НЕ ЗАМЕРЗНУТЬ «НАСМЕРТЬ» ?
Слайд 34

Герои романа Жюля Верна «Дети капитана Гранта»“ только собирались поужинать мясом подстреленной ими ламы (гуанако), как вдруг выяснилось, что оно совершенно не съедобно. Быть может, оно слишком долго лежало?” - озадаченно спросил один из них. “Нет, оно, к сожалению, слишком долго бежало! - ответил учёный-географ Паганель - Мясо гуанако вкусно только тогда, когда животное убито во время отдыха, но если за ним долго охотиться и животное долго бежало, тогда его мясо несъедобно”.
Слайд 35

Рефлексия (синквейн) - пятистрочная стихотворная форма, возникшая в США под влиянием японской поэзии. В дальнейшем она стала использоваться в дидактических целях, как эффективный метод развития образной речи, который позволяет быстро получить результат.
1 строка – имя существительное (тема синквейна) 2 строка – два прилагательных (раскрывающие тему синквейна) 3 строка – три глагола (описывают действия) 4 строка – фраза или предложение (высказывают своё отношение к теме) 5 строка – синоним (слово – резюме)
1 строка – имя существительное (тема синквейна) 2 строка – два прилагательных (раскрывающие тему синквейна) 3 строка – три глагола (описывают действия) 4 строка – фраза или предложение (высказывают своё отношение к теме) 5 строка – синоним (слово – резюме)
Слайд 36

Например, 1. Этилен 2. Ненасыщенный, активный 3. Горит, обесцвечивает, присоединяет 4. Этилен – представитель непредельных углеводородов 5. Алкен
Слайд 37

1. Глюкоза 2. Кристаллическая, растворимая 3. Горит, восстанавливается, окисляется 4. Глюкоза – представитель углеводов 5. Альдегидоспирт
Слайд 38

Домашнее задание:
§32, стр.131 – 136; упр.8 (б) стр.146
§32, стр.131 – 136; упр.8 (б) стр.146
Слайд 39

Спасибо
за
внимание!
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
