Слайды и текст этой онлайн презентации
Слайд 1
Текст надписи
УГЛЕРОД
Приложение
к разработке урока
в 9 классе по теме: Углерод
Выполнила:
учитель химии
МБОУ СОШ
с. Большие Озерки
Усанкина Н.А.
Слайд 2
?
ЗАГЛЯНЕМ
В ПРОШЛОЕ
Слайд 3
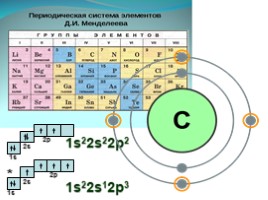
1s22s22p2
1s22s12p3
2p
2s
1s
*
1s
2s
2p
Слайд 4
Природные источники углерода
Слайд 5
Углерод многоликий
Слайд 6
А
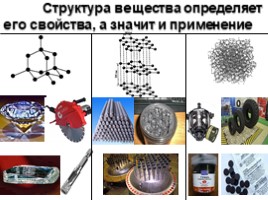
Структура вещества определяет
его свойства, а значит и применение
Слайд 7
Сокровища Алмазного фонда России
Слайд 8
Химические свойства углерода
При низких температурах углерод инертен, но при нагревании его
активность возрастает:
Углерод – восстановитель:
1) С + О2 = СО2 (углекислый газ)
С0 – 4е = С+4 1 - восстановитель
О2 + 4е = 2О-2 1 - окислитель
При недостатке кислорода – неполное сгорание, восстанавливается до оксида углерода (II):
C0 + C+4O2 = 2C+2O (угарный газ)
С0 + 2S = С+4S2 (сероуглерод)
С0 + 2F2 1000C C+4F4 (фторид углерода)
С другими галогенами углерод не взаимодействует.
С0 + H2Oпар 1200С С+4O2 + H2 (водяной газ)
2) Углерод восстанавливает металлы из их оксидов (получение металлов из руд):
2C0 + SnO2 = Sn + 2C+2O
3С0 + Fe2O3 = 2Fe + 3C+2O
3) С0 + 2Н2SO4конц. = C+4O2 + 2SO2 + 2H2O
C0 + 4HNO3конц. = С+4O2 + 4NO2 + 2H2O
Углерод – окислитель:
1) С + 2H2 t, P, cat CH4 (метан)
С0 + 4е = С+4 1 - окислитель
H2 – 2e = 2H+ 2 - восстановитель
С некоторыми металлами образует карбиды (Al, Ca):
2) 3С0 + 4AL = Al4C-43
3) С0 + Si 2000С SiC-4 (карборунд)
Слайд 9
Применение полученных в результате проявления
химических свойств углеродом соединений
СH4 (метан) , газ, бытовой газ, широкое применение в промышленности также находят его производные.
__________________________
СО2 («сухой лед»), в промышленности применяют для хранения пищевых продуктов. Не поддерживает горения, используют для тушения пожаров. Также используют для изготовления шипучих напитков и для получения соды.
___________________
SC2 (сероуглерод), жидкость с неприятным запахом, токсичен, применяют как растворитель жиров, масел, смол, каучуков, фосфора, йода, нитрата серебра. В производстве используется для получения вискозы (искусственного шелка).
____________________
СF4 (фторид углерода), бесцветный газ без запаха, применяется в качестве низкотемпературного хладагента (фреон, хладон), компонент дыхательных смесей при ___________________ глубоководных погружениях.
Слайд 10
Биологическая роль углерода
Слайд 11

Тест по теме: Углерод
1. Чему равен заряд ядра атома углерода?
1. +1 2. +6 3. +4 4. 0
2. Укажите степень окисления углерода.
1. –2, 0, +2 2. -4, 0, +2, +4 3. -5, -3, 0, +3, +5
3. Верно ли следующее утверждение: Углерод в природе встречается в виде простых веществ?
1. Верно 2. Неверно
4. Верно ли утверждение: Графит и алмаз являются углеродом?
1. Верно 2. Неверно
5. Простые вещества, образованные углеродом – это типичные ______________
6. Аллотропная модификация углерода – графит:
1. Твердое, прозрачное, бесцветное, аморфное вещество
2. Мягкое, непрозрачное, серое, кристаллическое вещество
3. Твердое, прозрачное, бесцветное, кристаллическое вещество
4. Твердое, прозрачное, бесцветное, кристаллическое вещество
7. Адсорбция - это процесс:
1) Поглощения и выделения газообразных веществ поверхностью твердых веществ
2) Выделения и поглощения газообразных веществ поверхностью твердых
3) Поглощения и выделения растворенных веществ поверхностью твердых веществ
4) Поглощение и удерживание на своей поверхности газы и растворенные вещества
8. Углерод проявляет свойства:
1. Окислительные 2. Восстановительные 3. Окислительные и восстановительные
9. Раскаленный ___________реагирует с водой с образованием водяного газа – смеси угарного газа
и водорода: С + Н2О = СО + Н2
10. Как называются вещества, которые образуются при взаимодействии углерода с металлами:
1. Карбиды 2) Карбонаты 3) Силикаты 4) Нитраты
11. Расставьте коэффициенты в уравнении: Fe2O3 + C → Fe + CO2. Ответ дайте в виде суммы
коэффициентов:
1. 12 2. 13 3. 14 4. 11
Слайд 12

Ответы на тест по теме: Углерод
1. Чему равен заряд ядра атома углерода?
1. +1 2. +6 3. +4 4. 0
2. Укажите степень окисления углерода.
1. –2, 0, +2 2. -4, 0, +2, +4 3. -5, -3, 0, +3, +5
3. Верно ли следующее утверждение: Углерод в природе встречается в виде простых веществ?
1. Верно 2. Неверно
4. Верно ли утверждение: Графит и алмаз являются углеродом?
1. Верно 2. Неверно
5. Простые вещества, образованные углеродом – это типичные неметаллы
6. Аллотропная модификация углерода – графит:
1. Твердое, прозрачное, бесцветное, аморфное вещество
2. Мягкое, непрозрачное, серое, кристаллическое вещество
3. Твердое, прозрачное, бесцветное, кристаллическое вещество
4. Твердое, прозрачное, бесцветное, кристаллическое вещество
7. Адсорбция - это процесс:
1) Поглощения и выделения газообразных веществ поверхностью твердых веществ
2) Выделения и поглощения газообразных веществ поверхностью твердых веществ
3) Поглощения и выделения растворенных веществ поверхностью твердых веществ
4) Поглощение и удерживание на своей поверхности газов и растворенных веществ
8. Углерод проявляет свойства:
1. Окислительные 2. Восстановительные 3. Окислительные и восстановительные
9. Раскаленный уголь реагирует с водой с образованием водяного газа – смеси угарного газа
и водорода: С + Н2О = СО + Н2
10. Как называются вещества, которые образуются при взаимодействии углерода с металлами:
1. Карбиды 2) Карбонаты 3) Силикаты 4) Нитраты
11. Расставьте коэффициенты в уравнении: Fe2O3 + C → Fe + CO2. Ответ дайте в виде суммы
коэффициентов:
1. 12 2. 13 3. 14 4. 11
 Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека»
Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека» Методическая разработка урока математики по теме Многоугольники. 5-й класс
Методическая разработка урока математики по теме Многоугольники. 5-й класс Методическая разработка урока обществознания в 10-м классе по теме «Нации и межнациональные отношения»
Методическая разработка урока обществознания в 10-м классе по теме «Нации и межнациональные отношения» Методическая разработка урока английского языка по теме Дорожная безопасность. 6-й класс
Методическая разработка урока английского языка по теме Дорожная безопасность. 6-й класс Разработка урока английского языка в 5 классе по теме «Разделительные вопросы» с использованием информационных технологий
Разработка урока английского языка в 5 классе по теме «Разделительные вопросы» с использованием информационных технологий Конспект урока литературного чтения по теме «Д.Лондон Бурый волк». 3-й класс
Конспект урока литературного чтения по теме «Д.Лондон Бурый волк». 3-й класс Технологическая карта урока по теме “Where there’s a will, there’s a way. Stress out”. 11-й класс
Технологическая карта урока по теме “Where there’s a will, there’s a way. Stress out”. 11-й класс