Слайды и текст этой онлайн презентации
Слайд 1
Ионные уравнения реакций
Химия 8 класс
.
Слайд 2
Лампочка прибора для определения
электропроводности загорится,
если электроды поместить в:
Раствор серной кислоты
Раствор сахара
Спирт
Слайд 3
Анион
Катод
Анод
Катион
Как называется отрицательный полюс источника тока?
Слайд 4
К какому полюсу источника тока двигаются отрицательно заряженные ионы:
Анион
Анод
Катод
Катион
Слайд 5
Установите соответствие
Б) Катионы
A) Анионы
2. Zn2+
3. H2
1. NO3-
Слайд 6
SO42-
Na+
Na+
= 2Na+ + SO42-
Диссоциация сульфата натрия:
Na2SO4
Слайд 7
Ba2+
Cl-
Cl-
Диссоциация хлорида бария:
= Ba2+ + 2Cl-
BaCl2
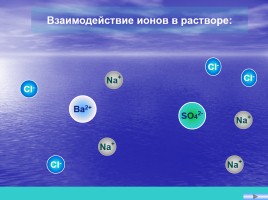
Слайд 8
SO42-
Na+
Na+
Ba2+
Cl-
Cl-
Cl-
Взаимодействие ионов в растворе:
Na+
Na+
Cl-
Слайд 9
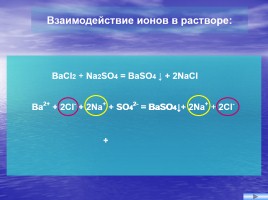
BaCl2 + Na2SO4 = BaSO4 ↓ + 2NaCl
Ba2+ + 2Cl- + 2Na+ + SO42- = BaSO4↓+ 2Na+ + 2Cl-
+
Взаимодействие ионов в растворе:
Ba2+
SO42-
= BaSO4↓
Слайд 10
Домашнее задание:
§ 37 упр. 1,2
Слайд 11
ЛИТЕРАТУРА
1. Габриелян О.С. Программа курса химии для 8 – 11 классов общеобразовательных учреждений. – М.: ДРОФА 2006.
2. Габриелян О.С. Химия 8 класс: учебник для общеобразовательных учреждений. – М.: ДРОФА. 2005.
3. Горковенко М.Ю. Химия 8 класс: Поурочные разработки к учебникам О.С.Габриеляна, Л.С.Гузея, В.В.Сорокина, Р.П.Суровцевой; Г.Е.Рудзитиса, Ф.Г.Фельдмана. – М.: ВАКО, 2004.
 Тема урока: «Ионные уравнения реакций»
Тема урока: «Ионные уравнения реакций» Ионные уравнения
Ионные уравнения Обобщение и систематизация знаний по теме «Растворение. Растворы. Свойства растворов электролитов, ионные уравнения, овр»
Обобщение и систематизация знаний по теме «Растворение. Растворы. Свойства растворов электролитов, ионные уравнения, овр» Учимся решать уравнения
Учимся решать уравнения Уравнение состояния идеального газа. Газовые законы
Уравнение состояния идеального газа. Газовые законы Использование инновационных технологий на уроках музыки и изобразительного искусства
Использование инновационных технологий на уроках музыки и изобразительного искусства Образовательные информационные ресурсы
Образовательные информационные ресурсы