Слайды и текст этой онлайн презентации
Слайд 1
Учитель химии МОУ СОШ № 1 г. Южноуральска Курсакова
Светлана Евгеньевна
Сера
Слайд 2
План:
Общая характеристика VI-а подгруппы
Сера
Сероводород и сульфиды
Оксиды серы
Оксид серы (IV)
Оксид серы (VI)
Сернистая кислота
Серная кислота
Слайд 4
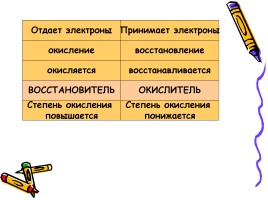
Отдает электроны
Принимает электроны
ВОССТАНОВИТЕЛЬ
восстанавливается
ОКИСЛИТЕЛЬ
окисляется
восстановление
окисление
Степень окисления
повышается
Степень окисления
понижается
Слайд 5
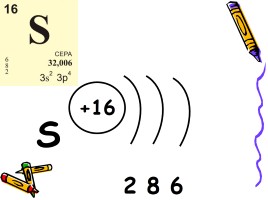
Строение атома
На внешнем электронном слое у атома серы шесть электронов.
Взаимодействуя с менее электроотрицательными элементами сера может принимать 2 электрона, проявляя степень окисления –2.
Также сера способна отдавать электроны, проявляя степень окисления от +2 до +6,
Слайд 6
По отношению к металлам, водороду и менее электроотрицательным неметаллам сера является окислителем со степенью окисления -2.
Степень окисления
Слайд 7
По отношению к фтору, кислороду, более электроотрицательным неметаллами, сложным веществам – сера является восстановителем
Окислительно-востановительные свойства
Слайд 8
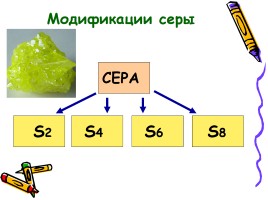
СЕРА
S2
S8
S6
S4
Модификации серы
Слайд 10
В обычных условиях это кристаллы так называемой ромбической модификации.
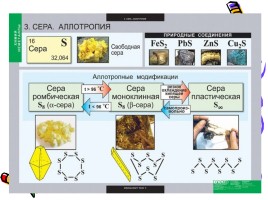
Аллотропные модификации серы.
Слайд 11
Известно несколько аллотропных модификаций серы. До температуры 150C молекула серы имеет циклическую форму. Это кольцо из 8 атомов, соединенных в виде короны.
Аллотропные модификации серы.
Слайд 12
Химическая связь –
ковалентная неполярная
2. Кристаллическая решетка –
молекулярная
Температуры плавления и кипения –
низкие
4.Летучие и непрочные
Слайд 13
В воде сера не растворяется (всплывает), растворима в органических растворителях.
Физические свойства
Слайд 14
При обычных условиях:
Hg + S =HgS
Процесс ДЕМЕРКУРИЗАЦИИ
Химические свойства
Слайд 15
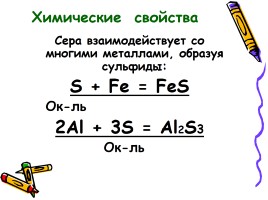
Сера взаимодействует со многими металлами, образуя сульфиды:
S + Fe = FeS
Ок-ль
2Al + 3S = Al2S3
Ок-ль
Химические свойства
Слайд 16
При нагревании сера реагирует с водородом, образуя сероводород:
S + Н2 = H2S
Химические свойства
Слайд 17
Из неметаллов только азот и йод не соединяются с серой. Сжигание серы в струе кислорода приводит к образованию сернистого газа или сернистого ангидрида SO2 :
S + O2 = SO2
Химические свойства
Слайд 18
Элементарная сера может также проявлять восстановительные свойства:
S + 2HNO3 = H2SO4 + 2NO
Химические свойства
Слайд 21
Домашнее задание:
§ 21 упр. 3
Слайд 22
Интернет источники:
http://media.memurlar.net/album/589/1c9c61d9-1ae2-e211-9ee7-14feb5cc13c9.jpg - сера
http://kzdocs.docdat.com/pars_docs/refs/15/14854/14854_html_2bf65e3f.jpg - химический элемент сера
http://everythingmaths.co.za/science/grade-10/12-the-particles-that-substances-are-made-of/images/eca278e55206d78105bdd5a0f38a4460.png -моноклинная сера
http://www.uchkom43.ru/admin/uploads/2711280561.jpeg - сера. Аллотропия
http://works.doklad.ru/images/uvSy1e5Fp44/m35153abe.png - применение серы
 Серая шейка. Литературное чтение 3 класс
Серая шейка. Литературное чтение 3 класс Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы
Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы Евгений Серафимович Велтистов. «Приключения Элекроника»
Евгений Серафимович Велтистов. «Приключения Элекроника» Мастер-класс. «Изготовление открытки с декорированием цветами из пайеток и бисера»
Мастер-класс. «Изготовление открытки с декорированием цветами из пайеток и бисера» Сакура из бисера
Сакура из бисера Серафим Саровский. Доброта
Серафим Саровский. Доброта Бизнес-план «Украшения из бисера»
Бизнес-план «Украшения из бисера»