Презентация - Углерод и его соединения
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 83%
- Слайдов: 21
- Просмотров: 6980
- Скачиваний: 3416
- Размер: 1.3 MB
- Класс: 10
- Формат: ppt / pptx
Слайды и текст этой онлайн презентации
Слайд 1

Углерод и его соединения
Работу выполнила: учитель ГБОУ СОШ №1465 Попова Светлана Анатольевна
Работу выполнила: учитель ГБОУ СОШ №1465 Попова Светлана Анатольевна
Слайд 2
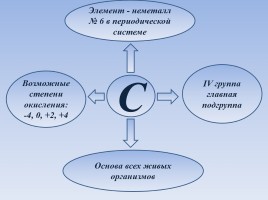
Элемент - неметалл № 6 в периодической системе
C
IV группа главная подгруппа
Возможные степени окисления: -4, 0, +2, +4
Основа всех живых организмов
C
IV группа главная подгруппа
Возможные степени окисления: -4, 0, +2, +4
Основа всех живых организмов
Слайд 3
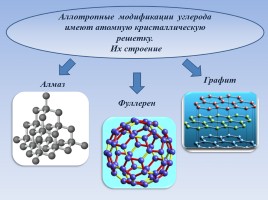
Аллотропные модификации углерода имеют атомную кристаллическую решетку.
Их строение
Алмаз
Графит
Фуллерен
Алмаз
Графит
Фуллерен
Слайд 4

Алмаз
Применяется в: Обрабатывающей промышленности Электротехнике Горной промышленности Ювелирном производстве
…это самое твердое вещество на Земле, тугоплавкое с высоким показателем преломления
Применяется в: Обрабатывающей промышленности Электротехнике Горной промышленности Ювелирном производстве
…это самое твердое вещество на Земле, тугоплавкое с высоким показателем преломления
Слайд 5

Графит
…это мягкое серо-черное вещество, тугоплавкое , являющееся полупроводником со слоистой структурой. Применяется в: Графитовых стержнях-электродах Производстве теплозащитного материала для головных частей ракет (термостойкость) Получении тиглей Изготовлении минеральных красок Карандашной промышленности
…это мягкое серо-черное вещество, тугоплавкое , являющееся полупроводником со слоистой структурой. Применяется в: Графитовых стержнях-электродах Производстве теплозащитного материала для головных частей ракет (термостойкость) Получении тиглей Изготовлении минеральных красок Карандашной промышленности
Слайд 6

Фуллерен
Фуллерены планируют использовать: 1. Для создания фотоприемников 2. Для создания сверхпроводящих материалов 3. В качестве красителей для копировальных машин 4. В качестве основы для аккумуляторных батарей 5. Для создания оптоэлектронных устройств 6. В медицине и фармакологии
… это новая аллотропная форма углерода , молекула которого состоит из 60-70 атомов , образующих сферу.
Фуллерены планируют использовать: 1. Для создания фотоприемников 2. Для создания сверхпроводящих материалов 3. В качестве красителей для копировальных машин 4. В качестве основы для аккумуляторных батарей 5. Для создания оптоэлектронных устройств 6. В медицине и фармакологии
… это новая аллотропная форма углерода , молекула которого состоит из 60-70 атомов , образующих сферу.
Слайд 7

Нахождение в природе
Мел, известняк, мрамор CaCO3
Магнезит MgCO3
Сидерит FeCO3
В самородном виде: алмаз и графит
В виде солей:
Содержание углерода в земной коре 0,1 % по массе
Мел, известняк, мрамор CaCO3
Магнезит MgCO3
Сидерит FeCO3
В самородном виде: алмаз и графит
В виде солей:
Содержание углерода в земной коре 0,1 % по массе
Слайд 8

Слайд 9

В составе растений и животных (~18 %).
В организме человека достигает около 21 % (15 кг на 70 кг массы тела). Углерод составляет 2/3 массы мышц и 1/3 массы костной ткани
Выводится из организма преимущественно с выдыхаемым воздухом (углекислый газ) и мочой (мочевина).
Углерод в живых организмах
В организме человека достигает около 21 % (15 кг на 70 кг массы тела). Углерод составляет 2/3 массы мышц и 1/3 массы костной ткани
Выводится из организма преимущественно с выдыхаемым воздухом (углекислый газ) и мочой (мочевина).
Углерод в живых организмах
Слайд 10
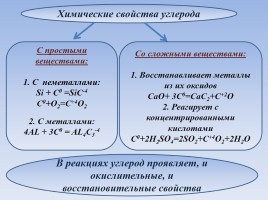
Химические свойства углерода
Со сложными веществами: 1. Восстанавливает металлы из их оксидов CaO+ 3C0=CaC2+C+2O 2. Реагирует с концентрированными кислотами С0+2H2SO4=2SO2+C+4O2+2H2O
С простыми веществами: 1. С неметаллами: Si + C0 =SiC-4 C0+O2=C+4O2 2. С металлами: 4AL + 3C0 = AL4C3-4
В реакциях углерод проявляет, и окислительные, и восстановительные свойства
Со сложными веществами: 1. Восстанавливает металлы из их оксидов CaO+ 3C0=CaC2+C+2O 2. Реагирует с концентрированными кислотами С0+2H2SO4=2SO2+C+4O2+2H2O
С простыми веществами: 1. С неметаллами: Si + C0 =SiC-4 C0+O2=C+4O2 2. С металлами: 4AL + 3C0 = AL4C3-4
В реакциях углерод проявляет, и окислительные, и восстановительные свойства
Слайд 11
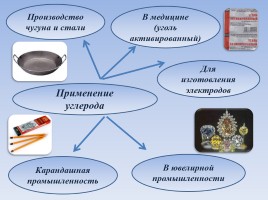
Применение углерода
Производство чугуна и стали
В медицине (уголь активированный)
Карандашная промышленность
Для изготовления электродов
В ювелирной промышленности
Производство чугуна и стали
В медицине (уголь активированный)
Карандашная промышленность
Для изготовления электродов
В ювелирной промышленности
Слайд 12
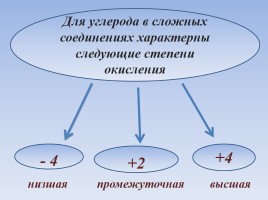
Для углерода в сложных соединениях характерны следующие степени окисления
- 4
+4
+2
низшая
промежуточная
высшая
- 4
+4
+2
низшая
промежуточная
высшая
Слайд 13
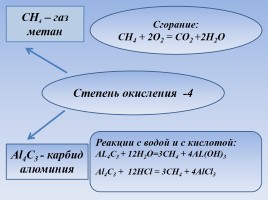
Степень окисления -4
CH4 – газ метан
Al4C3 - карбид алюминия
Сгорание: CH4 + 2O2 = CO2 +2H2O
Реакции с водой и с кислотой: AL4C3 + 12H2O=3CH4 + 4AL(OH)3 Al4C3 + 12HCl = 3CH4 + 4AlCl3
CH4 – газ метан
Al4C3 - карбид алюминия
Сгорание: CH4 + 2O2 = CO2 +2H2O
Реакции с водой и с кислотой: AL4C3 + 12H2O=3CH4 + 4AL(OH)3 Al4C3 + 12HCl = 3CH4 + 4AlCl3
Слайд 14

Степень окисления +2
CO - угарный газ сильный яд, опасный для жизни и здоровья человека (несолеобразующий оксид)
CO - угарный газ сильный яд, опасный для жизни и здоровья человека (несолеобразующий оксид)
Слайд 15

Степень окисления +4
H2CO3-угольная кислота
Соли угольной кислоты (например K2CO3-карбонат калия)
CO2-углекислый газ
H2CO3-угольная кислота
Соли угольной кислоты (например K2CO3-карбонат калия)
CO2-углекислый газ
Слайд 16

1.Реагирует с кислородом
2CO + O2 =CO2
2. Является восстановителем металлов из их оксидов
ZnO + CO = Zn + CO2
Химические свойства CO
Химические свойства CO
Слайд 17

Химические свойства CO2- (кислотный оксид)
1.Реагирует с водой CO2 + H2O = H2CO3 2.Реагирует с основными оксидами CO2 + CaO = CaCO3 3.Реагирует с щелочами CO2 + 2KOH = K2CO3 + H2O 4.Реагирует с углеродом CO2 + C = 2CO
1.Реагирует с водой CO2 + H2O = H2CO3 2.Реагирует с основными оксидами CO2 + CaO = CaCO3 3.Реагирует с щелочами CO2 + 2KOH = K2CO3 + H2O 4.Реагирует с углеродом CO2 + C = 2CO
Слайд 18

Химические свойства карбонатов (солей угольной кислоты)
1.Качественной реакцией на карбонаты является реакция с кислотами CaCO3 + 2HCL = CaCL2 + H2O + CO2 2. Нерастворимые в воде карбонаты термически неустойчивы CaCO3 = CaO + CO2 3.Карбонаты реагируют с солями Na2CO3 + BaCL2 = 2NaCL + BaCO3
1.Качественной реакцией на карбонаты является реакция с кислотами CaCO3 + 2HCL = CaCL2 + H2O + CO2 2. Нерастворимые в воде карбонаты термически неустойчивы CaCO3 = CaO + CO2 3.Карбонаты реагируют с солями Na2CO3 + BaCL2 = 2NaCL + BaCO3
Слайд 19

Углекислотный
огнетушитель
Сухой лед (хладагент)
Сода
Моющие средства
Лимонады
Соединения углерода вокруг нас
Сухой лед (хладагент)
Сода
Моющие средства
Лимонады
Соединения углерода вокруг нас
Слайд 20

http://urbanjewelers.biz/wp-content/uploads/2010/10/diamonds-e1288016603994.jpg
http://www.jabinesban.com/wp-content/uploads/2010/09/fullereno_fullereno.jpg
http://s58.radikal.ru/i160/1012/ff/2e7639eb01bc.jpg
http://www.rmnt.ru/pub/uploads/glass_cutter_0511_3.jpg
http://www.students.by/articles/19/1001931/PH04503.jpg
http://art-market.com.ua/media/catalog/product/cache/17/image/9df78eab33525d08d6e5fb8d27136e95/1/1/111111111111111_2.jpg
http://im5-tub-ru.yandex.net/i?id=42457246-63-72&n=21
Ссылки на источники информации и изображения:
И.И.Новошинский Н.С.Новошинская Химия 10 класс (профильный уровень)
http://www.jabinesban.com/wp-content/uploads/2010/09/fullereno_fullereno.jpg
http://s58.radikal.ru/i160/1012/ff/2e7639eb01bc.jpg
http://www.rmnt.ru/pub/uploads/glass_cutter_0511_3.jpg
http://www.students.by/articles/19/1001931/PH04503.jpg
http://art-market.com.ua/media/catalog/product/cache/17/image/9df78eab33525d08d6e5fb8d27136e95/1/1/111111111111111_2.jpg
http://im5-tub-ru.yandex.net/i?id=42457246-63-72&n=21
Ссылки на источники информации и изображения:
И.И.Новошинский Н.С.Новошинская Химия 10 класс (профильный уровень)
Слайд 21

http://im0-tub-ru.yandex.net/i?id=58758432-63-72&n=21
http://im2-tub-ru.yandex.net/i?id=584425754-01-72&n=21
http://im6-tub-ru.yandex.net/i?id=59807605-60-72&n=21
http://im7-tub-ru.yandex.net/i?id=28109246-51-72&n=21
http://im1-tub-ru.yandex.net/i?id=501551220-00-72&n=21
http://im5-tub-ru.yandex.net/i?id=51546160-51-72&n=21
http://im0-tub-ru.yandex.net/i?id=140463688-66-72&n=21
http://im4-tub-ru.yandex.net/i?id=412111321-54-72&n=21
http://im0-tub-ru.yandex.net/i?id=945542505-10-72&n=21
http://im6-tub-ru.yandex.net/i?id=795134635-71-72&n=21
http://im2-tub-ru.yandex.net/i?id=440598815-39-72&n=21
http://im2-tub-ru.yandex.net/i?id=584425754-01-72&n=21
http://im6-tub-ru.yandex.net/i?id=59807605-60-72&n=21
http://im7-tub-ru.yandex.net/i?id=28109246-51-72&n=21
http://im1-tub-ru.yandex.net/i?id=501551220-00-72&n=21
http://im5-tub-ru.yandex.net/i?id=51546160-51-72&n=21
http://im0-tub-ru.yandex.net/i?id=140463688-66-72&n=21
http://im4-tub-ru.yandex.net/i?id=412111321-54-72&n=21
http://im0-tub-ru.yandex.net/i?id=945542505-10-72&n=21
http://im6-tub-ru.yandex.net/i?id=795134635-71-72&n=21
http://im2-tub-ru.yandex.net/i?id=440598815-39-72&n=21
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.