Презентация - Открытый урок по химии «Оксиды»
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 95%
- Слайдов: 32
- Просмотров: 3703
- Скачиваний: 1559
- Размер: 1.54 MB
- Класс: 8
- Формат: ppt / pptx
Примеры похожих презентаций
 Открытый урок по химии 10 класс «Формулы и вещества»
Открытый урок по химии 10 класс «Формулы и вещества» Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека»
Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека» Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс
Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс Открытый урок по окружающему миру «Мхи - Лишайники - Водоросли - Папоротники»
Открытый урок по окружающему миру «Мхи - Лишайники - Водоросли - Папоротники» Отработка решения заданий ЕГЭ повышенного уровня на уроках химии
Отработка решения заданий ЕГЭ повышенного уровня на уроках химии Открытый урок «Логические операции»
Открытый урок «Логические операции» К открытому уроку «Природа и люди Древней Индии»
К открытому уроку «Природа и люди Древней Индии»
Слайды и текст этой онлайн презентации
Слайд 1

В чем горят дрова и газ, Фосфор, водород, алмаз? Дышит чем любой из нас Каждый миг и каждый час? Без чего мертва природа? Правильно без……….
Слайд 2

Автор :
Дидаева М. В.
учитель химии
МБОУ «СОШ № 5 с.Ачхой-Мартан»
Урок химии 8 класс «Свойства кислорода. Оксиды. »
МБОУ «СОШ № 5 с.Ачхой-Мартан»
Урок химии 8 класс «Свойства кислорода. Оксиды. »
Слайд 3

Девиз урока: «Кислород – это вещество,
вокруг которого вращается
земная химия».
Слайд 4

Тема: Свойства кислорода. Оксиды.
Цель: сформулировать у учащихся представление о кислороде, изучить его свойства, дать общее понятие об оксидах, окислении, рассмотреть практическую значимость и применение.
Цель: сформулировать у учащихся представление о кислороде, изучить его свойства, дать общее понятие об оксидах, окислении, рассмотреть практическую значимость и применение.
Слайд 5

Задачи:
Образовательные: познакомить учащихся с историей открытия кислорода,
именами ученых,
связанных с этим открытием,
общей характеристикой элемента и простого вещества,
изучить физические и химические свойства кислорода,
дать понятие об оксидах и окислении.
Познакомить учащихся с основными способами получения кислорода
в лаборатории и промышленности,
дать первоначальное понятие о катализаторе,
познакомить с нахождением кислорода в природе и его применением.
Слайд 6

Развивающие:
развитие навыков самостоятельной деятельности
через работу с учебником,
дополнительной литературой,
развитие познавательного интереса,
развитие логического мышления,
расширение кругозора.
Слайд 7

Воспитательные:
формирование основных мировоззренческих идеи
материальности мира,
воспитание настойчивости в овладении знаний,
самостоятельности, дисциплины, аккуратности,
воспитание любви к окружающей среде,
предмету.
Слайд 8
Физические свойства кислорода
История открытие кислорода
Кислород, общая характеристика
Окисление
Химические свойства кислорода
Получение кислорода.
кислород
История открытие кислорода
Кислород, общая характеристика
Окисление
Химические свойства кислорода
Получение кислорода.
кислород
Слайд 9

Слайд 10

Слайд 11

Слайд 12

Слайд 13

Нахождение в природе.
Кислород – самый распространённый
химический элемент в земной коре.
Воздух содержит 0,209 объёмных долей
или 20,9% кислорода,
что составляет
приблизительно 1/5 по объёму.
Слайд 14

Способы получения кислорода в лаборатории
1. Уравнения реакции получения кислорода разложением перманганата калия при нагревании
разложением некоторых кислород содержащих веществ 2H2O2 - 2Н2О + О2 пероксид вода кислород водорода 2KClO3 - 2KCl+ 3O2 хлорат хлорид кислород калия калия
1. Уравнения реакции получения кислорода разложением перманганата калия при нагревании
разложением некоторых кислород содержащих веществ 2H2O2 - 2Н2О + О2 пероксид вода кислород водорода 2KClO3 - 2KCl+ 3O2 хлорат хлорид кислород калия калия
Слайд 15

Способы получения кислорода в промышленности
1. Электролиз воды
1. Электролиз воды
Слайд 16

Физические свойства кислорода
Кислород – газ, состоящий из двухатомных молекул кислорода. Не имеет запаха и цвета. Кислород немного тяжелее воздуха: 1л кислорода при нормальных условиях весит 1,43г., 1л. воздуха – 1,29г.
Кислород – газ, состоящий из двухатомных молекул кислорода. Не имеет запаха и цвета. Кислород немного тяжелее воздуха: 1л кислорода при нормальных условиях весит 1,43г., 1л. воздуха – 1,29г.
Слайд 17

Химические свойства
.
Горение – это химическая реакция, при которой происходит окисление веществ с выделением теплоты и света.
.
Горение – это химическая реакция, при которой происходит окисление веществ с выделением теплоты и света.
Слайд 18

Взаимодействие с серой
IV II S + O2 S O
S + O2 = S O2
IV II S + O2 S O
S + O2 = S O2
Слайд 19

2. Взаимодействие с фосфором
v II
P + O2 → P O
Слайд 20

ВЗАИМОДЕЙСТВИЕ ПРОСТЫХ И СЛОЖНЫХ ВЕЩЕСТВ С КИСЛОРОДОМ НАЗЫВАЕТСЯ ОКИСЛЕНИЕМ. ГОРЕНИЕ —ХИМИЧЕСКАЯ РЕАКЦИЯ,ПРИ КОТОРОЙ ПРОИСХОДИТ ОКИСЛЕНИЕ ВЕЩЕСТВ С ВЫДЕЛЕНИЕМ ТЕПЛА И СВЕТА.
Слайд 21

SO2
- оксид серы(IV)
P2O5
- оксид фосфора(V)
Fe O
- оксид железа(II)
Fe2O3
- оксид железа(III)
Оксиды – это сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
- оксид серы(IV)
P2O5
- оксид фосфора(V)
Fe O
- оксид железа(II)
Fe2O3
- оксид железа(III)
Оксиды – это сложные вещества, которые состоят из двух элементов, одним из которых является кислород.
Слайд 22
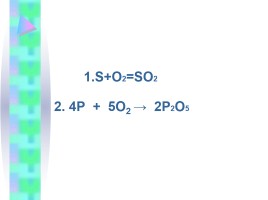
1.S+O2=SO2
2. 4P + 5O2 → 2P2O5
Слайд 23

ТЕСТ.
1. Самый распространенный х.э.: а) водород в) кремний б) кислород г) алюминий 2. Химический элемент кислород в природе распространен по массе: а) 59% в) 49% б) 94% г) 19%
1. Самый распространенный х.э.: а) водород в) кремний б) кислород г) алюминий 2. Химический элемент кислород в природе распространен по массе: а) 59% в) 49% б) 94% г) 19%
Слайд 24

9. В лаборатории кислород получают: а) р.соединения б) р.разложения в) р.замещения г) р.обмена 10. В промышленности кислород получают: а) разложением воды б) разложением КМnO4 в) из воздуха
Слайд 25

3. Впервые кислород получил:
а) А.Лавуазье в)М.Ломоносов
б) Д.Пристли г) Р.Бойль
4. Относительная атомная масса кислорода:
а) 8 в) 16
б) 32 г) 15
Слайд 26

5. Валентность кислорода в соединениях: а) II в) III б) I г) V 6. Формула простого вещества кислорода: а) О в) Н2 б) О2 г) О3
Слайд 27

7. Относительная молекулярная масса кислорода: а) 8 в) 32 б) 16 г) 23 8. Определяют кислород: а) по цвету б) по запаху в) по вкусу г) тлеющей лучинкой
Слайд 28

Вопросы для закрепления.
Из перечисленных формул веществ выпишите оксиды, и назовите их: HCl, SO3, KOH, CO2, HBr, ZnO, NaOH, H2SO4, MgO, Al2O3, ZnS, K2O.
Из перечисленных формул веществ выпишите оксиды, и назовите их: HCl, SO3, KOH, CO2, HBr, ZnO, NaOH, H2SO4, MgO, Al2O3, ZnS, K2O.
Слайд 29

Слайд 30

Вопросы к кроссворду: 1. Процесс взаимодействия простых и сложных веществ с кислородом. 2. Английский ученный открывший кислород. 3. Вещество поддерживающее горение. 4. Тип реакции 2Н2О→2Н2+О2. 5. вещества, получающиеся при горении. 6. Процесс сопровождающийся выделением тепла. 7. Тип реакции горения серы. 8. Самое распространенное вещество содержащее кислород.
Слайд 31

Ответить на вопросы.
Назовите химический элемент, наиболее распространенный в земной коре? В состав, каких соединений входит этот элемент? 2) Как получают кислород в лаборатории? 3) Что такое катализаторы, и каково их значение в химических процессах? 4) Охарактеризуйте химические и физические свойства кислорода. 5) Какие процессы относятся к процессам окисления? Какие вещества называются оксидами?
Назовите химический элемент, наиболее распространенный в земной коре? В состав, каких соединений входит этот элемент? 2) Как получают кислород в лаборатории? 3) Что такое катализаторы, и каково их значение в химических процессах? 4) Охарактеризуйте химические и физические свойства кислорода. 5) Какие процессы относятся к процессам окисления? Какие вещества называются оксидами?
Слайд 32

Домашнее задание: § 20,21 пересказ,
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
