Слайды и текст этой онлайн презентации
Слайд 1
Тепловые явления
Способы изменения внутренней энергии
Слайд 2
Внутренняя энергия
Это совокупность потенциальных и кинетических энергий всех молекул, составляющих тело.
U = ∑EP + ∑Ek
Слайд 3
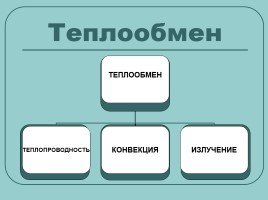
Способы изменения внутренней энергии
Работа
Теплообмен
Слайд 4
Работа
Способ изменения внутренней энергии, когда над телом совершается работа.
Слайд 8
Излучение
Земля обогревается благодаря излучению Солнца
Тепло от огня распространяется во все стороны
Слайд 9
Количество теплоты
Изменение внутренней энергии в результате теплообмена.
Слайд 10
Количество теплоты
Q = c·m·(t2-t1), где
с- удельная теплоемкость вещества
(эксперимент, таблица)
Слайд 11
Тепловые явления
Энергия топлива
Слайд 12
Энергия топлива
Энергией топлива называется количество теплоты, выделяющееся при сгорании топлива
Слайд 13
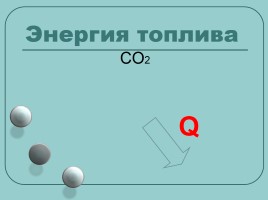
Энергия топлива
Q
CO2
Слайд 14
Энергия топлива
Q = qm
Слайд 15
Энергия топлива пример решения задачи
Дано: Решение:
m = 100 кг Q = qm;
q = 29·106 Дж/кг Q = 29·106 Дж/кг· 100 кг =
______________ = 29·108 Дж
Q - ?
Ответ: Q = 9·108 Дж Ответ: Q = 9·108 Дж
Какое количество теплоты выделится при сгорании 100 кг каменного угля?
Слайд 16
Закон сохранения тепловой энергии
В замкнутой теплоизолированной системе внутренняя энергия остается постоянной.
Q = Q1+Q2+…+Qn
Слайд 17
Тепловые явления
Изменения агрегатных состояний вещества
Слайд 18
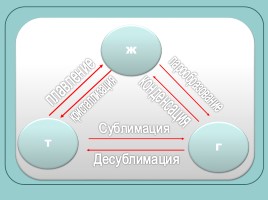
Ж
Г
Т
плавление
кристаллизация
парообразование
конденсация
Десублимация
Сублимация
Слайд 19
Примеры процессов, при которых происходят агрегатные превращения вещества
Плавление - таяние льда
Слайд 20
Кристаллизация
Замерзание воды
Слайд 21
Парообразование
Испарение воды, выбрасываемой гейзером
Слайд 22
Конденсация
Образование облаков
Слайд 23
Сублимация
Например, графит можно нагреть до тысячи градусов, и тем не менее в жидкость он не превратится: он будет сублимироваться, т.е. из твёрдого состояния сразу переходить в газообразное. Все запахи, которыми обладают твёрдые тела, также обусловлены возгонкой: вылетая из твёрдого тела молекулы образуют над ним газ (или пар), который и вызывает ощущение запаха.
Слайд 24
Десублимация
Узоры на окнах
Слайд 25
Тепловые явления
Плавление и кристаллизация
Слайд 26
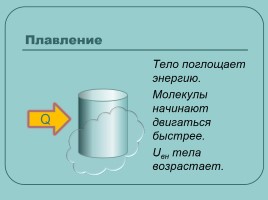
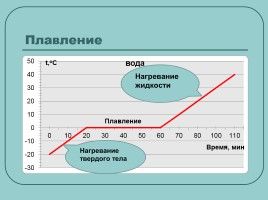
Плавление
Тело поглощает энергию.
Молекулы начинают двигаться быстрее.
Uвн тела возрастает.
Q
Слайд 28
Плавление
Плавление происходит при постоянной температуре (tпл - таблица).
При плавлении температура тела остается постоянной в течение всего процесса.
Вся поступающая к телу энергия расходуется на разрушение кристаллических связей.
Слайд 29
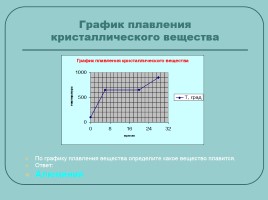
График плавления кристаллического вещества
По графику плавления вещества определите какое вещество плавится.
Ответ:
Алюминий
Слайд 30
Плавление
Количество теплоты при плавлении
λ - удельная теплота плавления
(эксперимент, таблица)
Q = λ·m
Слайд 31
Тепловые явления
Парообразование
Слайд 33
Испарение
Испарение – парообразование с поверхности жидкости
Скорость парообразования зависит от:
Температуры тела;
Площади поверхности испарения;
Рода вещества;
Наличие ветра.
Слайд 34
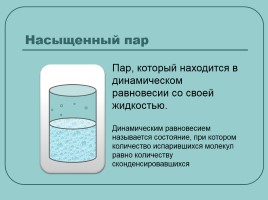
Насыщенный пар
Пар, который находится в динамическом равновесии со своей жидкостью.
Динамическим равновесием называется состояние, при котором количество испарившихся молекул равно количеству сконденсировавшихся
Слайд 35
Кипение
Процесс бурного парообразования с образованием пузырьков внутри жидкости
Понимающиеся пузырьки схлопываются перед кипением, что вызывает характерный шум жидкости перед закипанием.
Слайд 36
Температура кипения
Кипение происходит при постоянной температуре, называемой температурой кипения
tºкип – эксперимент, таблица
Слайд 37
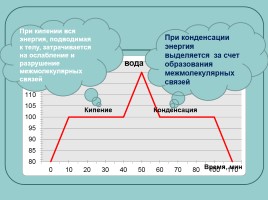
Кипение
Конденсация
При конденсации энергия выделяется за счет образования межмолекулярных связей
При кипении вся энергия, подводимая к телу, затрачивается на ослабление и разрушение межмолекулярных связей
Слайд 38
Удельная теплота парообразования
L – эксперимент, таблица
Определяет какое количество теплоты необходимо передать жидкости массой 1 кг, взятой при температуре кипения, для полного ее перехода в пар.
Слайд 39
Количество теплоты при парообразовании
Q = m L
Для нахождения количества теплоты при парообразовании произвольной массы данного вещества нужно массу вещества m, выраженную в кг, умножить на удельную теплоту парообразования L соответствующего вещества
Слайд 40
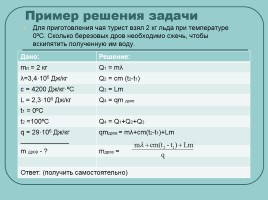
Пример решения задачи
Для приготовления чая турист взял 2 кг льда при температуре 0ºС. Сколько березовых дров необходимо сжечь, чтобы вскипятить полученную им воду.
Дано: Решение:
mл = 2 кг Q1 = mλ
λ=3,4·106 Дж/кг Q2 = cm (t2-t1)
с = 4200 Дж/кг·ºС Q3 = Lm
L = 2,3·106 Дж/кг Q4 = qm дров
t1 = 0ºC
t2 =100ºC Q4 = Q1+Q2+Q3
q = 29·106 Дж/кг
_____________ qmдров = mλ+cm(t2-t1)+Lm
m дров - ? mдров =
Ответ: (получить самостоятельно) Ответ: (получить самостоятельно)
 Способы изменения внутренней энергии
Способы изменения внутренней энергии Тепловые явления. Изменение агрегатных состояний веществ
Тепловые явления. Изменение агрегатных состояний веществ Тепловые явления. Изменение агрегатных состояний вещества (11 класс)
Тепловые явления. Изменение агрегатных состояний вещества (11 класс) Энергия топлива. Удельная теплота сгорания топлива. Закон сохранения и превращения энергии в механических и тепловых процессах
Энергия топлива. Удельная теплота сгорания топлива. Закон сохранения и превращения энергии в механических и тепловых процессах Внутренняя энергия
Внутренняя энергия Внутренняя энергия
Внутренняя энергия Способы тепловой кулинарной обработки сырья
Способы тепловой кулинарной обработки сырья