Слайды и текст этой онлайн презентации
Слайд 1
Кислоты
Урок-путешествие
по химии в 8 классе
учитель
Самсонова Л.В.
Слайд 2
«Просто знать- ещё не всё, знания нужно уметь использовать»
Слайд 3
Цели: сформировать понятия «кислота»,
«кислородсодержащие и бескислородные кислоты»,
«основность кислоты», умение эксперементально
определять кислоты среди других веществ, продолжить
умение работать с веществами, соблюдая правила
техники безопасности.
Слайд 4
Задачи:
Что мы вкладываем в смысл слова кислота?
По каким признакам можно класси-фицировать кислоты?
Какие особенные физические свойст-ва характерны для кислот?
Как определить растворы кислот среди растворов других веществ?
Слайд 5
Проверка домашнего задания
Упр.2
Cr (II)
Cr(OH)2
Cu (I)
CuOH
Ответ: основания окраску индикаторов не изменяют, т.к. являются
нерастворимыми.
Упр. 5
Дано:
m(NaOH)=120г
m(Cu(OH)2 )=49г
n(NaOH)=?
n(Cu(OH)2)=?
Решение:
n=
m
M
n(NaOH)=
120
M(23+16+1)
=3 моль
n(Cu(OH)2)=
49
М(64+(16+1)*2)
=0,5 моль
Ответ: 3 моль; 0,5 моль.
Станция Посадочная.
Слайд 6
Станция Успешная
Написать формулы оксидов.
Оксид серы(Vl)
Оксид фосфора(V)
Оксид железа(l l)
SO3
P2O5
FeO
Написать формулы оснований.
Гидроксид алюминия
Гидроксид натрия
Гидроксид марганца (II)
Al(OH)3
NaOH
Mn(OH)2
Слайд 7
Станция Информационная
Что нас объединяет?
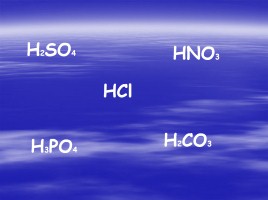
Слайд 8
H2SO4
HNO3
HCl
H3PO4
H2CO3
Слайд 10
Кислоты – это сложные вещества, молекула которых состоит из одного или нескольких атомов водорода и кислотного остатка.
Слайд 13
H3BO3
Борная кислота
Слайд 15
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ
Едкое вещество—кислота! Разрушает и раздражает кожу, слизистые оболочки.
Попавшие на кожу капли раствора кислоты немедленно смойте сильной струей холодной воды, а затем обработайте поврежденную поверхность 2%-м раствором питьевой соды.
Станция Безопасная
Слайд 16
Окраска лакмуса и метилоранжа в кислотах
лакмус
метилоранж
Слайд 17
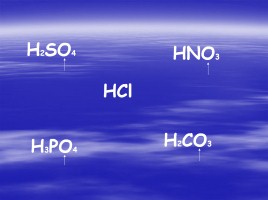
H2SO4
HNO3
HCl
H3PO4
H2CO3
Слайд 18
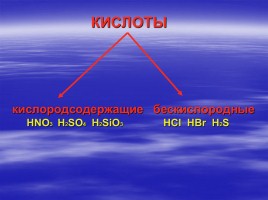
КИСЛОТЫ кислородсодержащие бескислородные HNO3 H2SO4 H2SiO3 HCl HBr H2S
Слайд 19
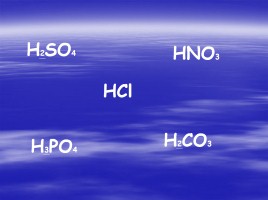
H2SO4
HNO3
HCl
H3PO4
H2CO3
Слайд 20
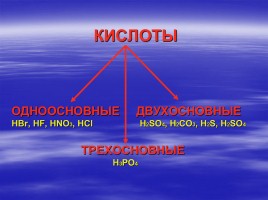
КИСЛОТЫ ОДНООСНОВНЫЕ ДВУХОСНОВНЫЕ HBr, HF, HNO3, HCl H2SO4, H2CO3, H2S, H2SO4 ТРЕХОСНОВНЫЕ H3PO4
Слайд 21
Д.И. Менделеев (1834 — 1907 гг.)
«Я не льщусь порывами дойти до
общего.»
Слайд 22
Кислоты делятся на кислород-содержащие и бескислородные по наличию кислорода; на од-ноосновные, двухосновные и трехосновные по количеству атомов водорода.
Станция Заключительная
Слайд 23
Станция рефлексивная
Что тебе удалось на уроке?
За что ты можешь себя похвалить?
Над чем еще нужно поработать?
Зачем тебе нужен был этот урок?
 Урок-путешествие «Страна Лексика»
Урок-путешествие «Страна Лексика» Урок-игра по математике в 5 классе «Космическое путешествие»
Урок-игра по математике в 5 классе «Космическое путешествие» К уроку Путешествие
К уроку Путешествие Урок-путешествие «Части слова»
Урок-путешествие «Части слова» Путешествие по школьной стране. Урок знаний в 4 классе
Путешествие по школьной стране. Урок знаний в 4 классе Урок химии в 10-м классе по теме «Аминокислоты»
Урок химии в 10-м классе по теме «Аминокислоты» Урок 3 класс. Урок – путешествие. Мифы древней греции «решение уравнений»
Урок 3 класс. Урок – путешествие. Мифы древней греции «решение уравнений»