Слайды и текст этой онлайн презентации
Слайд 1
Кристаллические и аморфные тела
Поверхностное натяжение жидкостей
Слайд 2
Основные состояния вещества
Газообразное
Жидкое
Твердое
Кристаллы Аморфные тела
Любое вещество может находиться в 3-х агрегатных состояниях, в зависимости от условий (температуры и давления)
Плазма
Слайд 3
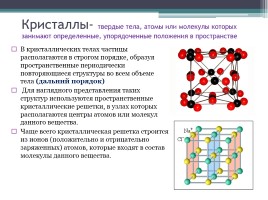
Кристаллы- твердые тела, атомы или молекулы которых занимают определенные, упорядоченные положения в пространстве
В кристаллических телах частицы располагаются в строгом порядке, образуя пространственные периодически повторяющиеся структуры во всем объеме тела (дальний порядок)
Для наглядного представления таких структур используются пространственные кристаллические решетки, в узлах которых располагаются центры атомов или молекул данного вещества.
Чаще всего кристаллическая решетка строится из ионов (положительно и отрицательно заряженных) атомов, которые входят в состав молекулы данного вещества.
Слайд 4
Кристаллы
Плавятся при определенной температуре (температуре плавления)
Свойства кристалла зависят
от типа кристаллической
решетки
Монокристалл – это одиночный кристалл
Физические свойства:
1)Правильная геометрическая форма
2)Постоянная температура плавления.
Слайд 5
Кристаллические решетки
Молекулярная
Атомная
Металлическая
Ионная
В узлах располагаются молекулы. Между ними действуют слабые силы притяжения, поэтому вещества летучи, у них низкие температуры плавления и кипения, малая твердость. Лед, йод. В узлах находятся отдельные атомы. Связи между ними самые прочные, поэтому вещества самые твердые, в воде не растворяются, у них высокие температуры плавления и кипения. Алмаз (углерод) В узлах находятся атомы металлов, легко переходящие в ионы, при отдаче электронов в общее пользование. Вещества ковкие, пластичные, имеют металлический блеск, высокую тепло- и электропроводность В узлах находятся положительные и отрицательные ионы. Связь между ними прочная, поэтому вещества обладают высокой твердостью, тугоплавкостью, нелетучие, но многие могут растворяться в воде. Хлорид натрия (соль)
Слайд 7
Колумбийский изумруд
Шапка Мономаха
Слайд 8
Поликристаллы
Поликристалл висмута
Аметист(разновидность кварца)
Поликристаллы – это твёрдые тела, состоящие из большого числа маленьких кристалликов. Примеры: металлы, кусочек сахара.
Слайд 9
Анизотропия кристалла- зависимость физических свойств от направления внутри кристалла
Различная механическая прочность по разным направлениям (слюда, графит)
Разные тепло – и электро- проводимости
Различные оптические свойства кристалла (разная преломляемость света - кварц)
Все кристаллические тела анизотропны
Слайд 10
Аморфные тела
Это твёрдые тела , где сохраняется только ближний порядок в расположении атомов.
(Кремнезём, смола, стекло, канифоль, сахарный леденец) .
Они не имеют постоянной температуры плавления и обладают текучестью.
При низких температурах они ведут себя подобно кристаллическим телам, а при высокой подобны жидкостям.
Слайд 11
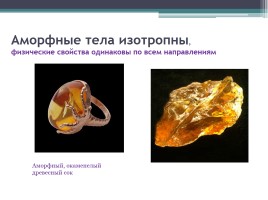
Аморфные тела изотропны, физические свойства одинаковы по всем направлениям
Аморфный, окаменелый древесный сок
Слайд 12
Жидкие кристаллы
Обладают одновременно
свойствами кристалла и
жидкости (анизотропией и текучестью)
Жидкие кристаллы – в основном органические вещества, молекулы которых имеют длинную нитевидную форму или форму плоских пластин
Слайд 13
Жидкости
В жидкостях наблюдается ближний порядок - упорядоченное относительное расположение (или взаимная ориентация в жидких кристаллах) соседних частиц жидкости внутри малых ее объемов
Слайд 14
Жидкости
Строение сходно со строением аморфных тел
Отличие: обладают большой текучестью
Слайд 15
Жидкость
Поверхностные явления – это
явления, связанные с существованием у жидкости свободной поверхности.
Избыточная энергия, которой обладают молекулы поверхностного слоя по сравнению с молекулами в толще жидкости, называется поверхностной (избыточной) энергией.
Удельная поверхностная энергия - отношение поверхностной энергии к площади поверхности σ= Е пов/s
[σ]=1 Дж/м2
Слайд 16
На поверхности жидкости остается такое количество молекул, при котором ее площадь остается минимальной для данного объема жидкости.
Капли жидкости принимают форму, близкую к шарообразной, при которой
площадь поверхности минимальна.
Собственная форма - шарообразная
Поверхностное натяжение-явление
вызванное притяжением молекул
поверхностного слоя к молекулам
внутри жидкости.
Сила поверхностного натяжения- сила,
направленная по касательной к
поверхности жидкости, перпендикулярно участку контура, ограничивающего поверхность, в сторону ее сокращения.
Слайд 17
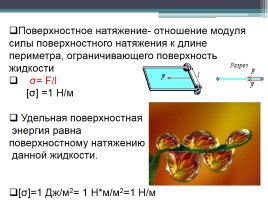
Поверхностное натяжение- отношение модуля силы поверхностного натяжения к длине периметра, ограничивающего поверхность жидкости
σ= F/l
[σ] =1 Н/м
Удельная поверхностная
энергия равна
поверхностному натяжению
данной жидкости.
[σ]=1 Дж/м2= 1 Н*м/м2=1 Н/м
Слайд 18
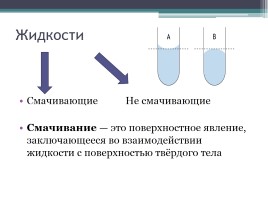
Жидкости
Смачивающие Не смачивающие
Смачивание — это поверхностное явление, заключающееся во взаимодействии жидкости с поверхностью твёрдого тела
Слайд 19
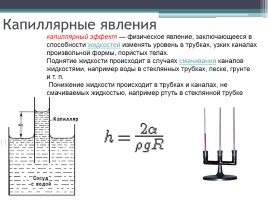
Капиллярные явления
капиллярный эффект — физическое явление, заключающееся в способности жидкостей изменять уровень в трубках, узких каналах произвольной формы, пористых телах.
Поднятие жидкости происходит в случаях смачивания каналов жидкостями, например воды в стеклянных трубках, песке, грунте и т. п.
Понижение жидкости происходит в трубках и каналах, не смачиваемых жидкостью, например ртуть в стеклянной трубке
Слайд 20
Плазма
ПЛАЗМА – частично или полностью ионизованный
газ, образованный из нейтральных
атомов
(или молекул)
и заряженных
частиц (ионов и
электронов
 Аморфные тела
Аморфные тела Давление твердого тела, газа и жидкостей
Давление твердого тела, газа и жидкостей Лабораторная работа №9 «Выяснение условий плавания тела в жидкости»
Лабораторная работа №9 «Выяснение условий плавания тела в жидкости» Решение экспериментальных задач по теме «Давление в твердых телах, жидкостях и газах»
Решение экспериментальных задач по теме «Давление в твердых телах, жидкостях и газах» Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах
Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах Диффузия в газах, жидкостях и твердых телах
Диффузия в газах, жидкостях и твердых телах Импульс тела (примеры на закон сохранения импульса)
Импульс тела (примеры на закон сохранения импульса)