Презентация - Занятие 1. Световая микроскопия
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 96%
- Слайдов: 41
- Просмотров: 2908
- Скачиваний: 909
- Размер: 15.18 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Занятие на развитие памяти, внимания, мышления
Занятие на развитие памяти, внимания, мышления Использование материала по страноведению на занятиях по английскому языку как средство приобщения учащихся к иноязычной культуре
Использование материала по страноведению на занятиях по английскому языку как средство приобщения учащихся к иноязычной культуре Конспект-презентация занятия по развитию лексико-грамматических категорий и связной речи в старшей группе по теме «Овощи»
Конспект-презентация занятия по развитию лексико-грамматических категорий и связной речи в старшей группе по теме «Овощи» Основные направления работы по обеспечению двигательной активности на логопедических занятиях на основании технологии В.Г.Алямовской. М.Н. Чернышова
Основные направления работы по обеспечению двигательной активности на логопедических занятиях на основании технологии В.Г.Алямовской. М.Н. Чернышова К занятию по теме Мой дом
К занятию по теме Мой дом Готовимся к школе «Занятие 12»
Готовимся к школе «Занятие 12» Алгоритм действий юридического лица при обращении через портал электронного правительства для получения лицензии на право занятия охранной деятельностью
Алгоритм действий юридического лица при обращении через портал электронного правительства для получения лицензии на право занятия охранной деятельностью
Слайды и текст этой онлайн презентации
Слайд 1

Занятие 1.
Световая микроскопия Доронина Татьяна Валерьевна 2019 год Московский государственный университет имени М. В. Ломоносова Биологический факультет Кафедра клеточной биологии и гистологии
Слайд 2

Строение светового микроскопа предметный столик узел смены объективов объективы окуляры конденсор тубусодержатель основание макро- и микровинты регулятор интенсивности света источник света бинокулярная насадка
Слайд 3
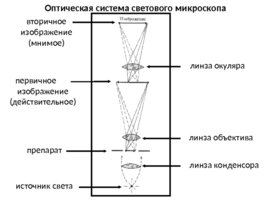
Оптическая система светового микроскопа источник света линза конденсора линза объектива препарат линза окуляра первичное изображение (действительное) вторичное изображение (мнимое)
Слайд 4
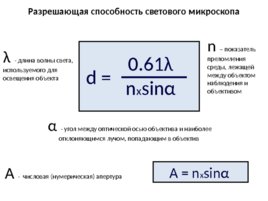
Разрешающая способность светового микроскопа 0.61λ n x sinα d α - угол между оптической осью объектива и наиболее отклоняющимся лучом, попадающим в объектив n – показатель преломления среды, лежащей между объектом наблюдения и объективом λ - длина волны света, используемого для освещения объекта А - числовая (нумерическая) апертура А n x sinα
Слайд 5

Слайд И. А. Воробьева
Слайд 6
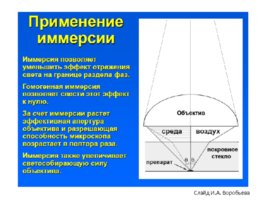
Слайд И. А. Воробьева
Слайд 7
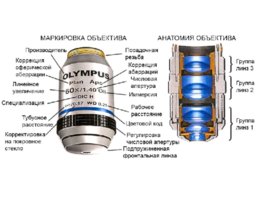
Слайд 8
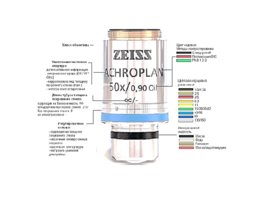
Слайд 9

Общие правила работы с микроскопом Нельзя переносить микроскоп за «горловину»: необходимо всегда второй рукой поддерживать его снизу . При работе с микроскопом нельзя применять большие усилия. Ни в коем случае нельзя касаться пальцами поверхности линз, зеркал и светофильтров . Чтобы предохранить внутренние поверхности объективов, а также призмы тубуса от попадания пыли, необходимо всегда оставлять окуляр в тубусе . Объективы должны находится в чистом состоянии. По окончании работы на микроскопе необходимо тщательно удалить остатки иммерсионного масла с фронтальной линзы объектива. После окончания работы на препарат должен был наведен объектив с малым увеличением. Нельзя оставлять «смотрящим вниз» объектив с увеличением 40х или 90х. Запрещается использовать иммерсионную жидкость с неиммерсионными объективам и .
Слайд 10
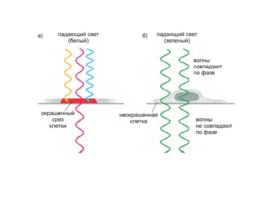
Слайд 11
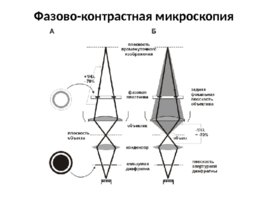
Фазово-контрастная микроскопия
Слайд 12
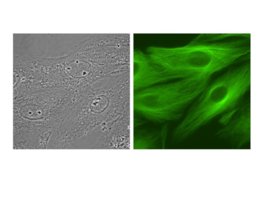
Слайд 13

Флуоресцентная микроскопия
Слайд 14
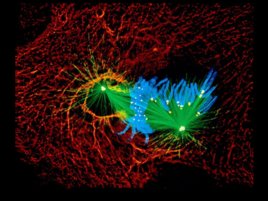
Слайд 15
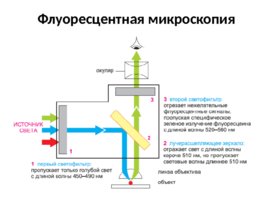
Флуоресцентная микроскопия
Слайд 16
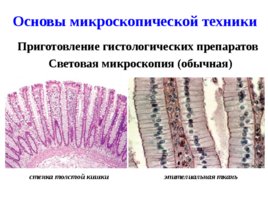
Основы микроскопической техники Приготовление гистологических препаратов Световая микроскопия (обычная) эпителиальная ткань стенка толстой кишки
Слайд 17

Мазки (костный мозг, кровь, ликвор); Пленки (брыжейки, нервная ткань); Отпечатки (печень, селезенка); Клетки культур; Гистологические срезы; Давленые препараты; Живые клетки (окрашенные с помощью витальных красителей) Витальные красители Акридиновый оранжевый (ядро) Янус зеленый (митохондрии) Нейтральный красный (лизосомы) Объекты
Слайд 18

Гистологические препараты постоянные временные живые клетки нужна фиксация клеток
Слайд 19
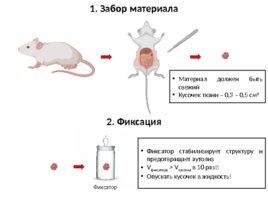
1. Забор материала Фиксатор стабилизирует структуру и предотвращает аутолиз V фиксатора V кусочка в 10 раз!! Опускать кусочек в жидкость! 2. Фиксация Фиксатор Материал должен быть свежий Кусочек ткани – 0,3 – 0,5 см 3
Слайд 20
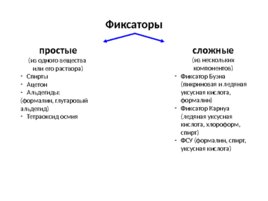
Фиксаторы простые (из одного вещества или его раствора) Спирты Ацетон Альдегиды: (формалин, глутаровый альдегид) Тетраоксид осмия cложные (из нескольких компонентов) Фиксатор Буэна (пикриновая и ледяная уксусная кислота, формалин) Фиксатор Карнуа (ледяная уксусная кислота, хлороформ, спирт) ФСУ (формалин, спирт, уксусная кислота)
Слайд 21
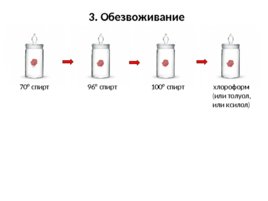
3. Обезвоживание 70 спирт 96 спирт 100 спирт хлороформ (или толуол, или ксилол)
Слайд 22
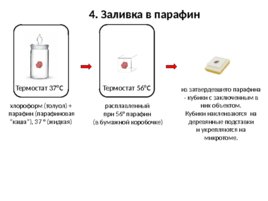
4. Заливка в парафин хлороформ (толуол) парафин (парафиновая каша ), 37 (жидкая) расплавленный при 56 парафин (в бумажной коробочке) из затвердевшего парафина - кубики с заключенным в них объектом. Кубики наклеиваются на деревянные подставки и укрепляются на микротоме. Термостат 37 С Термостат 56 С
Слайд 23

5. Получение срезов на микротоме 6. Наклеивание срезов на предметное стекло Получение срезов толщиной 2-4 мкм. Ленту срезов переносят на предметное стекло, заранее смазанное белком, расправляют под бинокуляром с помощью препаровальных игл и кладут на нагревательный столик (37 ), чтобы срезы хорошо присохли. нагревательный столик
Слайд 24

7. Депарафинирование 70 спирт 96 спирт 100 спирт 2 смены хлороформ (или толуол, или ксилол) 2 смены дистиллированная вода Для того чтобы срез ткани, залитый в парафин, окрасить, его надо подвергнуть обработке, в результате которой из среза удаляется парафин, препятствующий проникновению красителя, и ткань пропитывается водой, после чего может быть окрашена водными красителями
Слайд 25

8. Окрашивание Ядерные красители Цитоплазматические красители основные протравные (образуют с нуклеиновыми кислотами и кислыми белками ядра солеобразные соединения) азур, толуидиновый синий, метиленовый синий, метиловый зеленый, и др. гематоксилин, кармин, ализарин и др. В основном представляют собой карбоновые или сульфоновые кислоты, которые в тканях связываются с основными белками цитоплазмы, содержащими аргинин, лизин, оксилизин, гистидин. эозин, кислый фуксин, светлый зеленый и др.
Слайд 26
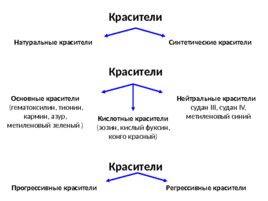
Красители Натуральные красители Синтетические красители Красители Основные красители (гематоксилин, тионин, кармин, азур, метиленовый зеленый ) Нейтральные красители судан III, судан IV, метиленовый синий Кислотные красители (эозин, кислый фуксин, конго красный) Красители Прогрессивные красители Регрессивные красители
Слайд 27

Гематоксилин Кампешевое дерево (Южная Америка) Гематоксилин (бесцветный) Гематеин (окрашен) С протравой гематеин образует солеобразное соединение – лак, которое окрашивает ядра
Слайд 28
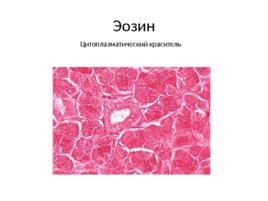
Эозин Цитоплазматический краситель
Слайд 29
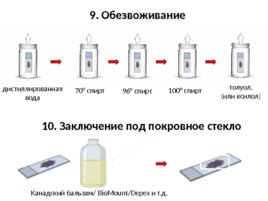
70 спирт 96 спирт 100 спирт толуол, (или ксилол) дистиллированная вода 9. Обезвоживание 10. Заключение под покровное стекло Канадский бальзам/ Bio Mount/Depex и т.д.
Слайд 30
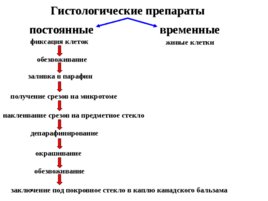
Гистологические препараты постоянные временные живые клетки фиксация клеток обезвоживание заливка в парафин получение срезов на микротоме наклеивание срезов на предметное стекло депарафинирование окрашивание обезвоживание заключение под покровное стекло в каплю канадского бальзама
Слайд 31

Культура клеток и тканей Клетки могут расти в культуре в течение длительного времени, если: снабжать клетки необходимыми питательными веществами обеспечить асептические условия на всех стадиях работы
Слайд 32
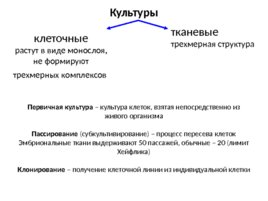
Культуры клеточные растут в виде монослоя, не формируют трехмерных комплексов тканевые трехмерная структура Первичная культура – культура клеток, взятая непосредственно из живого организма Пассирование (субкультивирование) – процесс пересева клеток Эмбриональные ткани выдерживают 50 пассажей, обычные – 20 (лимит Хейфлика) Клонирование – получение клеточной линии из индивидуальной клетки
Слайд 33
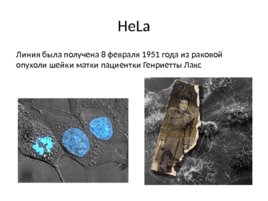
He La Линия была получена 8 февраля 1951 года из раковой опухоли шейки матки пациентки Генриетты Лакс
Слайд 34
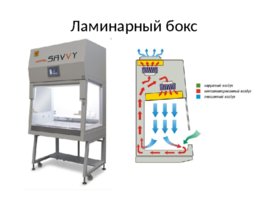
Ламинарный бокс
Слайд 35

Ламинарный бокс
Слайд 36
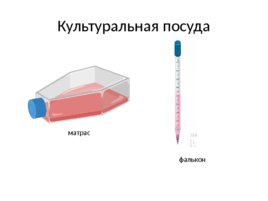
Культуральная посуда матрас фалькон
Слайд 37
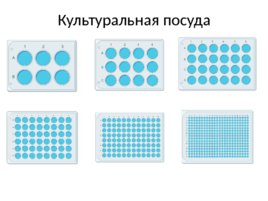
Культуральная посуда
Слайд 38

Культуральная среда раствор аминокислот, витаминов, глюкозы и т.д. на основе сбалансированного буферного раствора (обеспечивает осмотическое давление ) p H 7.2-7.5 (достигается с помощью системы бикарбонат натрия/СО2 )
Слайд 39

Для нормального роста клеток нужны: Культуральная среда Сыворотка L-глутамин (добавлять перед началом работы со средой, т.к. в водном растворе быстро разлагается) Антибиотики (обеспечение стерильности)
Слайд 40
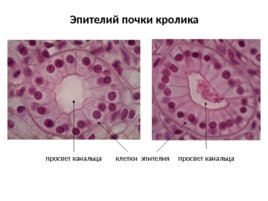
Эпителий почки кролика просвет канальца просвет канальца клетки эпителия
Слайд 41

^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
