Слайды и текст этой онлайн презентации
Слайд 1
Давление идеального газа. Основное уравнение МКТ.
План.
Задача урока.
Некоторые понятия теории вероятности.
Среднее значение квадрата скорости.
Давление идеального газа.
Вывод основного уравнения МКТ.
Применение основного уравнения МКТ к решению задачи.
Слайд 2
Задача урока :
Задача урока :
Пользуясь моделью идеального газа вычислить с помощью МКТ давление разреженного газа на стенки сосуда.
В чем трудность выполнения этой задачи?
Слайд 3
Трудности выполнения задачи: в движении принимает участие огромное количество частиц, движение которых нельзя описать с помощью законов механики Ньютона (описывается статистическими законами).
Статистические закономерности изучаются теорией вероятности.
Слайд 4
Некоторые понятия теории вероятности:
Событие (случай) – всякие явления которые могут происходить с системой.
Испытание – опыт или совокупность условий, в результате которого наступает то или иное событие.
Если событие при данном условии обязательно происходит, то оно называется достоверным (вероятность достоверного события равна 1)
Если оно произойти не может, то его называют невозможным (вероятность невозможного события равна 0).
Если событие в результате испытания может произойти, а может и не произойти, то событие называется случайным (вероятность случайного события есть количественная мера ожидаемой возможности его появления).
Слайд 5
Доска Гальтона
Попадание дробинок в тот или иной желоб представляет случайное событие.
Наблюдаемое относительное распределение всех дробинок по желобам является закономерным.
Слайд 6
Поведение частиц идеального газа можно предсказать с некоторой вероятностью.
В связи с этим вводятся не точные характеристики каждой молекулы, а средние значения физических величин.
Среднее значение квадрата скорости
V2=(V21+ V22+… V2n)/N
V2x=1/3V2
Слайд 7
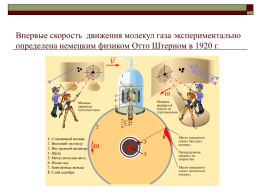
Впервые скорость движения молекул газа экспериментально определена немецким физиком Отто Штерном в 1920 г.
Слайд 8
Из опыта вытекают следующие выводы:
Распределение по скоростям подчиняется определенным закономерностям.
Значение скорости большинства молекул близки к некоторому значению, называемому наиболее вероятным.
При повышении температуры скорость молекул возрастает.
Скорости молекул постоянно меняются, но средний квадрат скорости вполне определенная величина.
Слайд 9
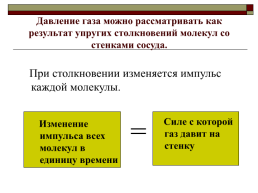
Давление газа можно рассматривать как результат упругих столкновений молекул со стенками сосуда.
При столкновении изменяется импульс каждой молекулы.
=
Силе с которой газ давит на стенку
Изменение импульса всех молекул в единицу времени
Слайд 10
(mV-mV0 )/Dt=f – сила давления одной
молекулы
F=f*N – сила давления N молекул,
где N=nV=nSVt,
p=F/S – сила действующая на единицу
площади (давление газа)
Слайд 11
В результате вычислений получаем основное уравнение МКТ
Слайд 12
Обозначим E=m0V2 /2 – среднюю кинетическую энергию поступательного движения молекул
Тогда
p=2/3nE
Слайд 13
Давление идеального газа на стенки сосуда зависит от:
Концентрации молекул.
Средней кинетической энергии молекул.
Слайд 14
Решение задач.
Плотность газа в балоне газополной электрической лампы 0,9 кг/м3. При горении лампы давление в ней возросло с 8*104 Па до 1,1*105 Па. На сколько увеличилась при этом средняя скорость молекул газа?
Слайд 15
Домашнее задание:
Параграфы 64,65.
Упражнение 11 (9,11,12)
 Основы теории вероятности - Основные понятия и определения
Основы теории вероятности - Основные понятия и определения Формирование математических понятий при изучении темы «Теория вероятностей»
Формирование математических понятий при изучении темы «Теория вероятностей» Теория вероятностей в заданиях ЕГЭ
Теория вероятностей в заданиях ЕГЭ Нахождение средней скорости движения
Нахождение средней скорости движения Теория вероятностей и статистика
Теория вероятностей и статистика Понятие и сущность перевода как деятельности. Теории перевода.
Понятие и сущность перевода как деятельности. Теории перевода. Понятие лексикологии - Лексическое и грамматическое значение слова
Понятие лексикологии - Лексическое и грамматическое значение слова