Слайды и текст этой онлайн презентации
Слайд 2
Разделите вещества на группы
AlCl3, O2, Al, SO3, Na, HCl, Cl2, Na2S
Слайд 3
Классификация веществ в зависимости от типа химической связи
Ионная AlCl3, Na2S
Ковалентная полярная SO3, HCl
Ковалентная неполярная O2, Cl2
Металлическая Al, Na
Слайд 4
Степень окисления
это заряд,
который может возникнуть у атома
в соединении,
если представить, что
связь в этом соединении
ионная
Слайд 5
Правила определения cтепени окисления
Слайд 6
1. У свободных атомов и у атомов в составе простых веществ СО равна 0.
Na2O, H2, Ba, H2SO4, N2, S, H2O, Al, Cu, HNO3, F2, CaO
Слайд 7
2. Металлы во всех соединениях имеют положительную СО, её максимальное значение равно номеру группы: А) у металлов главной подгруппы I группы +1 Б) у металлов главной подгруппы II группы +2 В) у металлов главной подгруппы III группы +3
Na, K2O, Fe, CaCO3, CrO3, AlCl3, Li3N, BaSO4, Zn, Mg(NO3)2, Mn2O7
Слайд 8
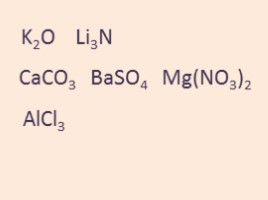
K2O Li3N
CaCO3 BaSO4 Mg(NO3)2
AlCl3
Слайд 9
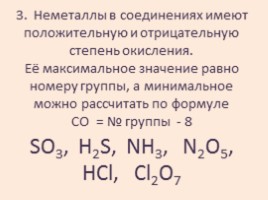
3. Неметаллы в соединениях имеют положительную и отрицательную степень окисления. Её максимальное значение равно номеру группы, а минимальное можно рассчитать по формуле СО = № группы - 8
SO3, H2S, NH3, N2O5, HCl, Cl2O7
Слайд 10
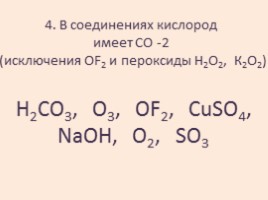
4. В соединениях кислород имеет СО -2 (исключения OF2 и пероксиды Н2О2, К2О2)
H2CO3, O3, OF2, CuSO4, NaOH, O2, SO3
Слайд 11
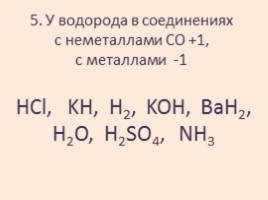
5. У водорода в соединениях с неметаллами СО +1, с металлами -1
HCl, KH, H2, KOH, BaH2, H2O, H2SO4, NH3
Слайд 12
6. В соединениях сумма степеней окисления всех атомов равна 0.
Слайд 13
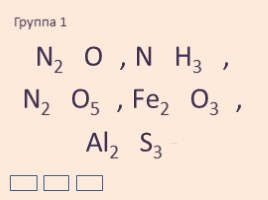
Группа 1
N2+1O-2, N-3 H3+1,
N2+5O5-2, Fe2+3O3-2,
Al2+3S3-2
Слайд 14
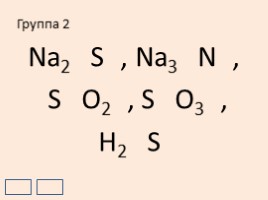
Группа 2
Na2+1S-2, Na3+1N-3,
S+4O2-2, S+6O3-2,
H2+1S-2
Слайд 15
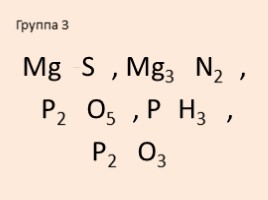
Группа 3
Mg+2S-2, Mg3+2N2-3,
P2+5O5-2, P-3H3+1,
P2+3O3-2
Слайд 16
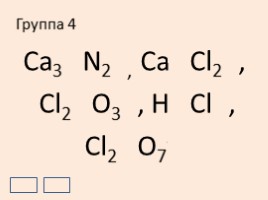
Группа 4
Ca3+2N2-3, Ca+2Cl2-1,
Cl2+3O3-2, H+1Cl-1,
Cl2+7O7-2
Слайд 17
Запишем значение постоянной степени окисления.
Умножим значение постоянной степени окисления на число атомов элемента.
Полученное число разделим на число атомов второго элемента.
Полученное число – значение степени окисления второго элемента.
Необходимо помнить, что сумма степеней окисления элементов в соединении равна 0.
Алгоритм определения cтепени окисления
Слайд 18
Составим уравнение. Для этого
определим значение постоянной степени окисления и умножим его на число атомов элемента;
неизвестную степень окисления обозначим Х и умножим на число атомов элемента;
сложим полученные произведения;
их сумма равна 0, так как сумма степеней окисления элементов в соединении равна 0.
Алгоритм определения cтепени окисления
Слайд 19
На уроке я узнал ….
На уроке я научился …
Сегодня мне удалось…
При подготовке домашнего задания мне надо обратить внимание на ….
Я хочу узнать …
Слайд 20
Степень окисления. Определение степени окисления по формуле вещества.
Слайд 21
Домашнее задание
1. Прочитайте текст §18 с. 100 – 104
2. Выучите определение и правила.
3. Выполните задания 5, 7 на с. 106
 Составление формул Бинарных соединений по степени окисления
Составление формул Бинарных соединений по степени окисления Решение неполного уравнения третьей степени
Решение неполного уравнения третьей степени По наличию второстепенных членов. Нераспространенные. Распространенные
По наличию второстепенных членов. Нераспространенные. Распространенные Главные и второстепенные члены предложения
Главные и второстепенные члены предложения Биоиндикационные исследования районов с разной степенью загрязненности атмосферы
Биоиндикационные исследования районов с разной степенью загрязненности атмосферы Решение систем уравнений второй степени урок закрепления знаний. Борисова в.С. Учитель математики мбоу сош №11
Решение систем уравнений второй степени урок закрепления знаний. Борисова в.С. Учитель математики мбоу сош №11 Степени сравнения прилагательных
Степени сравнения прилагательных