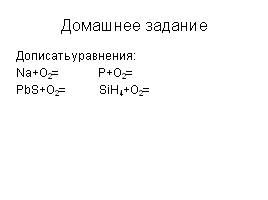Слайды и текст этой онлайн презентации
Слайд 1
Водород.
Водород в природе.Получение и применение водорода.
Физические свойства.
Слайд 2
Водород в природе.
Слайд 3
Открытие водорода
Парацельс-открыл водород
в XVI в.
Генри Кавендиш-выделил
водород в чистом виде и
изучил его свойства в
1776 г.
Лавуазье-первый получил
водород из воды в 1783 г.
Слайд 4
Получение водорода.
В лаборатории:
1.Zn+2HCl=ZnCl2+H2 (в аппарате
Киппа)
2.2Na+2H2O=2NaOH+H2
3.2H2O=2H2+O2(электролиз)
Слайд 5
Получение водорода.
В промышленности:
1.С+Н2О=Н2+СО(водяной газ)
2.СН4+2Н2О=4Н2+СО2(конверсия метана
водяным паром)
3.СН4=С+2Н2
Слайд 6
Физические свойства водорода.
Водород-газ без цвета ,запаха и вкуса,
легче воздуха в 14,5 раз,плохо растворим в воде,но хорошо в металлах.
Слайд 7
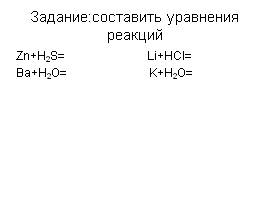
Задание:составить уравнения реакций
Zn+H2S= Li+HCl=
Ba+H2O= K+H2O=
Слайд 8
Проверить:
Zn+H2S=ZnS+H2 Li+2HCl=2LICl+H2
2K+2H2O=2KOH+H2 Ba+2H2O=Ba(OH)2+H2
Слайд 9
Решить задачи.
Какой объем займут 5 моль оксида серы(IV);16*1023 атомов серы;молекул воды?
Слайд 10
Домашнее задание
Дописать уравнения:
Na+O2= P+O2=
PbS+O2= SiH4+O2=
 Строение ароматических углеводородов - Ароматическая связь
Строение ароматических углеводородов - Ароматическая связь Постулаты Бора - Модель атома водорода по Бору
Постулаты Бора - Модель атома водорода по Бору Нефть - ценный источник углеводородов или экологическая проблема
Нефть - ценный источник углеводородов или экологическая проблема Классификация углеводородов
Классификация углеводородов Природные источники углеводородов
Природные источники углеводородов Природные углеводороды - Нефть
Природные углеводороды - Нефть Природные источники углеводородов
Природные источники углеводородов