Презентация - Классификация углеводородов
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 89%
- Слайдов: 11
- Просмотров: 4155
- Скачиваний: 1893
- Размер: 1.36 MB
- Класс: 10
- Формат: ppt / pptx
Примеры похожих презентаций
 Строение ароматических углеводородов - Ароматическая связь
Строение ароматических углеводородов - Ароматическая связь Нефть - ценный источник углеводородов или экологическая проблема
Нефть - ценный источник углеводородов или экологическая проблема Классификация технологий
Классификация технологий Опасные и чрезвычайные ситуации: классификация, общие понятия и определения
Опасные и чрезвычайные ситуации: классификация, общие понятия и определения Наркомания и наркотические вещества - Их действие на человека и классификация
Наркомания и наркотические вещества - Их действие на человека и классификация Трасология основные понятия классификация следов
Трасология основные понятия классификация следов Соли их классификация и свойства
Соли их классификация и свойства
Слайды и текст этой онлайн презентации
Слайд 1

Классификация углеводородов
Подготовила Ученица 10 класса Зарикова Мария Учитель Василенко Е.Ф. МОУ Катуаровская СОШ
Подготовила Ученица 10 класса Зарикова Мария Учитель Василенко Е.Ф. МОУ Катуаровская СОШ
Слайд 2

Классификацию веществ можно провести по любому признаку: по составу, свойству и т.д. Но А.М.Бутлеров посчитал , что первоосновой всех свойств является
химическое строение вещества.
Любое органическое вещество состоит из углерода , водорода и кислорода. Но именно углерод образовывает цепочки различной длины и конфигурации. Такие цепочки называют «углеродными скелетами».
Бутлеров А.М.
Бутлеров А.М.
Слайд 3
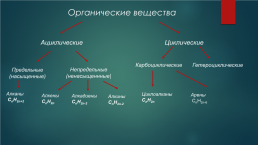
Органические вещества
Ациклические
Циклические
Карбоциклические
Гетероциклические
Непредельные (ненасыщеннные)
Предельные (насыщенные)
Алканы CnH2n+2
Циклоалканы CnH2n
Арены CnH2n-6
Алкены CnH2n
Алкадиены CnH2n-2
Алкины CnH2n-2
Ациклические
Циклические
Карбоциклические
Гетероциклические
Непредельные (ненасыщеннные)
Предельные (насыщенные)
Алканы CnH2n+2
Циклоалканы CnH2n
Арены CnH2n-6
Алкены CnH2n
Алкадиены CnH2n-2
Алкины CnH2n-2
Слайд 4

Алканы
Алка́ны (также насыщенные углеводороды, парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой CnH2n+2. (суффикс –ан)
Каждый атом углерода находится в sp3 – гибридизации . Форма молекулы в виде тетраэдра с углом 109,5°.Связь образуется посредством перекрывания гибридных орбиталей, причем максимальная область перекрывания лежит в пространстве на прямой, соединяющей ядра атомов. Это наиболее эффективное перекрывание, поэтому σ-связь считается наиболее прочной.
Для алканов свойственна изомерия углеродного скелета. Предельные соединения могут принимать различные геометрические формы, сохраняя при этом угол между связями. Количество изомеров возрастает с увеличением роста углеродной цепи. Например у бутана известно 2 изомера:
Алка́ны (также насыщенные углеводороды, парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой CnH2n+2. (суффикс –ан)
Каждый атом углерода находится в sp3 – гибридизации . Форма молекулы в виде тетраэдра с углом 109,5°.Связь образуется посредством перекрывания гибридных орбиталей, причем максимальная область перекрывания лежит в пространстве на прямой, соединяющей ядра атомов. Это наиболее эффективное перекрывание, поэтому σ-связь считается наиболее прочной.
Для алканов свойственна изомерия углеродного скелета. Предельные соединения могут принимать различные геометрические формы, сохраняя при этом угол между связями. Количество изомеров возрастает с увеличением роста углеродной цепи. Например у бутана известно 2 изомера:
Слайд 5

Алкены
Алкены — ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формулеCnH2n. Свое второе название — олефины — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел. (суффикс –ен )
Все атомы углерода находятся в sp2 – гибридизации; атомы находятся в плоскости, образуя угол 120 °С. Негибридизованные р-орбитали находятся над и под плоскостью молекулы, образуя π – связь. Эта связь менее прочная, поэтому боковое перекрывание не очень эффективно, чем осевое.
Для алкенов также характерна изомерия .
Алкены — ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формулеCnH2n. Свое второе название — олефины — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел. (суффикс –ен )
Все атомы углерода находятся в sp2 – гибридизации; атомы находятся в плоскости, образуя угол 120 °С. Негибридизованные р-орбитали находятся над и под плоскостью молекулы, образуя π – связь. Эта связь менее прочная, поэтому боковое перекрывание не очень эффективно, чем осевое.
Для алкенов также характерна изомерия .
Слайд 6

Алкадиены
Алкадиены – непредельные углеводороды, в состав которых входят две двойные связи. Общая формула алкадиенов – CnH2n-2
В зависимости от взаимного расположения кратных связей, диены подразделяются на три группы: сопряжённые диены, в которых двойные связи разделены одинарной (1,3-диены) Аллены с кумулированными двойными связями (1,2-диены) диены с изолированными двойными связями, в которых двойные связи разделены несколькими одинарными.
Строение алкинов.
π-электронные облака двойных связей перекрываются между собой, образуя единое π-облако. В сопряженной системе электроны делокализованы по всем атомам углерода:
Чем длиннее молекула, тем она более устойчива.
Алкадиены – непредельные углеводороды, в состав которых входят две двойные связи. Общая формула алкадиенов – CnH2n-2
В зависимости от взаимного расположения кратных связей, диены подразделяются на три группы: сопряжённые диены, в которых двойные связи разделены одинарной (1,3-диены) Аллены с кумулированными двойными связями (1,2-диены) диены с изолированными двойными связями, в которых двойные связи разделены несколькими одинарными.
Строение алкинов.
π-электронные облака двойных связей перекрываются между собой, образуя единое π-облако. В сопряженной системе электроны делокализованы по всем атомам углерода:
Чем длиннее молекула, тем она более устойчива.
Слайд 7

Алкины
Алкины – это непредельные углеводороды, молекулы которых содержат тройную связь. Общая формула – CnH2n-2.
Строение алкинов. Атомы углерода, которые образуют тройную связь, находятся в sp-гибридизации. σ-связи лежат в плоскости, под углом 180 °С, а π-связи образованы путем перекрывания 2х пар негибридных орбиталей соседних атомов углерода.
Изомерия алкинов. Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи. Пространственная изомерия не характерна.
Алкины – это непредельные углеводороды, молекулы которых содержат тройную связь. Общая формула – CnH2n-2.
Строение алкинов. Атомы углерода, которые образуют тройную связь, находятся в sp-гибридизации. σ-связи лежат в плоскости, под углом 180 °С, а π-связи образованы путем перекрывания 2х пар негибридных орбиталей соседних атомов углерода.
Изомерия алкинов. Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи. Пространственная изомерия не характерна.
Слайд 8

Циклоалканы
Циклоалканы, также полиметиленовые углеводороды, нафтены, цикланы, или циклопарафины — циклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам. Входят в состав нефти.
К циклоалканам относят предельные углеводороды с общей формулой CnH2n, имеющие циклическое строение. Названия циклоалканов строятся из названий соответствующих алканов с добавлением приставки цикло-
Для циклоалканов характерны следующие виды изомерии: Изомерия углеродного скелета; Пространственная; Межклассовая изомерия с алкенами. Все атомы углерода в молекулах циклоалканов имеют sp³-гибридизацию. Однако величины углов между гибридными орбиталями в циклобутане и особенно в циклопропане не 109°28', а меньше из-за геометрии, что создаёт в молекулах напряжение, поэтому малые циклы очень реакционноспособны. Циклопропан применяют для наркоза, но его применение ограничено из-за взрывоопасности.
Циклоалканы, также полиметиленовые углеводороды, нафтены, цикланы, или циклопарафины — циклические насыщенные углеводороды, по химическим свойствам близки к предельным углеводородам. Входят в состав нефти.
К циклоалканам относят предельные углеводороды с общей формулой CnH2n, имеющие циклическое строение. Названия циклоалканов строятся из названий соответствующих алканов с добавлением приставки цикло-
Для циклоалканов характерны следующие виды изомерии: Изомерия углеродного скелета; Пространственная; Межклассовая изомерия с алкенами. Все атомы углерода в молекулах циклоалканов имеют sp³-гибридизацию. Однако величины углов между гибридными орбиталями в циклобутане и особенно в циклопропане не 109°28', а меньше из-за геометрии, что создаёт в молекулах напряжение, поэтому малые циклы очень реакционноспособны. Циклопропан применяют для наркоза, но его применение ограничено из-за взрывоопасности.
Слайд 9

Арены
Арены (ароматические углеводороды) – соединения, в молекулах которых содержится одно или несколько бензольных колей – циклических групп атомов углерода со специфическим характером связей. Общая формула аренов – СnH2n-6
Изомерия аренов. Арены можно разделить на 2 группы: производные бензола: конденсированные арены
Для аренов характерна структурная изомерия, которая объясняется взаимным расположением заместителей в кольце.
Арены (ароматические углеводороды) – соединения, в молекулах которых содержится одно или несколько бензольных колей – циклических групп атомов углерода со специфическим характером связей. Общая формула аренов – СnH2n-6
Изомерия аренов. Арены можно разделить на 2 группы: производные бензола: конденсированные арены
Для аренов характерна структурная изомерия, которая объясняется взаимным расположением заместителей в кольце.
Слайд 10

Гетероциклические вещества
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол.
Производство и применение. Некоторые гетероциклические соединения получают из каменноугольной смолы (пиридин, хинолин, акридин и пр.) и при переработке растительного сырья (фурфурол). Многие природные и синтетические гетероциклические соединения — ценные красители (индиго), лекарственные вещества (хинин, морфин, акрихин, пирамидон). Гетероциклические соединения используют в производстве пластмасс, как ускорители вулканизации каучука, в кинофотопромышленности.
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол.
Производство и применение. Некоторые гетероциклические соединения получают из каменноугольной смолы (пиридин, хинолин, акридин и пр.) и при переработке растительного сырья (фурфурол). Многие природные и синтетические гетероциклические соединения — ценные красители (индиго), лекарственные вещества (хинин, морфин, акрихин, пирамидон). Гетероциклические соединения используют в производстве пластмасс, как ускорители вулканизации каучука, в кинофотопромышленности.
Слайд 11

Спасибо за внимание
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
