Презентация - Соли их классификация и свойства
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 93%
- Слайдов: 17
- Просмотров: 7948
- Скачиваний: 3232
- Размер: 0.22 MB
- Класс: 8
- Формат: ppt / pptx
Слайды и текст этой онлайн презентации
Слайд 1

Соли, их классификация и свойства
Автор: учитель химии МКОУ «Касторенская СОШ №1», п.г.т. Касторное Парамонов А.Ю., 2014
Автор: учитель химии МКОУ «Касторенская СОШ №1», п.г.т. Касторное Парамонов А.Ю., 2014
Слайд 2

Цели урока:
1)Познакомить учащихся с понятием соли, изучить основные классификации солей; 2)Изучить основные химические свойства солей; 3)Продолжить формирование умений составлять уравнения химических реакций; 4)Продолжить воспитывать культуру работы с реактивами;
1)Познакомить учащихся с понятием соли, изучить основные классификации солей; 2)Изучить основные химические свойства солей; 3)Продолжить формирование умений составлять уравнения химических реакций; 4)Продолжить воспитывать культуру работы с реактивами;
Слайд 3

Что такое соли?
Соли – это класс химических соединений, состоящих из ионов металла и ионов кислотного остатка. (Например: NaCl, NH4NO3, AgY) Солями называют электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы кислотных остатков. (Например: K3PO4 = 3K+ + PO43- )
Соли – это класс химических соединений, состоящих из ионов металла и ионов кислотного остатка. (Например: NaCl, NH4NO3, AgY) Солями называют электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы кислотных остатков. (Например: K3PO4 = 3K+ + PO43- )
Слайд 4
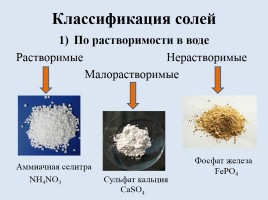
Классификация солей
По растворимости в воде Растворимые Нерастворимые Малорастворимые Аммиачная селитра NH4NO3 Сульфат кальция
Фосфат железа FePO4
CaSO4
По растворимости в воде Растворимые Нерастворимые Малорастворимые Аммиачная селитра NH4NO3 Сульфат кальция
Фосфат железа FePO4
CaSO4
Слайд 5
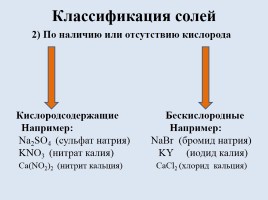
Классификация солей
2) По наличию или отсутствию кислорода Кислородсодержащие Бескислородные Например: Например: Na2SO4 (сульфат натрия) NaBr (бромид натрия) KNO3 (нитрат калия) KY (иодид калия) Ca(NO2)2 (нитрит кальция) CaCl2 (хлорид кальция)
2) По наличию или отсутствию кислорода Кислородсодержащие Бескислородные Например: Например: Na2SO4 (сульфат натрия) NaBr (бромид натрия) KNO3 (нитрат калия) KY (иодид калия) Ca(NO2)2 (нитрит кальция) CaCl2 (хлорид кальция)
Слайд 6

Разновидности солей
Соли бывают: Средние соли – это продукты полного замещения атомов водорода в кислоте на металл. Например: Na2CO3 (карбонат натрия) CuSO4 (сульфат меди) Диссоциация средних солей: Na2CO3 = 2Na+ + CO32-
Соли бывают: Средние соли – это продукты полного замещения атомов водорода в кислоте на металл. Например: Na2CO3 (карбонат натрия) CuSO4 (сульфат меди) Диссоциация средних солей: Na2CO3 = 2Na+ + CO32-
Слайд 7

Разновидности солей
2) Кислые соли – это продукты неполного замещения атомов водорода в кислоте на металл. Например: NaHCO3 (гидрокарбонат натрия) Mg(HSO4)2 (гидросульфат магния) Диссоциация кислых солей: Ca(HSO4)2 = Ca2+ + 2HSO4-
2) Кислые соли – это продукты неполного замещения атомов водорода в кислоте на металл. Например: NaHCO3 (гидрокарбонат натрия) Mg(HSO4)2 (гидросульфат магния) Диссоциация кислых солей: Ca(HSO4)2 = Ca2+ + 2HSO4-
Слайд 8

Разновидности солей
3) Основные соли – это продукты неполного замещения гидроксогрупп в основании на кислотный остаток. Например: (CuOH)2CO3 (гидроксокарбонат меди (II)) AlOHCl2 (гидроксохлорид алюминия) Диссоциация основных солей: AlOHCl2 = AlOH2+ + 2Cl-
3) Основные соли – это продукты неполного замещения гидроксогрупп в основании на кислотный остаток. Например: (CuOH)2CO3 (гидроксокарбонат меди (II)) AlOHCl2 (гидроксохлорид алюминия) Диссоциация основных солей: AlOHCl2 = AlOH2+ + 2Cl-
Слайд 9
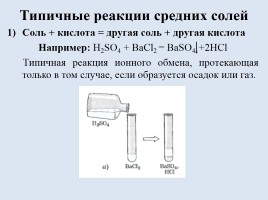
Типичные реакции средних солей
Соль + кислота = другая соль + другая кислота Например: H2SO4 + BaCl2 = BaSO4 +2HCl Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
Соль + кислота = другая соль + другая кислота Например: H2SO4 + BaCl2 = BaSO4 +2HCl Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
Слайд 10
Типичные реакции средних солей
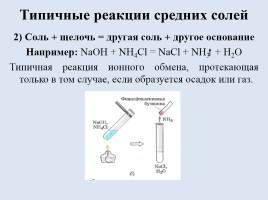
2) Соль + щелочь = другая соль + другое основание Например: NaOH + NH4Cl = NaCl + NH3 + H2O Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
2) Соль + щелочь = другая соль + другое основание Например: NaOH + NH4Cl = NaCl + NH3 + H2O Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
Слайд 11

Типичные реакции средних солей
3) Соль1 + соль2 = соль3 + соль4 Например: Na2SO4 + BaCl2 = BaSO4 +2NaCl Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок.
3) Соль1 + соль2 = соль3 + соль4 Например: Na2SO4 + BaCl2 = BaSO4 +2NaCl Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок.
Слайд 12

Типичные реакции средних солей
4) Соль + металл = другая соль + другой металл Например: CuSO4(p-p) + Fe = FeSO4 (p-p) + Cu Правила: а) Каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений; б) обе соли (и реагирующая, и образующаяся в результате реакции) должны быть растворимыми; в) металлы не должны взаимодействовать с водой, поэтому металлы главных подгрупп I и II группы ПС Д.И.Менделеева не вытесняют другие металлы из растворов солей.
4) Соль + металл = другая соль + другой металл Например: CuSO4(p-p) + Fe = FeSO4 (p-p) + Cu Правила: а) Каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений; б) обе соли (и реагирующая, и образующаяся в результате реакции) должны быть растворимыми; в) металлы не должны взаимодействовать с водой, поэтому металлы главных подгрупп I и II группы ПС Д.И.Менделеева не вытесняют другие металлы из растворов солей.
Слайд 13

Обобщение темы
Тест «Как я запомнил тему»: 1) Выберите формулу соли: а) HCl б) Ca(OH)2 в) Na2SO4 г) MgО 2) Какая из приведенных солей растворима в воде: а) AgCl б) MgS в) FePO4 г) CuSO4 3) Какая из приведенных солей бескислородная: а) CаSO4 б) KBr в) NH4NO3 г) Na2CO3
Тест «Как я запомнил тему»: 1) Выберите формулу соли: а) HCl б) Ca(OH)2 в) Na2SO4 г) MgО 2) Какая из приведенных солей растворима в воде: а) AgCl б) MgS в) FePO4 г) CuSO4 3) Какая из приведенных солей бескислородная: а) CаSO4 б) KBr в) NH4NO3 г) Na2CO3
Слайд 14

.
4) К какому типу солей относится данная соль - AlOHCl2: а) средняя б) основная в) кислая г) ни к одной из этих 5) Какая реакция не является типичной реакцией для средних солей: а) соль + металл б) соль + кислота в) соль + оксид г) соль + щелочь
4) К какому типу солей относится данная соль - AlOHCl2: а) средняя б) основная в) кислая г) ни к одной из этих 5) Какая реакция не является типичной реакцией для средних солей: а) соль + металл б) соль + кислота в) соль + оксид г) соль + щелочь
Слайд 15

Ответы:
1. в 2. г 3. б 4. б 5. в
1. в 2. г 3. б 4. б 5. в
Слайд 16

Домашнее задание:
§ 41 Упр. 2, 3.
§ 41 Упр. 2, 3.
Слайд 17

Список источников
1) Габриелян О.С. Химия. 8 класс: учеб. для общеобразоват. учрежд. / О.С. Габриелян. – 16 изд., стереотип. – М.: Дрофа, 2010.-270 с., [2]с.: ил. Использованы фотографии: http://ru.wikipedia.org/wiki/Фосфат железа (III) фосфат железа http://www.freetorg.ru/lead/ammiachnaya-selitra-azotno-fosforno-kalijnoe-udobrenie-npk,1506202.html аммиачная селитра http://www.freetorg.com.ua/lead/prodam-kalcij-sernokislyj,2478523.html сульфат кальция
1) Габриелян О.С. Химия. 8 класс: учеб. для общеобразоват. учрежд. / О.С. Габриелян. – 16 изд., стереотип. – М.: Дрофа, 2010.-270 с., [2]с.: ил. Использованы фотографии: http://ru.wikipedia.org/wiki/Фосфат железа (III) фосфат железа http://www.freetorg.ru/lead/ammiachnaya-selitra-azotno-fosforno-kalijnoe-udobrenie-npk,1506202.html аммиачная селитра http://www.freetorg.com.ua/lead/prodam-kalcij-sernokislyj,2478523.html сульфат кальция
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.