Презентация - Ферменты
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 86%
- Слайдов: 44
- Просмотров: 11280
- Скачиваний: 3370
- Размер: 2.07 MB
- Класс: 10
- Формат: ppt / pptx
Примеры похожих презентаций
 Ферменты – биологические катализаторы
Ферменты – биологические катализаторы Каталитическая активность ферментов
Каталитическая активность ферментов
 Альдегиды и кетоны
Альдегиды и кетоны
 Нуклеиновые кислоты (органическая химия)
Нуклеиновые кислоты (органическая химия)
 П.М. Третьяков - предприниматель, благотворитель, меценат, коллекционер
П.М. Третьяков - предприниматель, благотворитель, меценат, коллекционер
 Vegetables & Fruit - Овощи и фрукты
Vegetables & Fruit - Овощи и фрукты
 Сказка на английском языке для 2 класса «Теремок»
Сказка на английском языке для 2 класса «Теремок»
Слайды и текст этой онлайн презентации
Слайд 1

Ферменты
Братякова С.Б.
1
Братякова С.Б.
1
Слайд 2
Что такое ферменты?
ФЕРМЕНТЫ (от лат. fermentum — брожение, закваска) – это энзимы, специфические белки, увеличивающие скорость протекания химических реакций в клетках всех живых организмов. Наука о ферментах называется энзимологией.
Братякова С.Б.
2
ФЕРМЕНТЫ (от лат. fermentum — брожение, закваска) – это энзимы, специфические белки, увеличивающие скорость протекания химических реакций в клетках всех живых организмов. Наука о ферментах называется энзимологией.
Братякова С.Б.
2
Слайд 3

История изучения
Термин «фермент» был предложен в XVII веке химиком ван Гельмонтом при обсуждении механизмов пищеварения.
Братякова С.Б.
3
Термин «фермент» был предложен в XVII веке химиком ван Гельмонтом при обсуждении механизмов пищеварения.
Братякова С.Б.
3
Слайд 4

В 1833 французскими химиками А. Пайеном и Ж. Персо впервые из прорастающих зерен ячменя было выделено активное вещество, осуществляющее превращение крахмала в сахар и получившее название диастазы(амилазы).
Братякова С.Б.
4
Братякова С.Б.
4
Слайд 5
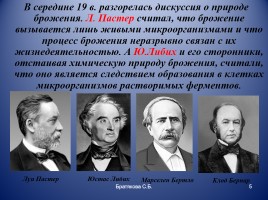
В середине 19 в. разгорелась дискуссия о природе брожения. Л. Пастер считал, что брожение вызывается лишь живыми микроорганизмами и что процесс брожения неразрывно связан с их жизнедеятельностью. А Ю.Либих и его сторонники, отстаивая химическую природу брожения, считали, что оно является следствием образования в клетках микроорганизмов растворимых ферментов.
Луи Пастер
Юстас Либих
Марселен Бертло
Клод Бернар
Братякова С.Б.
5
Луи Пастер
Юстас Либих
Марселен Бертло
Клод Бернар
Братякова С.Б.
5
Слайд 6

Дискуссия Либиха и Пастера о природе брожения была разрешена в 1897 Э.Бухнером, который, растирая дрожжи с инфузорной землёй, выделил из них бесклеточный растворимый ферментный препарат (зимазу), вызывавший спиртовое брожение. Открытие Бухнера утвердило материалистическое понимание природы брожений.
Братякова С.Б.
6
Братякова С.Б.
6
Слайд 7
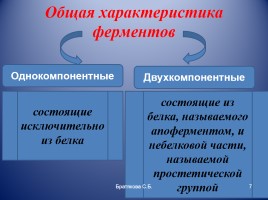
Общая характеристика ферментов
Однокомпонентные
Двухкомпонентные
состоящие исключительно из белка
состоящие из белка, называемого апоферментом, и небелковой части, называемой простетической группой
Братякова С.Б.
7
Однокомпонентные
Двухкомпонентные
состоящие исключительно из белка
состоящие из белка, называемого апоферментом, и небелковой части, называемой простетической группой
Братякова С.Б.
7
Слайд 8

Они значительно эффективнее (в 1014 – 1015 раз) небиологических катализаторов.
Высокая специфичность их действия.
Особенности ферментов:
Ферменты не капризны, однако каждая ферментативная реакция наиболее быстро протекает при строго определенном значении PH и t° C
Братякова С.Б.
8
Особенности ферментов:
Ферменты не капризны, однако каждая ферментативная реакция наиболее быстро протекает при строго определенном значении PH и t° C
Братякова С.Б.
8
Слайд 9

3.Ферменты – белки, при кипячении разрушаются и теряют свои ферментативные свойства.
1. Ферменты – катализаторы и поэтому могут ускорять определенные процессы. 2. Ферменты действуют на определенные субстраты (вещества).
Свойства ферментов
Братякова С.Б.
9
1. Ферменты – катализаторы и поэтому могут ускорять определенные процессы. 2. Ферменты действуют на определенные субстраты (вещества).
Свойства ферментов
Братякова С.Б.
9
Слайд 10

Функции ферментов
Ферменты выступают в роли катализаторов практически во всех биохимических реакциях Направляют и регулируют обмен веществ организма..
Братякова С.Б.
10
Ферменты выступают в роли катализаторов практически во всех биохимических реакциях Направляют и регулируют обмен веществ организма..
Братякова С.Б.
10
Слайд 11

Принцип действия ферментов
Фермент и субстрат должны подходить друг к другу «как ключ к замку»
Братякова С.Б.
11
Фермент и субстрат должны подходить друг к другу «как ключ к замку»
Братякова С.Б.
11
Слайд 12
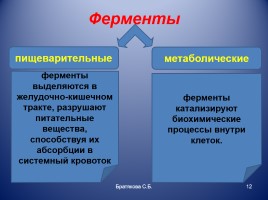
Ферменты
пищеварительные
метаболические
ферменты выделяются в желудочно-кишечном тракте, разрушают питательные вещества, способствуя их абсорбции в системный кровоток
ферменты катализируют биохимические процессы внутри клеток.
Братякова С.Б.
12
пищеварительные
метаболические
ферменты выделяются в желудочно-кишечном тракте, разрушают питательные вещества, способствуя их абсорбции в системный кровоток
ферменты катализируют биохимические процессы внутри клеток.
Братякова С.Б.
12
Слайд 13

Пищеварительные ферменты
Амилаза расщепляет углеводы и находится в слюне, панкреатическом секрете и в содержимом кишечника. Различные виды амилазы расщепляют различные сахара. Протеазы, находящиеся в желудочном соке, панкреатическом секрете и в содержимом кишечника, помогают переваривать белки. Липаза, находящаяся в желудочном соке и панкреатическом секрете, расщепляет жиры.
Братякова С.Б.
13
Амилаза расщепляет углеводы и находится в слюне, панкреатическом секрете и в содержимом кишечника. Различные виды амилазы расщепляют различные сахара. Протеазы, находящиеся в желудочном соке, панкреатическом секрете и в содержимом кишечника, помогают переваривать белки. Липаза, находящаяся в желудочном соке и панкреатическом секрете, расщепляет жиры.
Братякова С.Б.
13
Слайд 14

СВОЙСТВА ФЕРМЕНТОВ:
Селективность Эффективность Зависимость от температуры Зависимость от среды раствора
Братякова С.Б.
14
Селективность Эффективность Зависимость от температуры Зависимость от среды раствора
Братякова С.Б.
14
Слайд 15

Селективность ферментов:
Селективность(избирательность) -это свойство ферментов ускорять только одну или группу однотипных реакции. Селективность позволяет организму быстро и точно выполнить четкую программу синтеза веществ.
Братякова С.Б.
15
Селективность(избирательность) -это свойство ферментов ускорять только одну или группу однотипных реакции. Селективность позволяет организму быстро и точно выполнить четкую программу синтеза веществ.
Братякова С.Б.
15
Слайд 16

Эффективность ферментов:
Эффективность-свойство ускорения реакции. Скорость некоторых ферментативных реакции может быть в 1015 раз больше скорости реакции, протекающей в их отсутствие … Пример: 2Н2О2 каталаза 2Н2О+О2
Братякова С.Б.
16
Эффективность-свойство ускорения реакции. Скорость некоторых ферментативных реакции может быть в 1015 раз больше скорости реакции, протекающей в их отсутствие … Пример: 2Н2О2 каталаза 2Н2О+О2
Братякова С.Б.
16
Слайд 17

Зависимость от температуры
Термолабильность, т. е. высокая чувствительность к изменениям температуры. Так как ферменты являются белками, то для большинства из них температура свыше 70 C приводит к денатурации и потере активности. При увеличении температуры до 10 С реакция ускоряется в 2-3 раза, а при температурах близких к 0 С скорость ферментативных реакций замедляется до минимума.
Братякова С.Б.
17
Термолабильность, т. е. высокая чувствительность к изменениям температуры. Так как ферменты являются белками, то для большинства из них температура свыше 70 C приводит к денатурации и потере активности. При увеличении температуры до 10 С реакция ускоряется в 2-3 раза, а при температурах близких к 0 С скорость ферментативных реакций замедляется до минимума.
Братякова С.Б.
17
Слайд 18
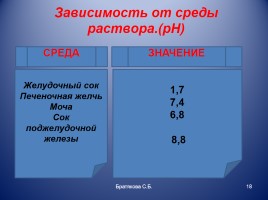
Зависимость от среды раствора.(рН)
СРЕДА
ЗНАЧЕНИЕ
Желудочный сок Печеночная желчь Моча Сок поджелудочной железы
1,7 7,4 6,8 8,8
Братякова С.Б.
18
СРЕДА
ЗНАЧЕНИЕ
Желудочный сок Печеночная желчь Моча Сок поджелудочной железы
1,7 7,4 6,8 8,8
Братякова С.Б.
18
Слайд 19

Классификация ферментов
1.Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции, например, каталаза: 2 H2O2-->O2+2 H2O 2.Трансферазы - ферменты, катализирующие перенос атомов или радикалов. 3.Гидролазы - ферменты, разрывающие внутримолекулярные связи путем присоединения молекул воды. Например, фосфатаза: OH R - O - P = O + H2O ROH + H3PO4 OH
Братякова С.Б.
19
1.Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции, например, каталаза: 2 H2O2-->O2+2 H2O 2.Трансферазы - ферменты, катализирующие перенос атомов или радикалов. 3.Гидролазы - ферменты, разрывающие внутримолекулярные связи путем присоединения молекул воды. Например, фосфатаза: OH R - O - P = O + H2O ROH + H3PO4 OH
Братякова С.Б.
19
Слайд 20

4.Лиазы - ферменты, отщепляющие от субстрата ту или иную группу без присоединения воды, негидролитическим путем.
Например: отщепление карбоксильной группы декарбоксилазой:
O O
// ||
CH3 - C - C CO2 + CH3 - C
||
O OH H
Братякова С.Б.
20
Братякова С.Б.
20
Слайд 21

5.Изомеразы - ферменты, катализирующие превращение одного изомера в другой:
глюкозо-6-фосфат глюкозо-1-фосфат
6.Синтетазы - ферменты, катализирующие реакции синтеза.
Братякова С.Б.
21
Братякова С.Б.
21
Слайд 22
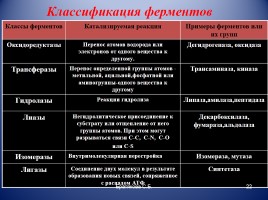
Классификация ферментов
Классы ферментов Катализируемая реакция Примеры ферментов или их групп
Оксидоредуктазы Перенос атомов водорода или электронов от одного вещества к другому. Дегидрогеназа, оксидаза
Трансферазы Перенос определенной группы атомов -метильной, ацильной,фосфатной или аминогруппы-одного вещества к другому Трансаминаза, киназа
Гидролазы Реакции гидролиза Липаза,амилаза,пептидаза
Лиазы Негидролитическое присоединение к субстрату или отщепление от него группы атомов. При этом могут разрываться связи С-С, C-N, C-O или C-S Декарбоксилаза, фумараза,альдолаза
Изомеразы Внутримолекулярная перестройка Изомераза, мутаза
Лигазы Соединение двух молекул в результате образования новых связей, сопряженное с распадом АТФ Синтетаза
Братякова С.Б.
22
Классы ферментов Катализируемая реакция Примеры ферментов или их групп
Оксидоредуктазы Перенос атомов водорода или электронов от одного вещества к другому. Дегидрогеназа, оксидаза
Трансферазы Перенос определенной группы атомов -метильной, ацильной,фосфатной или аминогруппы-одного вещества к другому Трансаминаза, киназа
Гидролазы Реакции гидролиза Липаза,амилаза,пептидаза
Лиазы Негидролитическое присоединение к субстрату или отщепление от него группы атомов. При этом могут разрываться связи С-С, C-N, C-O или C-S Декарбоксилаза, фумараза,альдолаза
Изомеразы Внутримолекулярная перестройка Изомераза, мутаза
Лигазы Соединение двух молекул в результате образования новых связей, сопряженное с распадом АТФ Синтетаза
Братякова С.Б.
22
Слайд 23

Местонахождение ферментов в организме
В клетке часть ферментов находится в цитоплазме, но в основном ферменты связаны с определенными клеточными структурами. В ядре, например, находятся ферменты, ответственные за репликацию — синтез ДНК и за ее транскрипцию — образование РНК .
ДНК-лигаза
Братякова С.Б.
23
В клетке часть ферментов находится в цитоплазме, но в основном ферменты связаны с определенными клеточными структурами. В ядре, например, находятся ферменты, ответственные за репликацию — синтез ДНК и за ее транскрипцию — образование РНК .
ДНК-лигаза
Братякова С.Б.
23
Слайд 24

Условия действия ферментов
Действие ферментов зависит от ряда факторов: От температуры (max 40-50°С) Активной реакции среды – pH (кислотность). От присутствия специфических активаторов и неспецифических или специфических ингибиторов.
Братякова С.Б.
24
Действие ферментов зависит от ряда факторов: От температуры (max 40-50°С) Активной реакции среды – pH (кислотность). От присутствия специфических активаторов и неспецифических или специфических ингибиторов.
Братякова С.Б.
24
Слайд 25

Специфичность и механизм действия ферментов
Действие ферментов, строго специфично и зависит от строения субстрата, на который фермент действует. Прекрасным примером такой зависимости служит катализируемая аргиназой реакция гидролитического расщепления аминокислоты аргинина на орнитин и мочевину:
Братякова С.Б.
25
Действие ферментов, строго специфично и зависит от строения субстрата, на который фермент действует. Прекрасным примером такой зависимости служит катализируемая аргиназой реакция гидролитического расщепления аминокислоты аргинина на орнитин и мочевину:
Братякова С.Б.
25
Слайд 26

Кофакторы ферментов
Многие ферменты для проявления активности нуждаются в веществах небелковой природы- кофакторах. Кофакторы могут быть как неорганическими молекулами (ионы металлов, железо-серные кластеры и др.), так и органическими (например, флавин или гем).
Братякова С.Б.
26
Многие ферменты для проявления активности нуждаются в веществах небелковой природы- кофакторах. Кофакторы могут быть как неорганическими молекулами (ионы металлов, железо-серные кластеры и др.), так и органическими (например, флавин или гем).
Братякова С.Б.
26
Слайд 27

Получение ферментов
Обычно ферменты вьделяют из тканей животных, растений, клеток и культуральных жидкостей микроорганизмов, биологических жидкостей (кровь, лимфа и др.). Для получения некоторых труднодоступных ферментов используются методы генетической инженерии.
Братякова С.Б.
27
Обычно ферменты вьделяют из тканей животных, растений, клеток и культуральных жидкостей микроорганизмов, биологических жидкостей (кровь, лимфа и др.). Для получения некоторых труднодоступных ферментов используются методы генетической инженерии.
Братякова С.Б.
27
Слайд 28

Болезни, связанные с нарушением выработки ферментов
Отсутствие или снижение активности какого-либо фермента (нередко и избыточная активность) у человека приводит к развитию заболеваний (энзимопатий) или гибели организма. Так, передаваемое по наследству заболевание детей — галактоземия (приводит к умственной отсталости) — развивается вследствие нарушения синтеза фермента, ответственного за превращение галактозы в легко усваиваемую глюкозу.
Братякова С.Б.
28
Отсутствие или снижение активности какого-либо фермента (нередко и избыточная активность) у человека приводит к развитию заболеваний (энзимопатий) или гибели организма. Так, передаваемое по наследству заболевание детей — галактоземия (приводит к умственной отсталости) — развивается вследствие нарушения синтеза фермента, ответственного за превращение галактозы в легко усваиваемую глюкозу.
Братякова С.Б.
28
Слайд 29

Причиной другого наследственного заболевания — фенилкетонурии, сопровождающегося расстройством психической деятельности, является потеря клетками печени способности синтезировать фермент, катализирующий превращение аминокислоты фенилаланина в тирозин.
Определение активности многих ферментов в крови, моче, спинно-мозговой, семенной и других жидкостях организма используется для диагностики ряда заболеваний. С помощью такого анализа сыворотки крови возможно обнаружение на ранней стадии инфаркта миокарда, вирусного гепатита, панкреатита, нефрита и других заболеваний.
Братякова С.Б.
29
Определение активности многих ферментов в крови, моче, спинно-мозговой, семенной и других жидкостях организма используется для диагностики ряда заболеваний. С помощью такого анализа сыворотки крови возможно обнаружение на ранней стадии инфаркта миокарда, вирусного гепатита, панкреатита, нефрита и других заболеваний.
Братякова С.Б.
29
Слайд 30
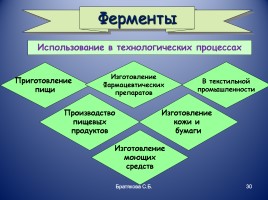
Ферменты
Использование в технологических процессах
Приготовление пищи
Производство пищевых продуктов
Изготовление Фармацевтических препаратов
Изготовление моющих средств
В текстильной промышленности
Изготовление кожи и бумаги
Братякова С.Б.
30
Использование в технологических процессах
Приготовление пищи
Производство пищевых продуктов
Изготовление Фармацевтических препаратов
Изготовление моющих средств
В текстильной промышленности
Изготовление кожи и бумаги
Братякова С.Б.
30
Слайд 31
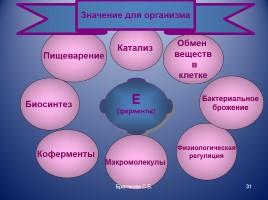
Физиологическая
регуляция
Пищеварение
Е (ферменты)
Биосинтез
Коферменты
Макромолекулы
Катализ
Бактериальное брожение
Обмен веществ в клетке
Значение для организма
Братякова С.Б.
31
Пищеварение
Е (ферменты)
Биосинтез
Коферменты
Макромолекулы
Катализ
Бактериальное брожение
Обмен веществ в клетке
Значение для организма
Братякова С.Б.
31
Слайд 32

Использование ферментов
Амилаза
Папаин
Фицин
Пепсин
Трипсин
Реннин
Протеаза
Каталаза
Глюкозооксидаза
Целлюлаза
Пектиназа
Братякова С.Б.
32
Амилаза
Папаин
Фицин
Пепсин
Трипсин
Реннин
Протеаза
Каталаза
Глюкозооксидаза
Целлюлаза
Пектиназа
Братякова С.Б.
32
Слайд 33

Амилаза
Промышленность Использование
Пивоваренная Осахаривание содержащегося в солоде крахмала
Текстильная Хлебопекарная Удаление крахмала, наносимого на нити во время шлихтования. Крахмал превращается в глюкозу. Дрожжевые клетки, сбраживая глюкозу, образуют углекислый газ, пузырьки которого разрыхляют тесто и придают хлебу пористую структуру.хлеб лучше подрумянивается и дольше не черствеет.
Братякова С.Б.
33
Промышленность Использование
Пивоваренная Осахаривание содержащегося в солоде крахмала
Текстильная Хлебопекарная Удаление крахмала, наносимого на нити во время шлихтования. Крахмал превращается в глюкозу. Дрожжевые клетки, сбраживая глюкозу, образуют углекислый газ, пузырьки которого разрыхляют тесто и придают хлебу пористую структуру.хлеб лучше подрумянивается и дольше не черствеет.
Братякова С.Б.
33
Слайд 34

Фицин
Промышленность Использование
Фармацевтическая Добавки к зубным пастам для удаления зубного налета.
Фотография Смывание желатина с использованной пленки для того, чтобы извлечь находящееся в нем серебро.
Братякова С.Б.
34
Промышленность Использование
Фармацевтическая Добавки к зубным пастам для удаления зубного налета.
Фотография Смывание желатина с использованной пленки для того, чтобы извлечь находящееся в нем серебро.
Братякова С.Б.
34
Слайд 35

Папаин
Промышленность Использование
Пивоваренная Этапы процесса пивоварения, регулирующие качество пены.
Мясная Умягчение мяса. Этот фермент довольно устойчив к повышению температуры и при нагревании мяса какое-то время продолжает действовать. Потом он, конечно, инактивируется.
Братякова С.Б.
35
Промышленность Использование
Пивоваренная Этапы процесса пивоварения, регулирующие качество пены.
Мясная Умягчение мяса. Этот фермент довольно устойчив к повышению температуры и при нагревании мяса какое-то время продолжает действовать. Потом он, конечно, инактивируется.
Братякова С.Б.
35
Слайд 36

Пепсин
Промышленность Использование
Пищевая Производство готовых каш.
Фармацевтическая Препараты, способствующие пищеварению (с дополнением к обычному действию пепсина в желудке).
Братякова С.Б.
36
Промышленность Использование
Пищевая Производство готовых каш.
Фармацевтическая Препараты, способствующие пищеварению (с дополнением к обычному действию пепсина в желудке).
Братякова С.Б.
36
Слайд 37

Трипсин
Промышленность Использование
Пищевая Производство продуктов для детского питания
Братякова С.Б.
37
Промышленность Использование
Пищевая Производство продуктов для детского питания
Братякова С.Б.
37
Слайд 38

Реннин
Промышленность Использование
Сыроделие Свертывание молока (получение сгустка казеина)
Братякова С.Б.
38
Промышленность Использование
Сыроделие Свертывание молока (получение сгустка казеина)
Братякова С.Б.
38
Слайд 39

Глюкозооксидаза
Промышленность Использование
Пищевая Удаление глюкозы или кислорода
Братякова С.Б.
39
Промышленность Использование
Пищевая Удаление глюкозы или кислорода
Братякова С.Б.
39
Слайд 40

Бактериальные протеазы
Промышленность Использование
Стирка белья Стиральные порошки с ферментными добавками
Кожевенная Текстильная Пищевая Отделение волоса – способ, при котором не повреждается ни волос, ни шкура Извлечение шерсти из обрывков овечьих шкур Получение белковых гидролизатов (в частности, для производства кормов)
Братякова С.Б.
40
Промышленность Использование
Стирка белья Стиральные порошки с ферментными добавками
Кожевенная Текстильная Пищевая Отделение волоса – способ, при котором не повреждается ни волос, ни шкура Извлечение шерсти из обрывков овечьих шкур Получение белковых гидролизатов (в частности, для производства кормов)
Братякова С.Б.
40
Слайд 41

Каталаза
Промышленность Использование
Пищевая Удаление пероксида водорода
Резиновая Получение (из пероксида водорода) кислорода, необходимого для превращения латекса в губчатую резину
Братякова С.Б.
41
Промышленность Использование
Пищевая Удаление пероксида водорода
Резиновая Получение (из пероксида водорода) кислорода, необходимого для превращения латекса в губчатую резину
Братякова С.Б.
41
Слайд 42

Целлюлаза. Пектиназа
Промышленность Использование
Пищевая Осветление фруктовых соков
Братякова С.Б.
42
Промышленность Использование
Пищевая Осветление фруктовых соков
Братякова С.Б.
42
Слайд 43

Сказ о дележе наследства
Умирал старый араб. Все его богатство состояло из 17 прекрасных белых верблюдов. Он собрал своих сыновей и объявил им свою последнюю волю: «Мой старший сын, опора семьи, должен получить после моей смерти половину верблюдов. Среднему сыну я завещаю треть всех верблюдов. Но и мой младший, любимый сын должен получить свою долю — одну девятую часть стада». Сказав это, старый араб умер. Похоронив отца, три брата стали делить верблюдов. Но исполнить волю отца они не смогли: невозможно было разделить 17 верблюдов ни пополам, ни на три части, ни на девять частей. Но тут через пустыню проходил дервиш. Бедный, как все ученые, он вел с собой черного облезлого верблюда, нагруженного книгами. Братья обратились к нему за помощью. И дервиш сказал: «Выполнить волю вашего отца очень просто. Я дарю вам моего верблюда, а вы попробуйте разделить наследство». У братьев оказалось 18 верблюдов, и все разрешилось. Старший сын получил половину верблюдов – 9, средний – треть стада – 6 и младший сын получил свою долю – двух верблюдов. Но 9, 6 и 2 дают 17, и после дележа оказался лишний верблюд — старый облезлый верблюд ученого. И дервиш сказал: «Отдайте мне назад моего верблюда за то, что я помог разделить вам наследство, а то мне придется самому тащить книги через пустыню». Вот этот черный верблюд и подобен ферменту. Он сделал возможным такой процесс, который без него был бы немыслим, а сам остался без изменений. Это действительно основное свойство ферментов, да и вообще всякого катализатора.
Братякова С.Б.
43
Умирал старый араб. Все его богатство состояло из 17 прекрасных белых верблюдов. Он собрал своих сыновей и объявил им свою последнюю волю: «Мой старший сын, опора семьи, должен получить после моей смерти половину верблюдов. Среднему сыну я завещаю треть всех верблюдов. Но и мой младший, любимый сын должен получить свою долю — одну девятую часть стада». Сказав это, старый араб умер. Похоронив отца, три брата стали делить верблюдов. Но исполнить волю отца они не смогли: невозможно было разделить 17 верблюдов ни пополам, ни на три части, ни на девять частей. Но тут через пустыню проходил дервиш. Бедный, как все ученые, он вел с собой черного облезлого верблюда, нагруженного книгами. Братья обратились к нему за помощью. И дервиш сказал: «Выполнить волю вашего отца очень просто. Я дарю вам моего верблюда, а вы попробуйте разделить наследство». У братьев оказалось 18 верблюдов, и все разрешилось. Старший сын получил половину верблюдов – 9, средний – треть стада – 6 и младший сын получил свою долю – двух верблюдов. Но 9, 6 и 2 дают 17, и после дележа оказался лишний верблюд — старый облезлый верблюд ученого. И дервиш сказал: «Отдайте мне назад моего верблюда за то, что я помог разделить вам наследство, а то мне придется самому тащить книги через пустыню». Вот этот черный верблюд и подобен ферменту. Он сделал возможным такой процесс, который без него был бы немыслим, а сам остался без изменений. Это действительно основное свойство ферментов, да и вообще всякого катализатора.
Братякова С.Б.
43
Слайд 44

1. Габриелян О. С., Маскаев Ф. Н., Пономарев С. Ю., Теренин В. И.Химия. 10 класс. Профильный уровень. М. Дрофа, 2009
2. Чертков И.Н. Методика формирований у учащихся основных понятий органической химии. – М.: Просвещение: 1991.
3. alhimic.ucoz.ru/load/26-1-0-39
4. www.alleng.ru/edu/chem1.htm
5. www.uchportal.ru/load/60-1-0-9056
6. http://ppt4web.ru/khimija
7. О. С. Габриелян, И.Г. Остроумов. «Химия. 10 класс. Настольная книга учителя»
Список использованной литературы и Интернет-ресурсов
Братякова С.Б.
44
Список использованной литературы и Интернет-ресурсов
Братякова С.Б.
44
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
