Презентация - Биологические окисления
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 95%
- Слайдов: 51
- Просмотров: 5287
- Скачиваний: 2553
- Размер: 0.83 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Биологический КВН
Биологический КВН Игра для учащихся 5-8 класса «Биологический брейн-ринг»
Игра для учащихся 5-8 класса «Биологический брейн-ринг» Биологические ритмы - Сон и его значение
Биологические ритмы - Сон и его значение Ферменты – биологические катализаторы
Ферменты – биологические катализаторы Составление формул Бинарных соединений по степени окисления
Составление формул Бинарных соединений по степени окисления Биологический калькулятор «Систематика»
Биологический калькулятор «Систематика» Биологические технологии в здравоохранении
Биологические технологии в здравоохранении
Слайды и текст этой онлайн презентации
Слайд 1

ЛЕКЦИЯ № 4
Биологическое окисление-1
Дисциплина: Биохимия
Биологическое окисление-1
Дисциплина: Биохимия
Слайд 2

Обмен энергии
Слайд 3
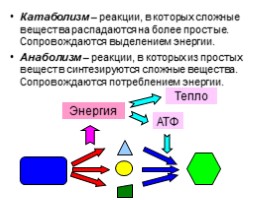
Катаболизм – реакции, в которых сложные вещества распадаются на более простые. Сопровождаются выделением энергии.
Анаболизм – реакции, в которых из простых веществ синтезируются сложные вещества. Сопровождаются потреблением энергии.
Энергия
Тепло
АТФ
Энергия
Тепло
АТФ
Слайд 4
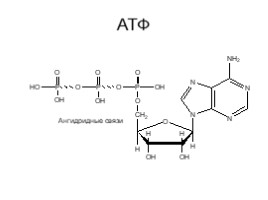
АТФ
Ангидридные связи
Ангидридные связи
Слайд 5
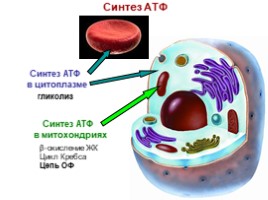
Синтез АТФ
Синтез АТФ в митохондриях
β-окисление ЖК Цикл Кребса Цепь ОФ
Синтез АТФ в цитоплазме
гликолиз
Синтез АТФ в митохондриях
β-окисление ЖК Цикл Кребса Цепь ОФ
Синтез АТФ в цитоплазме
гликолиз
Слайд 6
АДФ + Фн АТФ
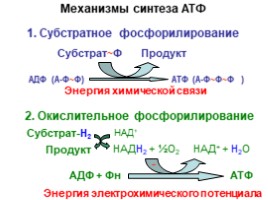
Механизмы синтеза АТФ
Энергия электрохимического потенциала
2. Окислительное фосфорилирование
АДФ (А-Ф~Ф) АТФ (А-Ф~Ф~Ф )
Энергия химической связи
1. Субстратное фосфорилирование
Субстрат~Ф Продукт
НАДН2 + ½О2 НАД+ + Н2О
Субстрат-H2 Продукт
НАД+
~
Механизмы синтеза АТФ
Энергия электрохимического потенциала
2. Окислительное фосфорилирование
АДФ (А-Ф~Ф) АТФ (А-Ф~Ф~Ф )
Энергия химической связи
1. Субстратное фосфорилирование
Субстрат~Ф Продукт
НАДН2 + ½О2 НАД+ + Н2О
Субстрат-H2 Продукт
НАД+
~
Слайд 7
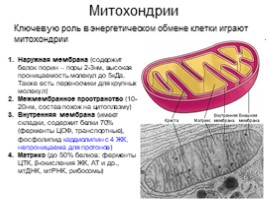
Митохондрии
Ключевую роль в энергетическом обмене клетки играют митохондрии
Наружная мембрана (содержит белок порин – поры 2-3нм, высокая проницаемость молекул до 5кДа. Также есть переносчики для крупных молекул) Межмембранное пространство (10-20нм, состав похож на цитоплазму) Внутренняя мембрана (имеет складки, содержит белки 70% (ферменты ЦОФ, транспортные), фосфолипид кардиолипин с 4 ЖК, непроницаема для протонов) Матрикс (до 50% белков: ферменты ЦТК, β-окисления ЖК, АТ и др., мтДНК, мтРНК, рибосомы)
Ключевую роль в энергетическом обмене клетки играют митохондрии
Наружная мембрана (содержит белок порин – поры 2-3нм, высокая проницаемость молекул до 5кДа. Также есть переносчики для крупных молекул) Межмембранное пространство (10-20нм, состав похож на цитоплазму) Внутренняя мембрана (имеет складки, содержит белки 70% (ферменты ЦОФ, транспортные), фосфолипид кардиолипин с 4 ЖК, непроницаема для протонов) Матрикс (до 50% белков: ферменты ЦТК, β-окисления ЖК, АТ и др., мтДНК, мтРНК, рибосомы)
Слайд 8

Митохондрии
Митохондрии млекопитающих обычно содержат от двух до десяти идентичных копий кольцевых молекул ДНК
NADH-дегидрогеназа (комплекс I) Кофермент Q цитохром c редуктаза/Цитохром b (комплекс III) цитохром c оксидаза (комплекс IV) АТФ-синтаза (комплекс V) рРНК тРНК
У человека в митохондриях 16565 пар нуклеотидов и содержит 37 генов: 13 кодируют биосинтез белков, 22 являются матрицей для тРНК, 2 являются матрицей для рРНК
Митохондрии млекопитающих обычно содержат от двух до десяти идентичных копий кольцевых молекул ДНК
NADH-дегидрогеназа (комплекс I) Кофермент Q цитохром c редуктаза/Цитохром b (комплекс III) цитохром c оксидаза (комплекс IV) АТФ-синтаза (комплекс V) рРНК тРНК
У человека в митохондриях 16565 пар нуклеотидов и содержит 37 генов: 13 кодируют биосинтез белков, 22 являются матрицей для тРНК, 2 являются матрицей для рРНК
Слайд 9

История развития учения о биологическом окислении
Антуан Лоран Лавуазье (1743 – 1794) – французский химик – в 1777г. впервые правильно истолковал явление горения как процесс соединения веществ с О2. Т.к. горение и дыхание сопровождаются потреблением О2 и выделение СО2, он предположил что, в их основе лежит один процесс. Но у дыхания были существенные отличия от горения, идёт: при низкой температуре; без пламени; в присутствии воды.
Антуан Лоран Лавуазье (1743 – 1794) – французский химик – в 1777г. впервые правильно истолковал явление горения как процесс соединения веществ с О2. Т.к. горение и дыхание сопровождаются потреблением О2 и выделение СО2, он предположил что, в их основе лежит один процесс. Но у дыхания были существенные отличия от горения, идёт: при низкой температуре; без пламени; в присутствии воды.
Слайд 10

В конце XIX века русские исследователи А.Н. Бах и В.И. Палладин, работая независимо друг от друга, предложили 2 основные теории для объяснения процессов, протекающих в ходе биологического окисления.
Алексей Николаевич Бах (1857 – 1946). В 1897г сформулировал «ПЕРЕКИСНУЮ ТЕОРИЮ МЕДЛЕННОГО ОКИСЛЕНИЯ», согласно которой молекула О2 сначала активируется в результате разрыва одной его связи (-О-О-) и присоединения к органическим веществам – оксидазам. Активированный О2 при взаимодействии с окисляемым веществом образует перекись.
Алексей Николаевич Бах (1857 – 1946). В 1897г сформулировал «ПЕРЕКИСНУЮ ТЕОРИЮ МЕДЛЕННОГО ОКИСЛЕНИЯ», согласно которой молекула О2 сначала активируется в результате разрыва одной его связи (-О-О-) и присоединения к органическим веществам – оксидазам. Активированный О2 при взаимодействии с окисляемым веществом образует перекись.
Слайд 11
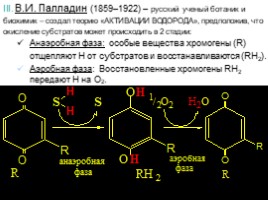
В.И. Палладин (1859–1922) – русский ученый ботаник и биохимик – создал теорию «АКТИВАЦИИ ВОДОРОДА», предположив, что окисление субстратов может происходить в 2 стадии:
Анаэробная фаза: особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH2).
Аэробная фаза: Восстановленные хромогены RH2 передают Н на О2.
Слайд 12

Отто Генрих Варбург открыл фермент(E) – цитохромоксидазу, работающую на заключительном этапе БО. Процесс БО представляет не только процессы дегидрирования, но и активирования О2 железосодержащими E.
Кейлин Дейвид (1881-1963) открыл цитохромы. Установил, что они способны передавать H+ и e- с окисляемого S на O2. Шенбайн показал, что БО – каталитический процесс, в котором используется активный кислород.
В дальнейшем значительный вклад в исследование БО внесли ряд и других учёных. Вот некоторые из них:
Кейлин Дейвид (1881-1963) открыл цитохромы. Установил, что они способны передавать H+ и e- с окисляемого S на O2. Шенбайн показал, что БО – каталитический процесс, в котором используется активный кислород.
В дальнейшем значительный вклад в исследование БО внесли ряд и других учёных. Вот некоторые из них:
Слайд 13
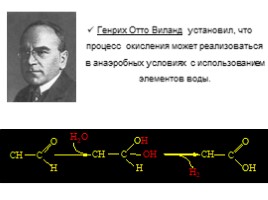
Генрих Отто Виланд установил, что процесс окисления может реализоваться в анаэробных условиях с использованием элементов воды.
Слайд 14

Современные представления о биологическом окислении
Согласно современной теории БО: окисление происходит как в аэробных, так и в анаэробных условиях; в аэробных организмах существует несколько путей использования О2; реакции БО необходимы для: получения энергии; синтеза новых веществ; разрушения чужеродных веществ; БО является сложным, многостадийным процессом, в котором ведущую роль играют ферменты -оксидоредуктазы.
Согласно современной теории БО: окисление происходит как в аэробных, так и в анаэробных условиях; в аэробных организмах существует несколько путей использования О2; реакции БО необходимы для: получения энергии; синтеза новых веществ; разрушения чужеродных веществ; БО является сложным, многостадийным процессом, в котором ведущую роль играют ферменты -оксидоредуктазы.
Слайд 15

Окислительно-восстановительные реакции (ОВР) – реакции, в которых меняется степень окисления субстрата за счет присоединения / отщепления:
1) 1 е-;
2) 2е- и 2Н+;
3) атомов кислорода
Субстрат-H2 + R Продукт + RH2
Субстрат-H2 + ½O2 Продукт + H2O
Цит1(Fe3+) + Цит2(Fe2+) Цит1(Fe2+) + Цит2(Fe3+)
Основные понятия БО
Субстрат-H2 + R Продукт + RH2
Субстрат-H2 + ½O2 Продукт + H2O
Цит1(Fe3+) + Цит2(Fe2+) Цит1(Fe2+) + Цит2(Fe3+)
Основные понятия БО
Слайд 16
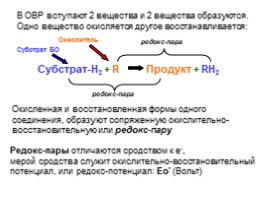
В ОВР вступают 2 вещества и 2 вещества образуются.
Одно вещество окисляется другое восстанавливается:
Субстрат-H2 + R Продукт + RH2
Окисленная и восстановленная формы одного соединения, образуют сопряженную окислительно-восстановительную или редокс-пару
редокс-пара
редокс-пара
Редокс-пары отличаются сродством к е-, мерой сродства служит окислительно-восстановительный потенциал, или редокс-потенциал: Ео' (Вольт)
Субстрат БО
Окислитель
Субстрат-H2 + R Продукт + RH2
Окисленная и восстановленная формы одного соединения, образуют сопряженную окислительно-восстановительную или редокс-пару
редокс-пара
редокс-пара
Редокс-пары отличаются сродством к е-, мерой сродства служит окислительно-восстановительный потенциал, или редокс-потенциал: Ео' (Вольт)
Субстрат БО
Окислитель
Слайд 17

Каждое вещество обладает определенным запасом внутренней энергии (Е).
Часть внутренней энергии, которая может быть использована для совершения полезной работы, называют свободной (G).
∆G = Ео'(SH2/S) – Ео'(R/RH2)
-0,42В
НАДН2
О2
+0,82В
е-
∆G =-1,12= 0,82- (-0,32)
Часть внутренней энергии, которая может быть использована для совершения полезной работы, называют свободной (G).
∆G = Ео'(SH2/S) – Ео'(R/RH2)
-0,42В
НАДН2
О2
+0,82В
е-
∆G =-1,12= 0,82- (-0,32)
Слайд 18

Биологическое окисление (БО) - совокупность окислительно-восстановительных реакций в живых клетках.
Особенности реакций БО:
протекают в аэробных и анаэробных условия;
катализируются оксидоредуктазами;
являются многостадийным процессом;
Существует несколько путей их использования: основной - синтез АТФ (90%), а также синтез новых веществ, разрушения ксенобиотиков и продуктов метаболизма.
Субстрат БО – вещество, способное отдавать электрон. (вещества, способные вступать в реакции окисления)
Субстрат-H2
Субстрат БО – вещество, способное отдавать электрон. (вещества, способные вступать в реакции окисления)
Субстрат-H2
Слайд 19

Дыхательная цепь – цепь переноса электронов.
В переносе электронов от субстратов БО к О2 принимают участие:
НАД– и НАДФ– зависимые ДГ;
ФАД– и ФМН– зависимые ДГ;
Цитохромы;
Коэнзим Q;
Белки, содержащие негеминовое железо.
Слайд 20
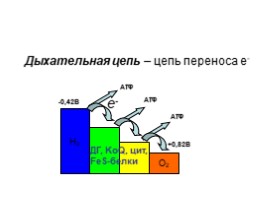
-0,42В
+0,82В
Н2
О2
е-
АТФ
АТФ
АТФ
Дыхательная цепь – цепь переноса е-
ДГ, KoQ, цит, FeS-белки
+0,82В
Н2
О2
е-
АТФ
АТФ
АТФ
Дыхательная цепь – цепь переноса е-
ДГ, KoQ, цит, FeS-белки
Слайд 21

В настоящее время выделено 4 основные пути использования О2 в организме:
Оксидазный путь
Функция: 90% О2 используется для синтеза АТФ;
Монооксигеназный путь (Обеспечивает включение 1 атома кислорода в молекулу субстрата)
Функции:
синтез новых веществ (стероидные гормоны),
обезвреживание ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР;
Пути использования О2 в клетке
Пути использования О2 в клетке
Слайд 22

Диоксигеназный путь (Обеспечивает включение молекулы кислорода в молекулу субстрата)
Функция:
деградация АК;
синтез новых веществ;
Свободно-радикальный путь
Функции:
внутриклеточное пищеварение;
разрушение бактерий, вирусов, онко- и стареющих клеток;
образование БАВ.
Слайд 23
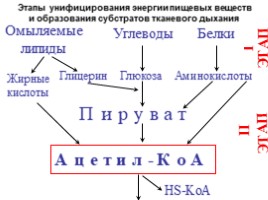
Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания
Омыляемые липиды
Углеводы
Белки
Глицерин
Глюкоза
А
м
и
н
о
к
и
с
л
о
т
ы
Жирные кислоты
Омыляемые липиды
Углеводы
Белки
Глицерин
Глюкоза
А
м
и
н
о
к
и
с
л
о
т
ы
Жирные кислоты
Слайд 24
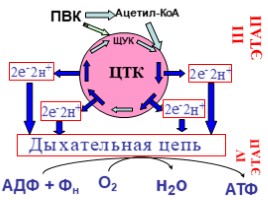
АДФ + Фн
О2
н2о
АТФ
ЦТК
Ацетил-КоА
ЩУК
ПВК
О2
н2о
АТФ
ЦТК
Ацетил-КоА
ЩУК
ПВК
Слайд 25
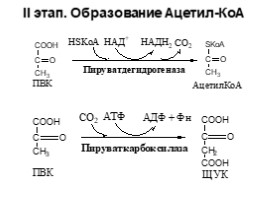
II этап. Образование Ацетил-КоА
Слайд 26

ЦТК является процессом окисления Ацетил–КоА - универсального продукта катаболизма углеводов, белков и омыляемых липидов;
ЦТК протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе в свободном состоянии, или на внутренней поверхности внутренней мембраны;
В ЦТК участвуют 5 витаминов В1, В2, РР, пантотеновая кислота и липоевая кислота в виде коферментов тиаминпирофосфата, ФАД, НАД+, КоА и липоата.
III этап. Цикл Кребса (цикл трикарбоновых кислот)
III этап. Цикл Кребса (цикл трикарбоновых кислот)
Слайд 27
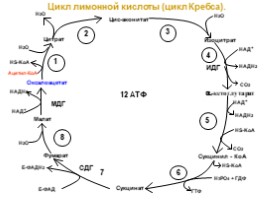
Цикл лимонной кислоты (цикл Кребса).
Цис-аконитат
Изоцитрат
Сукцинил - КоА
Сукцинат
Цитрат
Оксалоацетат
Малат
Фумарат
12 АТФ
МДГ
СДГ
ИДГ
-кетоглутарат
Цис-аконитат
Изоцитрат
Сукцинил - КоА
Сукцинат
Цитрат
Оксалоацетат
Малат
Фумарат
12 АТФ
МДГ
СДГ
ИДГ
-кетоглутарат
Слайд 28
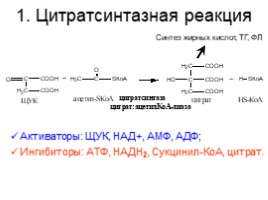
1. Цитратсинтазная реакция
Активаторы: ЩУК, НАД+, АМФ, АДФ; Ингибиторы: АТФ, НАДН2, Сукцинил-КоА, цитрат.
Синтез жирных кислот, ТГ, ФЛ
Активаторы: ЩУК, НАД+, АМФ, АДФ; Ингибиторы: АТФ, НАДН2, Сукцинил-КоА, цитрат.
Синтез жирных кислот, ТГ, ФЛ
Слайд 29
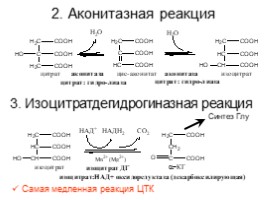
2. Аконитазная реакция
3. Изоцитратдегидрогиназная реакция
Самая медленная реакция ЦТК
Синтез Глу
3. Изоцитратдегидрогиназная реакция
Самая медленная реакция ЦТК
Синтез Глу
Слайд 30

4.α-Кетоглутаратдегидрогиназная реакция
Активаторы: ионы Са; Ингибиторы: АТФ, сукцинил-КоА, НАДH2; α-КГДГ комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД.
Синтез гема
Активаторы: ионы Са; Ингибиторы: АТФ, сукцинил-КоА, НАДH2; α-КГДГ комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД.
Синтез гема
Слайд 31

5. Сукцинил-КоА-синтетазная реакция
Это - единственная стадия ЦТК, в ходе которой генерируется высокоэнергетическая фосфатная связь на субстратном уровне; Это реакция субстратного фосфорилирования.
Субстратное фосфорилирование
Это - единственная стадия ЦТК, в ходе которой генерируется высокоэнергетическая фосфатная связь на субстратном уровне; Это реакция субстратного фосфорилирования.
Субстратное фосфорилирование
Слайд 32
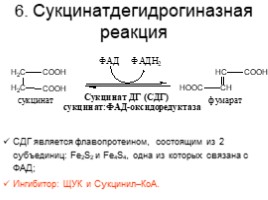
6. Сукцинатдегидрогиназная реакция
СДГ является флавопротеином, состоящим из 2 субъединиц: Fe2S2 и Fe4S4, одна из которых связана с ФАД; Ингибитор: ЩУК и Сукцинил–КоА.
СДГ является флавопротеином, состоящим из 2 субъединиц: Fe2S2 и Fe4S4, одна из которых связана с ФАД; Ингибитор: ЩУК и Сукцинил–КоА.
Слайд 33
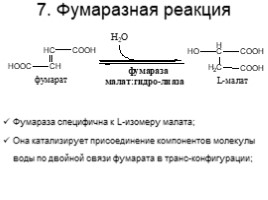
7. Фумаразная реакция
Фумараза специфична к L-изомеру малата; Она катализирует присоединение компонентов молекулы воды по двойной связи фумарата в транс-конфигурации;
Фумараза специфична к L-изомеру малата; Она катализирует присоединение компонентов молекулы воды по двойной связи фумарата в транс-конфигурации;
Слайд 34
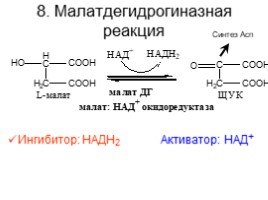
8. Малатдегидрогиназная реакция
Ингибитор: НАДН2 Активатор: НАД+
Синтез Асп
Ингибитор: НАДН2 Активатор: НАД+
Синтез Асп
Слайд 35
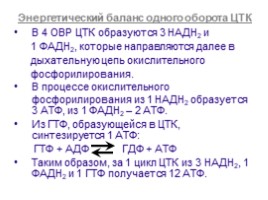
Энергетический баланс одного оборота ЦТК
В 4 ОВР ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования из 1 НАДН2 образуется 3 АТФ, из 1 ФАДН2 – 2 АТФ. Из ГТФ, образующейся в ЦТК, синтезируется 1 АТФ: ГТФ + АДФ ГДФ + АТФ Таким образом, за 1 цикл ЦТК из 3 НАДН2, 1 ФАДН2 и 1 ГТФ получается 12 АТФ.
В 4 ОВР ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования из 1 НАДН2 образуется 3 АТФ, из 1 ФАДН2 – 2 АТФ. Из ГТФ, образующейся в ЦТК, синтезируется 1 АТФ: ГТФ + АДФ ГДФ + АТФ Таким образом, за 1 цикл ЦТК из 3 НАДН2, 1 ФАДН2 и 1 ГТФ получается 12 АТФ.
Слайд 36

Регуляция ЦТК
Регуляторные (ключевые, лимитирующие) ферменты: Цитратсинтаза изоцитрат ДГ α-КГ ДГ СДГ Ингибирует – НАДН2 и АТФ, которые являются продуктами ЦТК и дыхательной цепи Активируют – НАД+ и АДФ Первая - пусковая реакция ЦТК зависит от концентрации ЩУК, Ацетил-КоА
Регуляторные (ключевые, лимитирующие) ферменты: Цитратсинтаза изоцитрат ДГ α-КГ ДГ СДГ Ингибирует – НАДН2 и АТФ, которые являются продуктами ЦТК и дыхательной цепи Активируют – НАД+ и АДФ Первая - пусковая реакция ЦТК зависит от концентрации ЩУК, Ацетил-КоА
Слайд 37
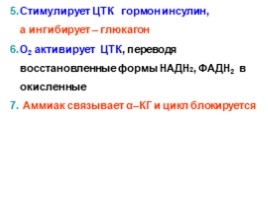
Стимулирует ЦТК гормон инсулин, а ингибирует – глюкагон
O2 активирует ЦТК, переводя восстановленные формы НAДH2, ФAДH2 в окисленные
Аммиак связывает α–КГ и цикл блокируется
Слайд 38

Биологическое значение ЦТК
1. образование водородных эквивалентов, которые в цепи ОФ обеспечивают синтез АТФ; 2. выполняет ведущую роль в: глюконеогенезе; переаминировании и дезаминировании АК; синтезе жирный кислот и липогенезе; синтезе гема.
3. интегрирует все виды обмена веществ
1. образование водородных эквивалентов, которые в цепи ОФ обеспечивают синтез АТФ; 2. выполняет ведущую роль в: глюконеогенезе; переаминировании и дезаминировании АК; синтезе жирный кислот и липогенезе; синтезе гема.
3. интегрирует все виды обмена веществ
Слайд 39

IV этап. Окислительное фосфорилирование
В 1966г. английский ученый Питер Денис Митчелл сформулировал хемиосмотическую гипотезу объясняющую принцип окислительного фосфорилирования. В 1979г. - Нобелевская премия
История окислительного фосфорилирования
В 1966г. английский ученый Питер Денис Митчелл сформулировал хемиосмотическую гипотезу объясняющую принцип окислительного фосфорилирования. В 1979г. - Нобелевская премия
История окислительного фосфорилирования
Слайд 40

цепь реакций, осуществляющихся в процессе дыхания, представляет собой последовательность сменяющих друг друга протонов и электронов.
Белковые носители таким образом организованы во внутренней митохондриальной мембране, что переносят протоны через мембрану.
Поскольку митохондриальная мембрана не допускает пассивного тока протонов, в процессе дыхания генерируется электрохимическая разность потенциалов – мембранный потенциал.
Под ее действием протоны с внешней поверхности стремятся назад во внутриклеточное пространство. Именно этот поток протонов, который можно сравнить с электрическим током в батарее, и выполняет всю работу.
Положения хемиосмотической теории
Положения хемиосмотической теории
Слайд 41
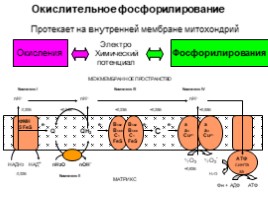
Окислительное фосфорилирование
Q
½О2 ½О2*
Н2О
НАДН2 НАД+
nН+
е-
QН2
nН2О
nОН-
nН+
АТФ синтаза
nН+
МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО
Фн + АДФ АТФ
C
Комплекс I
Комплекс III
Комплекс IV
е-
-0,32В
-0,30В
+0,04В
+0,25В
+0,55В
+0,82В
ФМН 5 FeS
B562 B566 C1 FeS
B562 B566 C1 FeS
a a3 Cu2+
a a3 Cu2+
МАТРИКС
е-
е-
+0,23В
Протекает на внутренней мембране митохондрий
Окисления
Электро Химический потенциал
Фосфорилирования
Комплекс II
Q
½О2 ½О2*
Н2О
НАДН2 НАД+
nН+
е-
QН2
nН2О
nОН-
nН+
АТФ синтаза
nН+
МЕЖМЕМБРАННОЕ ПРОСТРАНСТВО
Фн + АДФ АТФ
C
Комплекс I
Комплекс III
Комплекс IV
е-
-0,32В
-0,30В
+0,04В
+0,25В
+0,55В
+0,82В
ФМН 5 FeS
B562 B566 C1 FeS
B562 B566 C1 FeS
a a3 Cu2+
a a3 Cu2+
МАТРИКС
е-
е-
+0,23В
Протекает на внутренней мембране митохондрий
Окисления
Электро Химический потенциал
Фосфорилирования
Комплекс II
Слайд 42
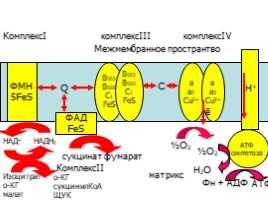
ФМН
5FеS
ФАД FeS
В562 В566 С1 FeS
В562 В566 С1 FeS
а а3 Сu2+
а а3 Сu2+
АТФ синтетаза
Q
C
НАД+
НАДН2
Изоцитрат α-КГ малат
α-КГ сукцинилКоА ЩУК
сукцинат
фумарат
½О2
½О2*
Н2О
АТФ
Фн + АДФ
КомплексΙΙ
КомплексΙ
комплексΙΙΙ
комплексΙV
Межмембранное пространтво
матрикс
окисление
ē
Н+
ФАД FeS
В562 В566 С1 FeS
В562 В566 С1 FeS
а а3 Сu2+
а а3 Сu2+
АТФ синтетаза
Q
C
НАД+
НАДН2
Изоцитрат α-КГ малат
α-КГ сукцинилКоА ЩУК
сукцинат
фумарат
½О2
½О2*
Н2О
АТФ
Фн + АДФ
КомплексΙΙ
КомплексΙ
комплексΙΙΙ
комплексΙV
Межмембранное пространтво
матрикс
окисление
ē
Н+
Слайд 43
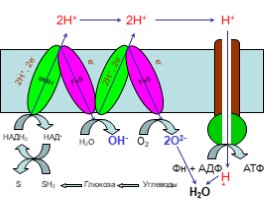
ФМН
FeS
НАДН2 НАД+
S SH2
Глюкоза Углеводы
2Н+, 2е-
е-
2Н+
FeS
2Н+, 2е-
е-
2Н+
Н2О ОН-
О2 2О2-
Н+
Н+
Фн + АДФ АТФ
Н2О
FeS
НАДН2 НАД+
S SH2
Глюкоза Углеводы
2Н+, 2е-
е-
2Н+
FeS
2Н+, 2е-
е-
2Н+
Н2О ОН-
О2 2О2-
Н+
Н+
Фн + АДФ АТФ
Н2О
Слайд 44
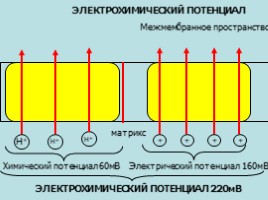
Н+
Н+
Н+
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ
Межмембранное пространство
Химический потенциал 60мВ
матрикс
+
+
+
+
Электрический потенциал 160мВ
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ 220мВ
Н+
Н+
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ
Межмембранное пространство
Химический потенциал 60мВ
матрикс
+
+
+
+
Электрический потенциал 160мВ
ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ 220мВ
Слайд 45
Н+
Н+
Н+
ē
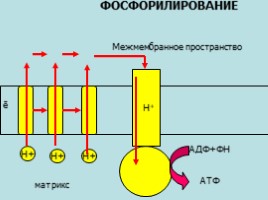
ФОСФОРИЛИРОВАНИЕ
АДФ+ФН
АТФ
Н+
Межмембранное пространство
матрикс
Н+
Н+
ē
ФОСФОРИЛИРОВАНИЕ
АДФ+ФН
АТФ
Н+
Межмембранное пространство
матрикс
Слайд 46

Модель F1 и F0 компонентов АТФ-синтазы – молекулярной машины
a, b, альфа, бета и дельта субъединицы образуют статор машины с, гамма и ипсилон субъединицы образуют ротор
a, b, альфа, бета и дельта субъединицы образуют статор машины с, гамма и ипсилон субъединицы образуют ротор
Слайд 47
Н+
Н+
Н+
ē
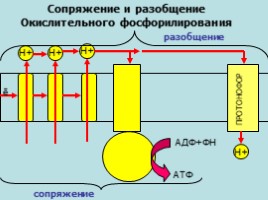
Сопряжение и разобщение Окислительного фосфорилирования
АДФ+ФН
АТФ
сопряжение
Н+
разобщение
ПРОТОНОФОР
Н+
Н+
ē
Сопряжение и разобщение Окислительного фосфорилирования
АДФ+ФН
АТФ
сопряжение
Н+
разобщение
ПРОТОНОФОР
Слайд 48
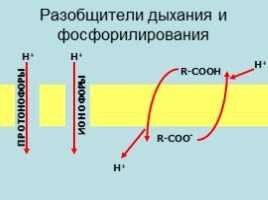
Разобщители дыхания и фосфорилирования
R-СООН
R-СОО-
Н+
Н+
ПРОТОНОФОРЫ
ИОНОФОРЫ
Н+
Н+
R-СООН
R-СОО-
Н+
Н+
ПРОТОНОФОРЫ
ИОНОФОРЫ
Н+
Н+
Слайд 49

2,4-Динитрофенол
2,4-динитрофенол является классическим разобщителем окислительного фосфорилирования. При действии на митохондрии стимулирует их дыхание, но ингибирует сопряженное с ним фосфорилирование, т.е. синтез АТФ из АДФ и фосфата.
2,4-динитрофенол является классическим разобщителем окислительного фосфорилирования. При действии на митохондрии стимулирует их дыхание, но ингибирует сопряженное с ним фосфорилирование, т.е. синтез АТФ из АДФ и фосфата.
Слайд 50

Дыхательный контроль
- Зависимость интенсивности дыхания митохондрий от концентрации АДФ. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г Молекула АТФ «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается.
- Зависимость интенсивности дыхания митохондрий от концентрации АДФ. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г Молекула АТФ «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается.
Слайд 51

Спасибо за внимание!
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
