Презентация - Курс «Материаловедение»
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 86%
- Слайдов: 19
- Просмотров: 4588
- Скачиваний: 1864
- Размер: 5.33 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Виртуальная экскурсия по городам Чувашии
Виртуальная экскурсия по городам Чувашии Виртуальная экскурсия «Храмы Воловского района Липецкой области»
Виртуальная экскурсия «Храмы Воловского района Липецкой области» Конкурс знатоков русского языка для 5-6 классов
Конкурс знатоков русского языка для 5-6 классов Виртуальная экскурсия «Разнообразие рек Краснодарского края»
Виртуальная экскурсия «Разнообразие рек Краснодарского края» Урок-экскурсия по лесу «Делим числа»
Урок-экскурсия по лесу «Делим числа» Золотое кольцо России. Интерактивная экскурсия
Золотое кольцо России. Интерактивная экскурсия Всероссийский дистанционный конкурс «Кот ученый» посвящен писателю-юбиляру Аркадию Петровичу Гайдару
Всероссийский дистанционный конкурс «Кот ученый» посвящен писателю-юбиляру Аркадию Петровичу Гайдару
Слайды и текст этой онлайн презентации
Слайд 1

Курс «Материаловедение» Лекции: 51 час (16 раз 1 (2) лекции) Лабораторные работы: 17 часов (4 раза х 2 л р) Домашнее задание: сдача защита на лабораторном практикуме Самостоятельная проработка курса: 30 часов Лектор: Минаков Александр Александрович 101 ауд. ГУК, УДЦ «Физико-механические свойства материалов» электронная почта: labmatved yandex.ru моб. телефон: 8-915-344-72-70
Слайд 2

Как найти 101 ауд. ?
Слайд 3

Модули I II III IV Лабораторный практикум 1-ая часть курса Экзамен 4 раза х 2 л р 8 л р по II части 0...25 баллов 0...25 баллов (выполнение защита) курса Оц1 Оц2 Домашнее задание 0...30 баллов (0-14 «2»; 15-17 «3»; (выполнение защита) (0-17 «2»; 18-20 18-20 «4»; 21-25 «5») 0...20 баллов «3»; 21-25 «4»; <12 баллов незачёт по лаб-му Если: 26-30 «5») «2» незачёт данные практикуму недопуск до модули выносятся на экзамена экзамен; (0-11 «2»; 12-13 «3»; 14-16 от «3» до «5» «4»; 17-20 «5») зачёт данные модули не 0...20 0...30 0...50 баллов Оц3 выносятся на экзамен. (0-29 «2»; 30-33 «3»; 34-41 «4»; 42-50 «5») Если: «2» незачёт по II части курса > экзамен на пересдачу; от «3» до «5» зачёт по II части курса. Итог по экзамену (при успешной сдаче всего перечисленного) Оценка за экзамен ( Оц1 Оц2 Оц3 ) 3
Слайд 4

Лабораторные работы проходят на кафедре МТ-8 в ГУК (3-ий этаж вверх по лестнице над сбербанком). Номер кабинета НЕ совпадает с номером л р, найти кабинет поможет дежурный инженер из кабинета № 13) На л р приходить подготовленными по теории! Верхнюю одежду перед л р сдавать в гардероб. номера лабораторных работ группа преподаватели 2,3 7,8 5,6 9,10 РК 4 51; РК 4 59 вторник Фахуртдинов Р. С. 24 сентября 8 октября 22 октября 5 ноября (8-30 11-50) Карпухин С. Д. РК 4 52 вторник Мохова А. С. Смирнов А. Е. 29 октября 12 ноября 26 ноября 10 декабря (12-00 15-25) - названия лабораторных работ смотри с методических указаниях (будут присланы мной старосте Вашей группы)
Слайд 5
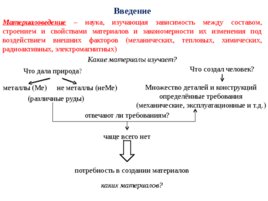
Введение Материаловедение наука, изучающая зависимость между составом, строением и свойствами материалов и закономерности их изменения под воздействием внешних факторов (механических, тепловых, химических, радиоактивных, электромагнитных) Какие материалы изучает? Что дала природа? Что создал человек? металлы (Ме) не металлы (не Ме) Множество деталей и конструкций определённые требования (различные руды) (механические, эксплуатационные и т.д.) отвечают ли требованиям? чаще всего нет потребность в создании материалов каких материалов?
Слайд 6

Конструкционные материалы это такие материалы, из которых изготавливаются различные виды конструкций и деталей машин, воспринимающих силовые нагрузки. Основные конструкционные материалы: Новые классы конструкционных 90 % от всех материалов: 1) сплавы на основе Fe («чёрные 10 % от всех металлы») сталь и чугун; - полупроводники; 2) сплавы на основе Al, Cu, Ti и т.д. - пластические массы; («цветные металлы»). - композиционные материалы; - аморфные сплавы; - металлокерамики; - сверхпроводящие керамики; - наноматериалы; - материалы с памятью формы и т.д. Конструкционные материалы обладают комплексом свойств и характеристик, отвечающих заданным требованиям А как получить эти свойства и повлиять на них?
Слайд 7

СВОЙСТВА ХИМИЧЕСКИЙ СОСТАВ СТРОЕНИЕ (СТРУКТУРА) А как повлиять на хим-ий состав и структуру? Этапы технологии металлов: I Металлургия получение металла заданного состава (косвенно и формы) Изменение II Механическая технология получение из металла изделий структуры заданной внешней формы на всех III Термическая обработка (Т. О.) или химико-термическая этапах обработка (Х. Т. О.) получение заданных (!!!) свойств Содержание курса I часть курса «Закономерности формирования структуры и способы управления свойствами материалов» (32 часа 16 лекций 10,5 недель 2 модуля) II часть курса «Материалы, применяемые в машиностроении» (19 часов 9,5 лекций 6,5 недель модуль-экзамен)
Слайд 8

I часть «Закономерности формирования структуры и способы управления свойствами материалов» 3 главы 3 главы ( I модуль ) ( II модуль ) Глава I «Кристаллическое строение Глава IV «Сплавы. Влияние химического материалов» состава сплава на структуру сплавов» Глава II «Формирование структуры Глава V «Влияние термической обработки металла в процессе литья» на структуру и свойства сплавов» Глава III «Формирование структуры Глава VI «Влияние химико-термической металла при деформировании» обработки и поверхностной термической обработки на структуру и свойства сплавов»
Слайд 9
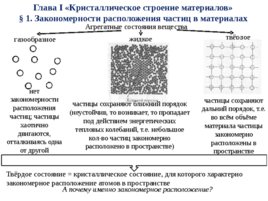
Глава I «Кристаллическое строение материалов» 1. Закономерности расположения частиц в материалах Агрегатные состояния вещества газообразное жидкое твёрдое нет закономерности частицы сохраняют ближний порядок частицы сохраняют расположения (неустойчив, то возникает, то пропадает дальний порядок, т.е. частиц; частицы под действием энергетических во всём объёме хаотично тепловых колебаний, т.е. небольшое материала частицы двигаются, кол-во частиц закономерно закономерно отталкиваясь одна расположено в пространстве) расположены в от другой пространстве Твёрдое состояние кристаллическое состояние, для которого характерно закономерное расположение атомов в пространстве А почему именно закономерное расположение?
Слайд 10
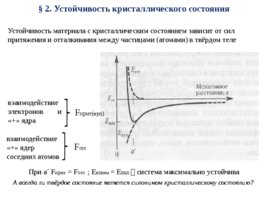
2. Устойчивость кристаллического состояния Устойчивость материала с кристаллическим состоянием зависит от сил притяжения и отталкивания между частицами (атомами) в твёрдом теле взаимодействие электронов и Fприт(кул) « » ядра взаимодействие « » ядер Fотт соседних атомов При a Fприт Fотт ; Eвзаим Emin система максимально устойчива А всегда ли твёрдое состояние является синонимом кристаллическому состоянию?
Слайд 11
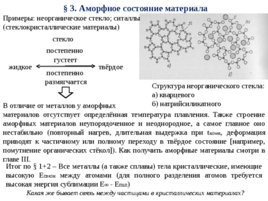
3. Аморфное состояние материала Примеры: неорганическое стекло; ситаллы (стеклокристаллические материалы) стекло постепенно густеет жидкое твёрдое постепенно размягчается Структура неорганического стекла: а) кварцевого б) натрийсиликатного В отличие от металлов у аморфных материалов отсутствует определённая температура плавления. Также строение аморфных материалов неупорядоченное и неоднородное, а самое главное оно нестабильно (повторный нагрев, длительная выдержка при tкомн, деформация приводят к частичному или полному переходу в твёрдое состояние например, помутнение органических стёкол ). Как получить аморфные материалы смотри в главе III. Итог по 1 2 Все металлы (а также сплавы) тела кристаллические, имеющие высокую Eсвязи между атомами (для полного разделения атомов требуется высокая энергия сублимации E - Emin) Какая же бывает связь между частицами в кристаллических материалах?
Слайд 12

4. Типы связей в кристаллических материалах А. Молекулярная связь (силы Ван-дер-Ваальса): - между атомами молекулами ионами (H2, Y2, Cl2, H2O, CO2, органические вещества); - образование диполей при поляризации; - связь ненаправленная, т.к. соседние частицы равноценны; - укладка частиц компактная; - связь слабая (Eсвязи 0,1-1 к Дж моль) Свойства кристаллов: низкая tплавл, диэлектрики.
Слайд 13
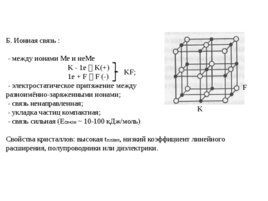
Б. Ионная связь : - между ионами Ме и не Ме K - 1e K( ) KF; 1e F F (-) - электростатическое притяжение между F разноимённо-заряженными ионами; - связь ненаправленная; - укладка частиц компактная; K - связь сильная (Eсвязи 10-100 к Дж моль) Свойства кристаллов: высокая tплавл, низкий коэффициент линейного расширения, полупроводники или диэлектрики.
Слайд 14
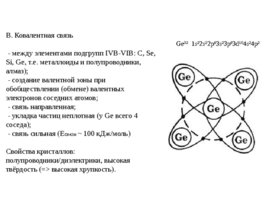
В. Ковалентная связь Ge32 1s22s22p63s23p63d104s24p2 - между элементами подгрупп IVB-VIB: C, Se, Si, Ge, т.е. металлоиды и полупроводники, алмаз); - создание валентной зоны при обобществлении (обмене) валентных электронов соседних атомов; - связь направленная; - укладка частиц неплотная (у Ge всего 4 соседа); - связь сильная (Eсвязи 100 к Дж моль) Свойства кристаллов: полупроводники диэлектрики, высокая твёрдость ( > высокая хрупкость).
Слайд 15
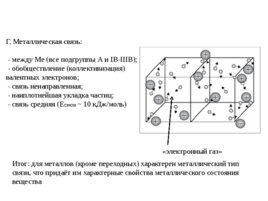
Г. Металлическая связь: - между Ме (все подгруппы А и IB-IIIB); - обобществление (коллективизация) валентных электронов; - связь ненаправленная; - наиплотнейшая укладка частиц; - связь средняя (Eсвязи 10 к Дж моль) «электронный газ» Итог: для металлов (кроме переходных) характерен металлический тип связи, что придаёт им характерные свойства металлического состояния вещества
Слайд 16
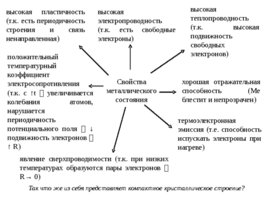
высокая пластичность высокая высокая (т.к. есть периодичность электропроводность теплопроводность строения и связь (т.к. есть свободные (т.к. высокая ненаправленная) электроны) подвижность свободных положительный электронов) температурный коэффициент Свойства электросопротивления хорошая отражательная металлического (т.к. с t увеличивается способность (Ме состояния колебания атомов, блестит и непрозрачен) нарушается периодичность термоэлектронная потенциального поля эмиссия (т.е. способность подвижность электронов испускать электроны при R) нагреве) явление сверхпроводимости (т.к. при низких температурах образуются пары электронов R 0) Так что же из себя представляет компактное кристаллическое строение?
Слайд 17

5. Атомно-кристаллическая структура Ме (идеальный случай) Атомно-кристаллическая структура это взаимное расположение атомов (т.е. ионов) в кристалле. Кристалл это совокупность атомов (т.е. ионов), расположенных в определённой последовательности, повторяющаяся периодически в пространстве и имеющая правильную геометрическую форму. Для описания атомно-кристаллической структуры используется понятие кристаллическая решётка (КР). КР воображаемая пространственная сетка, в узлах которой располагаются атомы (т.е. ионы), образующие Ме. Для описания любой КР вводится понятие элементарной кристаллической ячейки (ЭЯ). ЭЯ наименьший объём кристалла, последовательным перемещением которого в пространстве вдоль 3-х осей может быть построена вся КР.
Слайд 18
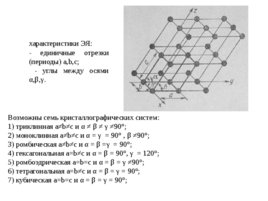
характеристики ЭЯ: - единичные отрезки (периоды) a,b,c; - углы между осями α,β,γ. Возможны семь кристаллографических систем: 1) триклинная a b c и α β γ 90 ; 2) моноклинная a b c и α γ 90 , β 90 ; 3) ромбическая a b c и α β γ 90 ; 4) гексагональная a b c и α β 90 , γ 120 ; 5) ромбоэдрическая a b c и α β γ 90 ; 6) тетрагональная a b c и α β γ 90 ; 7) кубическая a b c и α β γ 90 ;
Слайд 19
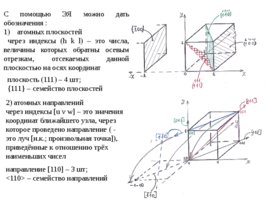
С помощью ЭЯ можно дать обозначения : 1) атомных плоскостей через индексы (h k l) это числа, величины которых обратны осевым отрезкам, отсекаемых данной плоскостью на осях координат плоскость (111) 4 шт; 111 семейство плоскостей 2) атомных направлений через индексы u v w это значения координат ближайшего узла, через которое проведено направление ( - это луч н.к.; произвольная точка ), приведённые к отношению трёх наименьших чисел направление 110 3 шт; <110> семейство направлений
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
