Презентация - Глобальные регуляторные системы бактерий
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 81%
- Слайдов: 21
- Просмотров: 4003
- Скачиваний: 1827
- Размер: 0.82 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Биосфера – глобальная экологическая система
Биосфера – глобальная экологическая система Обобщение и систематизация знаний по теме «Глагол»
Обобщение и систематизация знаний по теме «Глагол» Система уроков по синтаксису сложного предложения в 9 классах «Тире и двоеточие в бессоюзном предложении»
Система уроков по синтаксису сложного предложения в 9 классах «Тире и двоеточие в бессоюзном предложении» Комплексная система управления «умный дом»
Комплексная система управления «умный дом» Организация системы контроля качества образования
Организация системы контроля качества образования Бактерии и болезни растений
Бактерии и болезни растений Рейтинговая система оценивания достижений учащихся
Рейтинговая система оценивания достижений учащихся
Слайды и текст этой онлайн презентации
Слайд 1
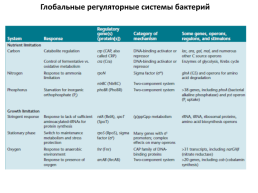
Глобальные регуляторные системы бактерий
Слайд 2
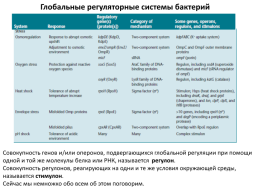
Глобальные регуляторные системы бактерий
Совокупность генов и/или оперонов, подвергающихся глобальной регуляции при помощи одной и той же молекулы белка или РНК, называется регулон. Совокупность регулонов, реагирующих на одни и те же условия окружающей среды, называется стимулон. Сейчас мы немножко обо всем об этом поговорим.
Совокупность генов и/или оперонов, подвергающихся глобальной регуляции при помощи одной и той же молекулы белка или РНК, называется регулон. Совокупность регулонов, реагирующих на одни и те же условия окружающей среды, называется стимулон. Сейчас мы немножко обо всем об этом поговорим.
Слайд 3
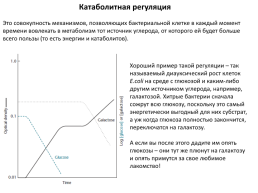
Катаболитная регуляция
Это совокупность механизмов, позволяющих бактериальной клетке в каждый момент времени вовлекать в метаболизм тот источник углерода, от которого ей будет больше всего пользы (то есть энергии и катаболитов).
Хороший пример такой регуляции – так называемый диауксический рост клеток E.coli на среде с глюкозой и каким-либо другим источником углерода, например, галактозой. Хитрые бактерии сначала сожрут всю глюкозу, поскольку это самый энергетически выгодный для них субстрат, а уж когда глюкоза полностью закончится, переключатся на галактозу. А если вы после этого дадите им опять глюкозы – они тут же плюнут на галактозу и опять примутся за свое любимое лакомство!
Это совокупность механизмов, позволяющих бактериальной клетке в каждый момент времени вовлекать в метаболизм тот источник углерода, от которого ей будет больше всего пользы (то есть энергии и катаболитов).
Хороший пример такой регуляции – так называемый диауксический рост клеток E.coli на среде с глюкозой и каким-либо другим источником углерода, например, галактозой. Хитрые бактерии сначала сожрут всю глюкозу, поскольку это самый энергетически выгодный для них субстрат, а уж когда глюкоза полностью закончится, переключатся на галактозу. А если вы после этого дадите им опять глюкозы – они тут же плюнут на галактозу и опять примутся за свое любимое лакомство!
Слайд 4
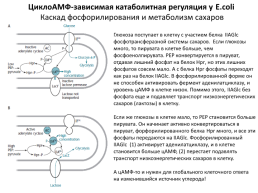
ЦиклоАМФ-зависимая катаболитная регуляция у E.coli
Каскад фосфорилирования и метаболизм сахаров
Глюкоза поступает в клетку с участием белка IIАGlc фосфотрансферазной системы сахаров. Если глюкозы много, то пирувата в клетке больше, чем фосфоенолпирувата. РЕР конвертируется в пируват, отдавая лишний фосфат на белок Hpr, но этих лишних фосфатов совсем мало. А с белка Hpr фосфаты переходят как раз на белок IIAGlc. В фосфорилированной форме он не способен активировать фермент аденилатциклазу, и уровень цАМФ в клетке низок. Помимо этого, IIAGlc без фосфата еще и подавляет транспорт низкоэнергетических сахаров (лактозы) в клетку. Если же глюкозы в клетке мало, то РЕР становится больше пирувата. Он начинает активно конвертироваться в пируват, форфорилированного белка Hpr много, и все эти фосфаты передаются на IIAGlc. Фосфорилированный IIAGlc (1) активирует аденилатциклазу, и в клетке становится больше цАМФ, (2) перестает подавлять транспорт низкоэнергетических сахаров в клетку. А цАМФ-то и нужен для глобального клеточного ответа на изменившийся источник углерода!
Глюкоза поступает в клетку с участием белка IIАGlc фосфотрансферазной системы сахаров. Если глюкозы много, то пирувата в клетке больше, чем фосфоенолпирувата. РЕР конвертируется в пируват, отдавая лишний фосфат на белок Hpr, но этих лишних фосфатов совсем мало. А с белка Hpr фосфаты переходят как раз на белок IIAGlc. В фосфорилированной форме он не способен активировать фермент аденилатциклазу, и уровень цАМФ в клетке низок. Помимо этого, IIAGlc без фосфата еще и подавляет транспорт низкоэнергетических сахаров (лактозы) в клетку. Если же глюкозы в клетке мало, то РЕР становится больше пирувата. Он начинает активно конвертироваться в пируват, форфорилированного белка Hpr много, и все эти фосфаты передаются на IIAGlc. Фосфорилированный IIAGlc (1) активирует аденилатциклазу, и в клетке становится больше цАМФ, (2) перестает подавлять транспорт низкоэнергетических сахаров в клетку. А цАМФ-то и нужен для глобального клеточного ответа на изменившийся источник углерода!
Слайд 5
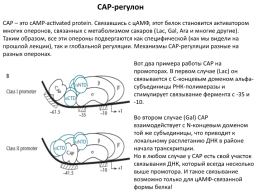
САР-регулон
САР – это cAMP-activated protein. Связавшись с цАМФ, этот белок становится активатором многих оперонов, связанных с метаболизмом сахаров (Lac, Gal, Ara и многие другие). Таким образом, все эти опероны подвергаются как специфической (как мы видели на прошлой лекции), так и глобальной регуляции. Механизмы САР-регуляции разные на разных оперонах.
Вот два примера работы САР на промоторах. В первом случае (Lac) он связывается с С-концевым доменом альфа-субъединицы РНК-полимеразы и стимулирует связывание фермента с -35 и -10. Во втором случае (Gal) САР взаимодействует с N-концевым доменом той же субъединицы, что приводит к локальному расплетанию ДНК в районе начала транскрипции. Но в любом случае у САР есть свой участок связывания ДНК, который всегда несколько выше промотора. И такое связывание возможно только для цАМФ-связанной формы белка!
САР – это cAMP-activated protein. Связавшись с цАМФ, этот белок становится активатором многих оперонов, связанных с метаболизмом сахаров (Lac, Gal, Ara и многие другие). Таким образом, все эти опероны подвергаются как специфической (как мы видели на прошлой лекции), так и глобальной регуляции. Механизмы САР-регуляции разные на разных оперонах.
Вот два примера работы САР на промоторах. В первом случае (Lac) он связывается с С-концевым доменом альфа-субъединицы РНК-полимеразы и стимулирует связывание фермента с -35 и -10. Во втором случае (Gal) САР взаимодействует с N-концевым доменом той же субъединицы, что приводит к локальному расплетанию ДНК в районе начала транскрипции. Но в любом случае у САР есть свой участок связывания ДНК, который всегда несколько выше промотора. И такое связывание возможно только для цАМФ-связанной формы белка!
Слайд 6
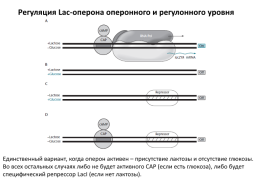
Регуляция Lac-оперона оперонного и регулонного уровня
Единственный вариант, когда оперон активен – присутствие лактозы и отсутствие глюкозы. Во всех остальных случаях либо не будет активного САР (если есть глюкоза), либо будет специфический репрессор LacI (если нет лактозы).
Единственный вариант, когда оперон активен – присутствие лактозы и отсутствие глюкозы. Во всех остальных случаях либо не будет активного САР (если есть глюкоза), либо будет специфический репрессор LacI (если нет лактозы).
Слайд 7
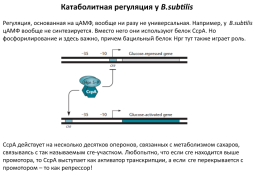
Катаболитная регуляция у B.subtilis
Регуляция, основанная на цАМФ, вообще ни разу не универсальная. Например, у B.subtilis цАМФ вообще не синтезируется. Вместо него они используют белок СсрА. Но фосфорилирование и здесь важно, причем бацильный белок Hpr тут также играет роль.
СсрА действует на несколько десятков оперонов, связанных с метаболизмом сахаров, связываясь с так называемым cre-участком. Любопытно, что если cre находится выше промотора, то СсрА выступает как активатор транскрипции, а если cre перекрывается с промотором – то как репрессор!
Регуляция, основанная на цАМФ, вообще ни разу не универсальная. Например, у B.subtilis цАМФ вообще не синтезируется. Вместо него они используют белок СсрА. Но фосфорилирование и здесь важно, причем бацильный белок Hpr тут также играет роль.
СсрА действует на несколько десятков оперонов, связанных с метаболизмом сахаров, связываясь с так называемым cre-участком. Любопытно, что если cre находится выше промотора, то СсрА выступает как активатор транскрипции, а если cre перекрывается с промотором – то как репрессор!
Слайд 8
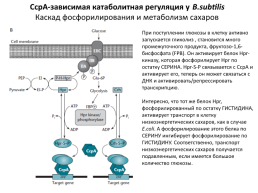
СсрА-зависимая катаболитная регуляция у B.subtilis
Каскад фосфорилирования и метаболизм сахаров
При поступлении глюкозы в клетку активно запускается гликолиз , становится много промежуточного продукта, фруктозо-1,6-бисфосфата (FPB). Он активирует белок Hpr-киназу, которая фосфорилирует Hpr по остатку СЕРИНА. Hpr-S-P связывается с СсрА и активирует его, теперь он может связаться с ДНК и активировать/репрессировать транскрипцию. Интересно, что тот же белок Hpr, фосфорилированный по остатку ГИСТИДИНА, активирует транспорт в клетку низкоэнергетических сахаров, как в случае E.coli. А фосфорилирование этого белка по СЕРИНУ ингибирует фосфорилирование по ГИСТИДИНУ. Соответственно, транспорт низкоэнергетических сахаров получается подавленным, если имеется большое количество глюкозы.
При поступлении глюкозы в клетку активно запускается гликолиз , становится много промежуточного продукта, фруктозо-1,6-бисфосфата (FPB). Он активирует белок Hpr-киназу, которая фосфорилирует Hpr по остатку СЕРИНА. Hpr-S-P связывается с СсрА и активирует его, теперь он может связаться с ДНК и активировать/репрессировать транскрипцию. Интересно, что тот же белок Hpr, фосфорилированный по остатку ГИСТИДИНА, активирует транспорт в клетку низкоэнергетических сахаров, как в случае E.coli. А фосфорилирование этого белка по СЕРИНУ ингибирует фосфорилирование по ГИСТИДИНУ. Соответственно, транспорт низкоэнергетических сахаров получается подавленным, если имеется большое количество глюкозы.
Слайд 9
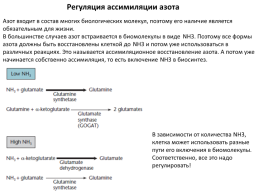
Регуляция ассимиляции азота
Азот входит в состав многих биологических молекул, поэтому его наличие является обязательным для жизни. В большинстве случаев азот встраивается в биомолекулы в виде NH3. Поэтому все формы азота должны быть восстановлены клеткой до NH3 и потом уже использоваться в различных реакциях. Это называется ассимиляционное восстановление азота. А потом уже начинается собственно ассимиляция, то есть включение NH3 в биосинтез.
В зависимости от количества NH3, клетка может использовать разные пути его включения в биомолекулы. Соответственно, все это надо регулировать!
Азот входит в состав многих биологических молекул, поэтому его наличие является обязательным для жизни. В большинстве случаев азот встраивается в биомолекулы в виде NH3. Поэтому все формы азота должны быть восстановлены клеткой до NH3 и потом уже использоваться в различных реакциях. Это называется ассимиляционное восстановление азота. А потом уже начинается собственно ассимиляция, то есть включение NH3 в биосинтез.
В зависимости от количества NH3, клетка может использовать разные пути его включения в биомолекулы. Соответственно, все это надо регулировать!
Слайд 10
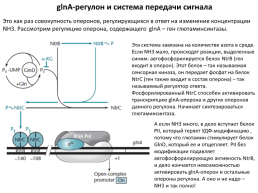
glnA-регулон и система передачи сигнала
Это как раз совокупность оперонов, регулирующихся в ответ на изменение концентрации NH3. Рассмотрим регуляцию оперона, содержащего glnA – ген глютаминсинтазы.
Эта система завязана на количестве азота в среде. Если NH3 мало, происходят реакции, выделенные синим: автофосфорилируется белок NtrB (ген входит в оперон). Этот белок – так называемая сенсорная киназа, он передает фосфат на белок NtrC (ген также входит в состав оперона) – так называемый регулятор ответа. Фосфорилированный NtrC способен активировать транскрипцию glnA-оперона и других оперонов данного регулона. Начинает синтезироваться глютаминсинтаза.
А если NH3 много, в дело вступает белок PII, который теряет УДФ-модификацию , потому что глютамин стимулирует белок GlnD, который ее и отщепляет. PII без модификации подавляет автофосфорилирующую активность NtrB, и дело кончается невозможностью активировать glnA-оперон и остальные опероны регулона. А оно и не надо – NH3 и так полно!
Это как раз совокупность оперонов, регулирующихся в ответ на изменение концентрации NH3. Рассмотрим регуляцию оперона, содержащего glnA – ген глютаминсинтазы.
Эта система завязана на количестве азота в среде. Если NH3 мало, происходят реакции, выделенные синим: автофосфорилируется белок NtrB (ген входит в оперон). Этот белок – так называемая сенсорная киназа, он передает фосфат на белок NtrC (ген также входит в состав оперона) – так называемый регулятор ответа. Фосфорилированный NtrC способен активировать транскрипцию glnA-оперона и других оперонов данного регулона. Начинает синтезироваться глютаминсинтаза.
А если NH3 много, в дело вступает белок PII, который теряет УДФ-модификацию , потому что глютамин стимулирует белок GlnD, который ее и отщепляет. PII без модификации подавляет автофосфорилирующую активность NtrB, и дело кончается невозможностью активировать glnA-оперон и остальные опероны регулона. А оно и не надо – NH3 и так полно!
Слайд 11

glnA-оперон устроен любопытным образом
В этом опероне три промотора, но только один (р2) подвержен NtrC-зависимой регуляции. Это потому, что остальные промоторы могут узнаваться обычной РНК-полимеразой с сигма70-субъединицей. А вот р2 подходит только для фермента с нестандартной сигма54-субъединицей.
Никаких -35 и -10 элементов в промоторах для сигмы54 (она же сигмаN) нет, вместо этого есть совсем другие элементы, -24 и -12.
Промоторы р1 и р3 нужны для того, чтобы в клетке даже в случае большого количества NH3 в среде имелись малые количества глютаминсинтазы, она же все равно нужна.
В этом опероне три промотора, но только один (р2) подвержен NtrC-зависимой регуляции. Это потому, что остальные промоторы могут узнаваться обычной РНК-полимеразой с сигма70-субъединицей. А вот р2 подходит только для фермента с нестандартной сигма54-субъединицей.
Никаких -35 и -10 элементов в промоторах для сигмы54 (она же сигмаN) нет, вместо этого есть совсем другие элементы, -24 и -12.
Промоторы р1 и р3 нужны для того, чтобы в клетке даже в случае большого количества NH3 в среде имелись малые количества глютаминсинтазы, она же все равно нужна.
Слайд 12
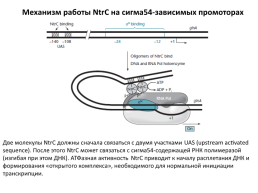
Механизм работы NtrC на сигма54-зависимых промоторах
Две молекулы NtrC должны сначала связаться с двумя участками UAS (upstream activated sequence). После этого NtrC может связаться с сигма54-содержащей РНК полимеразой (изгибая при этом ДНК). АТФазная активность NtrC приводит к началу расплетания ДНК и формирования «открытого комплекса», необходимого для нормальной инициации транскрипции.
Две молекулы NtrC должны сначала связаться с двумя участками UAS (upstream activated sequence). После этого NtrC может связаться с сигма54-содержащей РНК полимеразой (изгибая при этом ДНК). АТФазная активность NtrC приводит к началу расплетания ДНК и формирования «открытого комплекса», необходимого для нормальной инициации транскрипции.
Слайд 13
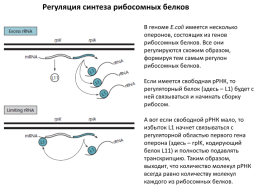
Регуляция синтеза рибосомных белков
В геноме E.coli имеется несколько оперонов, состоящих из генов рибосомных белков. Все они регулируются схожим образом, формируя тем самым регулон рибосомных белков. Если имеется свободная рРНК, то регуляторный белок (здесь – L1) будет с ней связываться и начинать сборку рибосом. А вот если свободной рРНК мало, то избыток L1 начнет связываться с регуляторной областью первого гена оперона (здесь – rplK, кодирующий белок L11) и полностью подавлять транскрипцию. Таким образом, выходит, что количество молекул рРНК всегда равно количеству молекул каждого из рибосомных белков.
В геноме E.coli имеется несколько оперонов, состоящих из генов рибосомных белков. Все они регулируются схожим образом, формируя тем самым регулон рибосомных белков. Если имеется свободная рРНК, то регуляторный белок (здесь – L1) будет с ней связываться и начинать сборку рибосом. А вот если свободной рРНК мало, то избыток L1 начнет связываться с регуляторной областью первого гена оперона (здесь – rplK, кодирующий белок L11) и полностью подавлять транскрипцию. Таким образом, выходит, что количество молекул рРНК всегда равно количеству молекул каждого из рибосомных белков.
Слайд 14
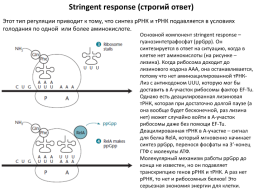
Stringent response (строгий ответ)
Этот тип регуляции приводит к тому, что синтез рРНК и тРНК подавляется в условиях голодания по одной или более аминокислоте.
Основной компонент stringent response – гуанозинтетрафосфат (ppGpp). Он синтезируется в ответ на ситуацию, когда в клетке нет аминокислоты (на рисунке – лизина). Когда рибосома доходит до лизинового кодона ААА, она останавливается, потому что нет аминоацилированной тРНК-Лиз с антикодоном UUU, которую мог бы доставить в А-участок рибосомы фактор EF-Tu. Однако есть деацилированная лизиновая тРНК, которая при достаточно долгой паузе (а она вообще будет бесконечной, раз лизина нет) может случайно войти в А-участок рибосомы даже без помощи EF-Tu. Деацилированная тРНК в А-участке – сигнал для белка RelA, который мгновенно начинает синтез ppGpp, перенося фосфаты на 3’-конец ГТФ с молекулы АТФ. Молекулярный механизм работы ppGpp до конца не известен, но он подавляет транскрипцию генов рРНК и тРНК. А раз нет рРНК, то нет и рибосомных белков! Это серьезная экономия энергии для клетки.
Этот тип регуляции приводит к тому, что синтез рРНК и тРНК подавляется в условиях голодания по одной или более аминокислоте.
Основной компонент stringent response – гуанозинтетрафосфат (ppGpp). Он синтезируется в ответ на ситуацию, когда в клетке нет аминокислоты (на рисунке – лизина). Когда рибосома доходит до лизинового кодона ААА, она останавливается, потому что нет аминоацилированной тРНК-Лиз с антикодоном UUU, которую мог бы доставить в А-участок рибосомы фактор EF-Tu. Однако есть деацилированная лизиновая тРНК, которая при достаточно долгой паузе (а она вообще будет бесконечной, раз лизина нет) может случайно войти в А-участок рибосомы даже без помощи EF-Tu. Деацилированная тРНК в А-участке – сигнал для белка RelA, который мгновенно начинает синтез ppGpp, перенося фосфаты на 3’-конец ГТФ с молекулы АТФ. Молекулярный механизм работы ppGpp до конца не известен, но он подавляет транскрипцию генов рРНК и тРНК. А раз нет рРНК, то нет и рибосомных белков! Это серьезная экономия энергии для клетки.
Слайд 15

Heat shock response (ответ на тепловой шок)
При повышении температуры бактериальная клетка начинает синтезировать целый ряд так называемых белков теплового шока – в основном это шапероны и протеазы, щепящие неправильно сложившиеся белки. Но начинается все опять с необычной сигмы!
В норме синтез такой сигмыН выключен из-за шпильки, включающей в себя SD этой мРНК. Но она расплетается само по себе при повышении температуры, это термосенсор! И уж тогда сигмаН начинает синтезироваться в больших количествах, что, в свою очередь, разрешает синтез белков теплового шока со специальных сигмаН-промоторов.
При повышении температуры бактериальная клетка начинает синтезировать целый ряд так называемых белков теплового шока – в основном это шапероны и протеазы, щепящие неправильно сложившиеся белки. Но начинается все опять с необычной сигмы!
В норме синтез такой сигмыН выключен из-за шпильки, включающей в себя SD этой мРНК. Но она расплетается само по себе при повышении температуры, это термосенсор! И уж тогда сигмаН начинает синтезироваться в больших количествах, что, в свою очередь, разрешает синтез белков теплового шока со специальных сигмаН-промоторов.
Слайд 16
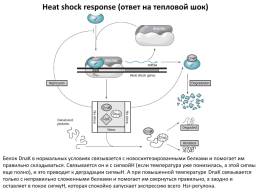
Heat shock response (ответ на тепловой шок)
Белок DnaK в нормальных условиях связывается с новосинтезированными белками и помогает им правильно складываться. Связывается он и с сигмойН (если температура уже понизилась, а этой сигмы еще полно), и это приводит к деградации сигмыН. А при повышенной температуре DnaK связывается только с неправильно сложенными белками и помогает им свернуться правильно, а заодно и оставляет в покое сигмуН, которая спокойно запускает экспрессию всего Hsr-регулона.
Белок DnaK в нормальных условиях связывается с новосинтезированными белками и помогает им правильно складываться. Связывается он и с сигмойН (если температура уже понизилась, а этой сигмы еще полно), и это приводит к деградации сигмыН. А при повышенной температуре DnaK связывается только с неправильно сложенными белками и помогает им свернуться правильно, а заодно и оставляет в покое сигмуН, которая спокойно запускает экспрессию всего Hsr-регулона.
Слайд 17
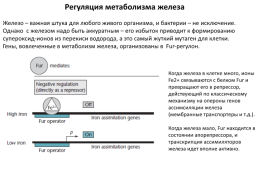
Регуляция метаболизма железа
Железо – важная штука для любого живого организма, и бактерии – не исключение. Однако с железом надо быть аккуратным – его избыток приводит к формированию супероксид-ионов из перекиси водорода, а это самый жуткий мутаген для клетки. Гены, вовлеченные в метаболизм железа, организованы в Fur-регулон.
Когда железа в клетке много, ионы Fe2+ связываются с белком Fur и превращают его в репрессор, действующий по классическому механизму на опероны генов ассимсиляции железа (мембранные транспортеры и т.д.). Когда железа мало, Fur находится в состоянии апорепрессора, и транскрипция ассимиляторов железа идет вполне активно.
Железо – важная штука для любого живого организма, и бактерии – не исключение. Однако с железом надо быть аккуратным – его избыток приводит к формированию супероксид-ионов из перекиси водорода, а это самый жуткий мутаген для клетки. Гены, вовлеченные в метаболизм железа, организованы в Fur-регулон.
Когда железа в клетке много, ионы Fe2+ связываются с белком Fur и превращают его в репрессор, действующий по классическому механизму на опероны генов ассимсиляции железа (мембранные транспортеры и т.д.). Когда железа мало, Fur находится в состоянии апорепрессора, и транскрипция ассимиляторов железа идет вполне активно.
Слайд 18
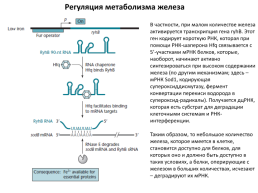
Регуляция метаболизма железа
В частности, при малом количестве железа активируется транскрипция гена ryhB. Этот ген кодирует короткую РНК, которая при помощи РНК-шаперона Hfq связывается с 5’-участками мРНК белков, которые, наоборот, начинают активно синтезироваться при высоком содержании железа (по другим механизмам; здесь – мРНК Sod1, кодирующая супероксиддисмутазу, фермент конвертации перекиси водорода в супероксид-радикалы). Получается дцРНК, которая есть субстрат для деградации клеточными системам и РНК-интерференции. Таким образом, то небольшое количество железа, которое имеется в клетке, становится доступно для белков, для которых оно и должно быть доступно в таких условиях, а белки, оперирующие с железом в больших количествах, исчезают – деградируют их мРНК.
В частности, при малом количестве железа активируется транскрипция гена ryhB. Этот ген кодирует короткую РНК, которая при помощи РНК-шаперона Hfq связывается с 5’-участками мРНК белков, которые, наоборот, начинают активно синтезироваться при высоком содержании железа (по другим механизмам; здесь – мРНК Sod1, кодирующая супероксиддисмутазу, фермент конвертации перекиси водорода в супероксид-радикалы). Получается дцРНК, которая есть субстрат для деградации клеточными системам и РНК-интерференции. Таким образом, то небольшое количество железа, которое имеется в клетке, становится доступно для белков, для которых оно и должно быть доступно в таких условиях, а белки, оперирующие с железом в больших количествах, исчезают – деградируют их мРНК.
Слайд 19
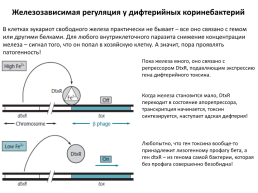
Железозависимая регуляция у дифтерийных коринебактерий
В клетках эукариот свободного железа практически не бывает – все оно связано с гемом или другими белками. Для любого внутриклеточного паразита снижение концентрации железа – сигнал того, что он попал в хозяйскую клетку. А значит, пора проявлять патогенность!
Пока железа много, оно связано с репрессором DtxR, подавляющим экспрессию гена дифтерийного токсина. Когда железа становится мало, DtxR переходит в состояние апорепрессора, транскрипция начинается, токсин синтезируется, наступает адская дифтерия! Любопытно, что ген токсина вообще-то принадлежит лизогенному профагу бета, а ген dtxR – из генома самой бактерии, которая без профага совершенно безобидна!
В клетках эукариот свободного железа практически не бывает – все оно связано с гемом или другими белками. Для любого внутриклеточного паразита снижение концентрации железа – сигнал того, что он попал в хозяйскую клетку. А значит, пора проявлять патогенность!
Пока железа много, оно связано с репрессором DtxR, подавляющим экспрессию гена дифтерийного токсина. Когда железа становится мало, DtxR переходит в состояние апорепрессора, транскрипция начинается, токсин синтезируется, наступает адская дифтерия! Любопытно, что ген токсина вообще-то принадлежит лизогенному профагу бета, а ген dtxR – из генома самой бактерии, которая без профага совершенно безобидна!
Слайд 20
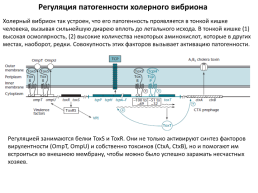
Регуляция патогенности холерного вибриона
Холерный вибрион так устроен, что его патогенность проявляется в тонкой кишке человека, вызывая сильнейшую диарею вплоть до летального исхода. В тонкой кишке (1) высокая осмолярность, (2) высокие количества некоторых аминокислот, которые в других местах, наоборот, редки. Совокупность этих факторов вызывает активацию патогенности.
Регуляцией занимаются белки ToxS и ToxR. Они не только активируют синтез факторов вирулентности (OmpT, OmpU) и собственно токсинов (CtxA, CtxB), но и помогают им встроиться во внешнюю мембрану, чтобы можно было успешно заражать несчастных хозяев.
Холерный вибрион так устроен, что его патогенность проявляется в тонкой кишке человека, вызывая сильнейшую диарею вплоть до летального исхода. В тонкой кишке (1) высокая осмолярность, (2) высокие количества некоторых аминокислот, которые в других местах, наоборот, редки. Совокупность этих факторов вызывает активацию патогенности.
Регуляцией занимаются белки ToxS и ToxR. Они не только активируют синтез факторов вирулентности (OmpT, OmpU) и собственно токсинов (CtxA, CtxB), но и помогают им встроиться во внешнюю мембрану, чтобы можно было успешно заражать несчастных хозяев.
Слайд 21
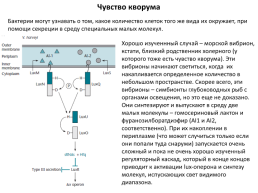
Чувство кворума
Бактерии могут узнавать о том, какое количество клеток того же вида их окружает, при помощи секреции в среду специальных малых молекул.
Хорошо изученнный случай – морской вибрион, кстати, близкий родственник холерного (у которого тоже есть чувство кворума). Эти вибрионы начинают светиться, когда их накапливается определенное количество в небольшом пространстве. Скорее всего, эти вибрионы – симбионты глубоководных рыб с органами освещения, но это еще не доказано. Они синтезируют и выпускают в среду две малых молекулы – гомосериновый лактон и фуранозилборатдиэфир (AI1 и AI2, соответственно). При их накоплении в периплазме (что может случиться только если они попали туда снаружи) запускается очень сложный и пока не очень хорошо изученный регуляторный каскад, который в конце концов приводит к активации lux-оперона и синтезу молекул, испускающих свет видимого диапазона.
Бактерии могут узнавать о том, какое количество клеток того же вида их окружает, при помощи секреции в среду специальных малых молекул.
Хорошо изученнный случай – морской вибрион, кстати, близкий родственник холерного (у которого тоже есть чувство кворума). Эти вибрионы начинают светиться, когда их накапливается определенное количество в небольшом пространстве. Скорее всего, эти вибрионы – симбионты глубоководных рыб с органами освещения, но это еще не доказано. Они синтезируют и выпускают в среду две малых молекулы – гомосериновый лактон и фуранозилборатдиэфир (AI1 и AI2, соответственно). При их накоплении в периплазме (что может случиться только если они попали туда снаружи) запускается очень сложный и пока не очень хорошо изученный регуляторный каскад, который в конце концов приводит к активации lux-оперона и синтезу молекул, испускающих свет видимого диапазона.
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
