Презентация - Химические свойства металлов
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 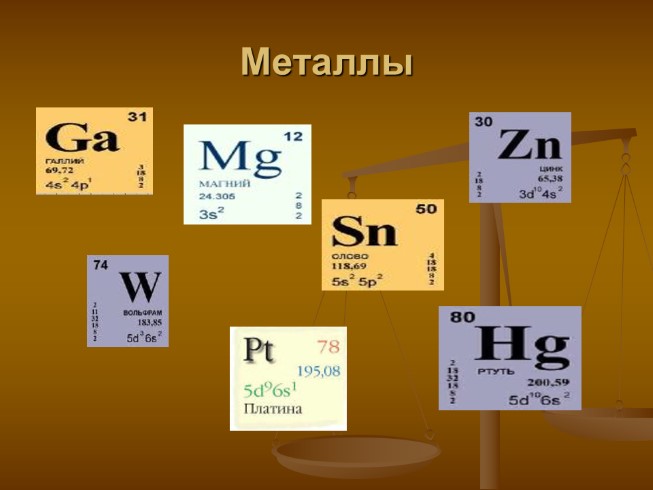
|
Распечатать
- Уникальность: 86%
- Слайдов: 20
- Просмотров: 5968
- Скачиваний: 3284
- Размер: 1.72 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Химические свойства металлов - Электрохимический ряд напряжения металлов
Химические свойства металлов - Электрохимический ряд напряжения металлов Общие химические свойства металлов
Общие химические свойства металлов Химические свойства металлов
Химические свойства металлов Химические свойства металлов 9 класс
Химические свойства металлов 9 класс Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы
Сера. Аллотропия серы. Физические и химические свойства серы. Применение серы Металлическая химическая связь
Металлическая химическая связь Общие свойства металлов
Общие свойства металлов
Слайды и текст этой онлайн презентации
Слайд 1

Металлы
Слайд 2

Вариант 1. 1. Выберите группу элементов, в которой находятся только металлы а) Al, As, P; б) Mg, Ca, Si;
в) K, Ca, Pb.
2. Атом калия имеет электронную конфигурацию а) 1s22s2;
б) 1s22s22p63s23p64s1; в) 1s22s22p4
3. Укажите общее в строении атомов Mg и Al: а) два электрона на последнем электронном слое; б) три электрона на последнем электронном слое;
в) одинаковое число электронных слоев.
4. Для всех металлов характерны:
а) металлический блеск, ковкость, пластичность б) легкоплавкость, сверхпроводимость, твердость
в) электропроводность, хрупкость, тугоплавкость
5. Тип связи в простом веществе калия: а) ионная; б) металлическая; в) ковалентная полярная
Вариант 2. 1. Выберите группу элементов, в которой находятся только металлы а) H, As, P; б) Mg, Ca, Pb;в) K, Ca, N. 2. Атом магния имеет электронную конфигурацию. а) 1s22s2; б) 1s22s22p63s2; в) 1s22s22p4 3. Укажите общее в строении атомов K и Na: а) один электрон на последнем электронном слое; б) три электрона на последнем электронном слое; в) одинаковое число электронных слоев. 4. К физическим свойствам металлов не относят а) пластичность б) электропроводность в) металлический блеск г) растворимость в воде 5. Тип связи в простом веществе магний: а) ионная; б) металлическая; в) ковалентная полярная
Вариант 2. 1. Выберите группу элементов, в которой находятся только металлы а) H, As, P; б) Mg, Ca, Pb;в) K, Ca, N. 2. Атом магния имеет электронную конфигурацию. а) 1s22s2; б) 1s22s22p63s2; в) 1s22s22p4 3. Укажите общее в строении атомов K и Na: а) один электрон на последнем электронном слое; б) три электрона на последнем электронном слое; в) одинаковое число электронных слоев. 4. К физическим свойствам металлов не относят а) пластичность б) электропроводность в) металлический блеск г) растворимость в воде 5. Тип связи в простом веществе магний: а) ионная; б) металлическая; в) ковалентная полярная
Слайд 3

Вариант 1. 1. Выберите группу элементов, в которой находятся только металлы а) Al, As, P;
б) Mg, Ca, Si; в) K, Ca, Pb.
2. Атом калия имеет электронную конфигурацию а) 1s22s2;
б) 1s22s22p63s23p64s1;
в) 1s22s22p4
3. Укажите общее в строении атомов Mg и Al: а) два электрона на последнем электронном слое; б) три электрона на последнем электронном слое; в) одинаковое число электронных слоев.
4. Для всех металлов характерны:
а) металлический блеск, ковкость, пластичность б) легкоплавкость, сверхпроводимость, твердость в) электропроводность, хрупкость, тугоплавкость
5. Тип связи в простом веществе калия: а) ионная; б) металлическая; в) ковалентная полярная
Вариант 2. 1. Выберите группу элементов, в которой находятся только металлы а) H, As, P; б) Mg, Ca, Pb; в) K, Ca, N. 2. Атом магния имеет электронную конфигурацию. а) 1s22s2; б) 1s22s22p63s2; в) 1s22s22p4 3. Укажите общее в строении атомов K и Na: а) один электрон на последнем электронном слое; б) три электрона на последнем электронном слое; в) одинаковое число электронных слоев. 4. К физическим свойствам металлов не относят а) пластичность б) электропроводность в) металлический блеск г) растворимость в воде 5. Тип связи в простом веществе магний: а) ионная; б) металлическая; в) ковалентная полярная
Вариант 2. 1. Выберите группу элементов, в которой находятся только металлы а) H, As, P; б) Mg, Ca, Pb; в) K, Ca, N. 2. Атом магния имеет электронную конфигурацию. а) 1s22s2; б) 1s22s22p63s2; в) 1s22s22p4 3. Укажите общее в строении атомов K и Na: а) один электрон на последнем электронном слое; б) три электрона на последнем электронном слое; в) одинаковое число электронных слоев. 4. К физическим свойствам металлов не относят а) пластичность б) электропроводность в) металлический блеск г) растворимость в воде 5. Тип связи в простом веществе магний: а) ионная; б) металлическая; в) ковалентная полярная
Слайд 4

Химические свойства металлов
Слайд 5

Взаимодействие с неметаллами
Na + Cl2 =
Mg + O2 =
Al + S =
Са + O2 =
Na + Cl2 =
Mg + O2 =
Al + S =
Са + O2 =
Слайд 6

Взаимодействие с неметаллами
2Na + Cl2 = 2NaCl 2Са + O2 = 2СаO
2Mg + O2 = 2MgO 2Al + 3S = Al2S3
2Na + Cl2 = 2NaCl 2Са + O2 = 2СаO
2Mg + O2 = 2MgO 2Al + 3S = Al2S3
Слайд 7

Взаимодействие со сложными веществами:
с водой
Li K Ca Na Mg Al Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au
При обычных условиях M + H2O → H2 + основание При нагревании M+H2O→H2+оксид M + H2O ≠
с водой
Li K Ca Na Mg Al Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au
При обычных условиях M + H2O → H2 + основание При нагревании M+H2O→H2+оксид M + H2O ≠
Слайд 8
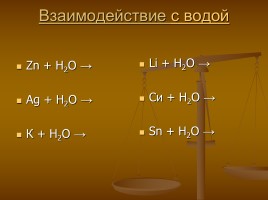
Взаимодействие с водой
Zn + H2O → Ag + H2O → К + H2O →
Li + H2O → Си + H2O → Sn + H2O →
Zn + H2O → Ag + H2O → К + H2O →
Li + H2O → Си + H2O → Sn + H2O →
Слайд 9
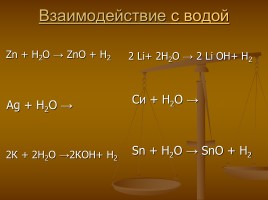
Взаимодействие с водой
Zn + H2O → ZnO + H2 Ag + H2O → 2К + 2H2O →2КOH+ H2
2 Li+ 2H2O → 2 Li OH+ H2 Си + H2O → Sn + H2O → SnO + H2
Zn + H2O → ZnO + H2 Ag + H2O → 2К + 2H2O →2КOH+ H2
2 Li+ 2H2O → 2 Li OH+ H2 Си + H2O → Sn + H2O → SnO + H2
Слайд 10

Взаимодействие растворами кислот
Li K Ca Na Mg Al |Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au Li K Ca Na Mg Al |Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au
Вытесняют H2↑ из растворов кислот Не вытесняют H2↑ из растворов кислот
Li K Ca Na Mg Al |Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au Li K Ca Na Mg Al |Zn Cr Fe Ni Pb (H2) Cu Hg Ag Pt Au
Вытесняют H2↑ из растворов кислот Не вытесняют H2↑ из растворов кислот
Слайд 11

Взаимодействие растворами кислот
Zn + H2SO4 (р-р) Au+ HCl →
Cu + H2SO4 (р-р)
Ni
+ HCl
→
→
→
Zn + H2SO4 (р-р) Au+ HCl →
Cu + H2SO4 (р-р)
Ni
+ HCl
→
→
→
Слайд 12

Взаимодействие растворами кислот
Zn + H2SO4 (р-р) → ZnSO4 +H2 Au+ HCl →
Cu + H2SO4 (р-р) →
Ni
+ 2HCl
→
Ni
Cl
+H2
2
Zn + H2SO4 (р-р) → ZnSO4 +H2 Au+ HCl →
Cu + H2SO4 (р-р) →
Ni
+ 2HCl
→
Ni
Cl
+H2
2
Слайд 13

Взаимодействие с растворами солей
Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее.
Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее.
Слайд 14

Взаимодействие с растворами солей
Ag + Pb Cl2 → Zn + FeCl3 →
Fe + AgNO3 →
Pb(NO3)2
Cu
+
→
Ag + Pb Cl2 → Zn + FeCl3 →
Fe + AgNO3 →
Pb(NO3)2
Cu
+
→
Слайд 15

Взаимодействие с растворами солей
Ag + Pb Cl2 → 3Zn + 2FeCl3 → 3ZnCl2+ 2Fe
Cu → Fe + 2 AgNO3 → Fe(NO3)2+2Ag
+
Pb(NO3)2
Ag + Pb Cl2 → 3Zn + 2FeCl3 → 3ZnCl2+ 2Fe
Cu → Fe + 2 AgNO3 → Fe(NO3)2+2Ag
+
Pb(NO3)2
Слайд 16
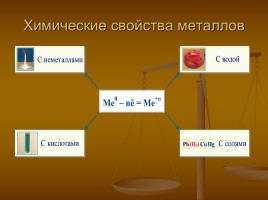
Химические свойства металлов
Слайд 17

Химические свойства металлов
Al + HCl Zn + CuCl2 Ва + H2O Na + N2
Ca + P Cа + H2O Al + CuCl2 Fe + H2SO4( раствор)
Al + HCl Zn + CuCl2 Ва + H2O Na + N2
Ca + P Cа + H2O Al + CuCl2 Fe + H2SO4( раствор)
Слайд 18

Химические свойства металлов
2Al + 6HCl = 2AlCl3+3H2 Zn + CuCl2 = ZnCl2 + Cu Ва + 2H2O = Ва(OH) 2+ H2 6Na + N2 = 2Na3N
3Ca + 2P = Ca3 P2 Cа + 2H2O = Са(OH) 2+ H2 2Al + 3CuCl2 = 3Cu+ 2Al Cl3 Fe + H2SO4( раствор) = Fe SO4 +H2
2Al + 6HCl = 2AlCl3+3H2 Zn + CuCl2 = ZnCl2 + Cu Ва + 2H2O = Ва(OH) 2+ H2 6Na + N2 = 2Na3N
3Ca + 2P = Ca3 P2 Cа + 2H2O = Са(OH) 2+ H2 2Al + 3CuCl2 = 3Cu+ 2Al Cl3 Fe + H2SO4( раствор) = Fe SO4 +H2
Слайд 19
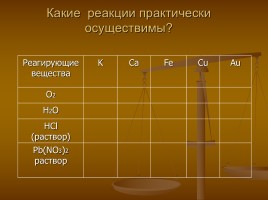
Какие реакции практически осуществимы?
Реагирующие вещества K Ca Fe Cu Au
О2
Н2О
HCl (раствор)
Pb(NO3)2 раствор
Реагирующие вещества K Ca Fe Cu Au
О2
Н2О
HCl (раствор)
Pb(NO3)2 раствор
Слайд 20
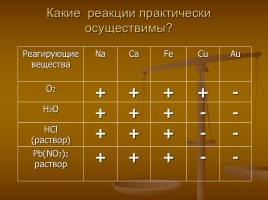
Какие реакции практически осуществимы?
Реагирующие вещества Na Ca Fe Cu Au
О2 + + + + -
Н2О + + + - -
HCl (раствор) + + + - -
Pb(NO3)2 раствор + + + - -
Реагирующие вещества Na Ca Fe Cu Au
О2 + + + + -
Н2О + + + - -
HCl (раствор) + + + - -
Pb(NO3)2 раствор + + + - -
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
