Слайды и текст этой онлайн презентации
Слайд 1
Тема урока: «Серная кислота как электролит».
Цель урока: изучить свойства серной кислоты разной концентрации.
Слайд 2
ошибка
ошибка
подумай
верно
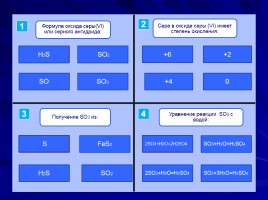
SO2
SO
H2S
SO3
верно
подумай
ошибка
ошибка
+6
+4
+2
0
ошибка
ошибка
подумай
верно
H2S
FeS2
S
SO2
подумай
ошибка
ошибка
верно
2SO3+H2O=2H2SO4
SO3+H2O=H2SO4
2SO3+H2O=H2SO4
SO3+3H2O=H2SO4
1
2
4
3
Слайд 3
Разбавление серной кислоты водой.
034.wmv
Слайд 4
Физические свойства серной кислоты
Образование гидратов, при взаимодействии серной кислоты с водой:
H2SO4 + nH2O = H2SO4 * nH2O +Q
Серная кислота — бесцветная маслянистая жидкость, почти вдвое (=1,83 г/см3) тяжелее воды, не имеет запаха. Гигроскопична. Поглощает влагу с выделением большого количества теплоты.
Слайд 5
Химические свойства серной кислоты.
Свойства
H2SO4 разб. H2SO4 конц
1. Индикатор: (5 группа)
а) лакмус
б) метиловый оранжевый
2. С металлами, стоящими в
электрохимическом ряду напряжений до и после Н2 (1 группа)
3. С основными оксидами (2 группа)
4. С основаниями (3 группа)
5. С солями. Качественная реакция на SO42-
(4 группа)
6. С неметаллами (5 группа)
красный
розовый
не изменяет окраску индикатора.
Слайд 6
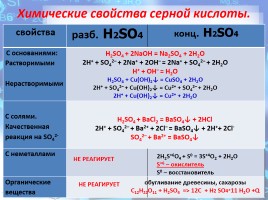
Химические свойства серной кислоты.
свойства разб. H2SO4 конц. H2SO4
С металлами, стоящими в электрохимическом ряду напряжений до Н2
после Н2
С основными оксидами
H2+SO4 +Zn0 =Zn+2SO4 +H2↑ H+ – окислитель Zn0 – восстановитель
НЕ РЕАГИРУЕТ с металлами после водорода.
4H2S+6O4+3Zn0 =3Zn+2SO4+S0↓+4H2O S+6 – окислитель Zn0 – восстановитель 5H2SO4 + 4Ca=4CaSO4 + H2S↑+ 4H2O На холоде пассивирует Fe,Cr,Ni,Al.
2H2S+6O4+Cu0 =Cu+2SO4 + S+4O2 +2H2O S+6 – окислитель Cu0 – восстановитель
Не реагирует с Au и Pt
H2SO4 + MgO = MgSO4 + H2O MgO + 2H+ + SO42– → Mg2+ + SO42– + H2O MgO + 2H+ → Mg2+ + H2O
Слайд 7
Химические свойства концентрированной серной кислоты.
mmlab.chemistry.404i.oms
Слайд 8
Химические свойства серной кислоты.
свойства разб. H2SO4 конц. H2SO4
С основаниями:
Растворимыми
Нерастворимыми
С солями. Качественная реакция на SO42-
С неметаллами
Органические вещества
H2SO4 + 2NaOH = Na2SO4 + 2H2O 2H+ + SO42– + 2Na+ + 2OH– = 2Na+ + SO42– + 2H2O H+ + OH– = H2O
H2SO4 + Cu(OH)2↓ = CuSO4 + 2H2O 2H+ + SO42– + Cu(OH)2↓ = Cu2+ + SO42– + 2H2O 2H+ + Cu(OH)2↓ = Cu2+ + 2H2O
H2SO4 + BaCl2 = BaSO4↓ + 2HCl 2H+ + SO42– + Ba2+ + 2Cl– = BaSO4↓ + 2H++ 2Cl- SO42– + Ba2+ = BaSO4↓
НЕ РЕАГИРУЕТ
2H2S+6O4 + S0 = 3S+4O2 + 2H2O S+6 – окислитель S0 – восстановитель
НЕ РЕАГИРУЕТ
обугливание древесины, сахарозы
C12H22O11 + H2SO4 => 12C + H2 SO4*11 H2O +Q
Слайд 9
Химические свойства концентрированной серной кислоты.
mmlab.chemistry.404i.oms
Слайд 10
Химические свойства концентрированной серной кислоты.
032.wmv
Слайд 11
ВЫВОД:
H2SO4 - сильный окислитель.
Свойства разбавленной и концентрированной серной кислоты отличаются, так как разные окислители:
в разбавленной окислителем является ион H+
в концентрированной S+6 .
Слайд 12
ошибка
ошибка
подумай
верно
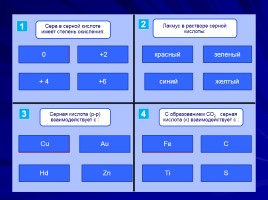
+2
+ 4
0
+6
верно
подумай
ошибка
ошибка
красный
синий
зеленый
желтый
ошибка
ошибка
подумай
верно
Hd
Au
Cu
Zn
подумай
ошибка
ошибка
верно
Fe
С
Ti
S
1
2
4
3
Слайд 13
Домашнее задание.
§20, стр. 98-104.
Упражнение № 1-2, стр. 105 – на «3». Упражнение № 4, стр. 105 – на «4». Упражнение № 5, стр. 105 – на «5».
Творческое задание №7, стр. 108 (по желанию).
Желаю успеха!
Слайд 14
ПРОВЕРЬ СЕБЯ:
В двух одинаковых сосудах без этикеток налиты равные объемы разбавленной и концентрированной серной кислоты. Предложите простейший способ идентификации (определения) жидкостей.
2. В не очень далекие времена иногда между стеклами в двойных оконных рамах на зиму ставили стаканчик с концентрированной серной кислотой, чтобы стекла не потели. Какова роль серной кислоты?
3. С какими из перечисленных металлов при температуре 200С не реагирует концентрированная серная кислота:
1) Cu, 2) Zn, 3) Mg, 4) Au.
4.С образованием СО2 концентрированная серная кислота взаимодействует с:
1) Fe 2) Ti 3) C 4) S
Слайд 15
Спасибо
за внимание!
 Сущность электролиза как способа получения веществ
Сущность электролиза как способа получения веществ Новейшая история как историческая эпоха - Мир в начале ХХ в. - Политическое развитие в начале ХХ в.
Новейшая история как историческая эпоха - Мир в начале ХХ в. - Политическое развитие в начале ХХ в. Школа как производитель - Школа купила компьютер
Школа как производитель - Школа купила компьютер Урок-путешествие «Кислоты»
Урок-путешествие «Кислоты» Как животные воспринимают мир для 2 класса
Как животные воспринимают мир для 2 класса Наследственное право как отрасль права
Наследственное право как отрасль права Как называются эти предметы?
Как называются эти предметы?