Презентация - Физиология дыхания для анестезиологов
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 93%
- Слайдов: 73
- Просмотров: 4808
- Скачиваний: 2172
- Размер: 10.73 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Физиология дыхания
Физиология дыхания Анатомия и физиология с позиции анестезиологии и реаниматологии
Анатомия и физиология с позиции анестезиологии и реаниматологии Учимся мыслить логически (для детей 5-7 лет)
Учимся мыслить логически (для детей 5-7 лет) Электронная физкультминутка для глаз
Электронная физкультминутка для глаз Рекомендации для родителей «Игры с куклой и использование разнообразного дидактического материала»
Рекомендации для родителей «Игры с куклой и использование разнообразного дидактического материала» От героев былых времен (для совместного исполнения всем классом)
От героев былых времен (для совместного исполнения всем классом) Сборник дидактических игр для устного счёта 1 класс (сложение и вычитание в пределах первого десятка)
Сборник дидактических игр для устного счёта 1 класс (сложение и вычитание в пределах первого десятка)
Слайды и текст этой онлайн презентации
Слайд 1
Физиология дыхания
для анестезиологов
Слайд 2

Дыхание – это процесс газообмена между организмом и окружающей средой, сопровождающийся поглощением кислорода и выделением углекислого газа. Дыхательная система выполняет эту важнейшую функцию (газообмен), без которой невозможна жизнь.
Слайд 3

Дыхание протекает в несколько стадий:
1) внешнее дыхание – обмен кислорода (О2) и углекислого газа (СО2) между внешней средой и кровью легочных капилляров. В свою очередь внешнее дыхание можно разделить на два процесса: а) газообмен между внешней средой и альвеолами легких, что обозначается как «легочная вентиляция»; б) газообмен между альвеолярным воздухом и кровью легочных капилляров; 2) транспорт О2 и СО2 кровью; 3) обмен О2 и СО2 между кровью и клетками организма; 4) тканевое дыхание. Дыхательная система состоит из воздухоносных путей и собственно дыхательных (респираторных) отделов. Полость носа, носовая часть глотки, гортань, трахея, бронхи различных калибров, включая бронхиолы, являются воздухоносными путями. В них воздух согревается, очищается от различных частиц и увлажняется. Альвеолярные ходы и альвеолы являются собственно дыхательными (респираторными) отделами, в которых и происходит газообмен.
Слайд 4
Слайд 5
Слайд 6
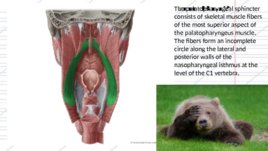
The palatopharyngeal sphincter consists of skeletal muscle fibers of the most superior aspect of the palatopharyngeus muscle. The fibers form an incomplete circle along the lateral and posterior walls of the nasopharyngeal isthmus at the level of the C1 vertebra.
Слайд 7
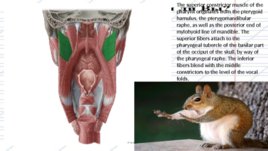
The superior constrictor muscle of the pharynx originates from the pterygoid hamulus, the pterygomandibular raphe, as well as the posterior end of mylohyoid line of mandible. The superior fibers attach to the pharyngeal tubercle of the basilar part of the occiput of the skull, by way of the pharyngeal raphe. The inferior fibers blend with the middle constrictors to the level of the vocal folds.
Слайд 8
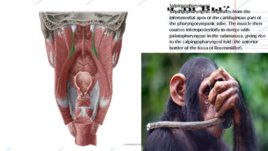
Salpingopharyngeus Salpingopharyngeus originates from the inferomedial apex of the cartilaginous part of the pharyngotympanic tube. The muscle then courses inferoposteriorly to merge with palatopharyngeus in the submucosa, giving rise to the salpingopharyngeal fold (the anterior border of the fossa of Rosenmüller).
Слайд 9
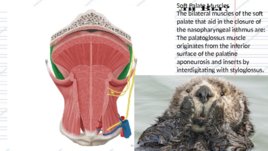
Soft Palate Muscles The bilateral muscles of the soft palate that aid in the closure of the nasopharyngeal isthmus are: The palatoglossus muscle originates from the inferior surface of the palatine aponeurosis and inserts by interdigitating with styloglossus.
Слайд 10
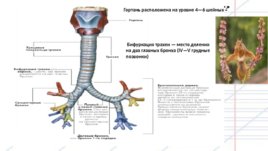
Гортань расположена на уровне 4—6 шейных Бифуркация трахеи — место деления на два главных бронха (IV—V грудные позвонки)
Слайд 11
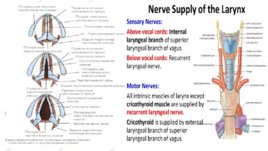
Слайд 12
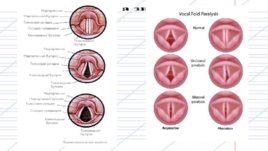
Слайд 13

Объём крови лёгочных капилляров составляет 80-150 мл при толщине её слоя в них всего 5-8 мкм. Газообмен осуществляется на уровне аэрогематического барьера, на границе раздела фаз воздуха и крови. Процесс этот со вдохом усиливается благодаря уменьшению с нарастающим вдохом толщины аэрогематического барьера. Толщина альвеолярнокапиллярной мембраны составляет 0,5 мкм. Средний диаметр лёгочных капилляров (7 мкм) почти равен диаметру эритроцита. При прохождении по капиллярам лёгких эритроциты плотно прилегают к альвеолярнокапиллярной мембране и путь диффузии в самом эритроците оказывается длиннее пути через мембрану. Из 5 л крови, протекающих через лёгкие за 1 мин, в лёгочных капиллярах одномоментно находятся и участвует в газообмене только 70-100 мл. Этот объём крови образует на альвеолокапиллярной мембране пленку площадью 50-100 м2 и толщиной в один эритроцит. Для обеспечения полноценного газообмена каждый капилляр контактирует не с одной, а с несколькими альвеолами. Ёмкость капилляров лёгких относительно постоянна, но общий внутрилёгочный объём крови может изменяться от 500 до 1000 мл. Таким образом, лёгкие играют роль резервуара для системного кровообращения.
Слайд 14

Для создания потока газа необходим градиент давлений. При спонтанном дыхании Вдыхаемый воздух перемещается в дыхательные пути за счет создания субатмосферного давления в альвеолах (порядка –5 см H2O в состоянии покоя), при этом происходит увеличение емкости грудной полости за счет сокращения мышц вдоха. Во время выдоха давление в альвеолах слегка превосходит атмосферное и газоток устремляется в сторону внешней среды. Механизм дыхания
Слайд 15
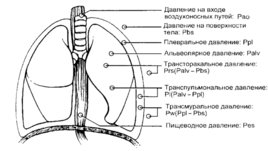
Слайд 16

Процесс дыхания
Дыхательный объем (500 мл), умноженный на частоту дыханий в минуту (14 дыханий в минуту), дает минутный объем дыхания (7000 мл/мин): VE f х VT, «анатомическое мертвое пространство» (VD) - это дыхательный объем , который не участвует в газообмене, то есть до дыхательных бронхиол (17-й порядок ветвления бронхиального дерева). Его объем составляет приблизительно 2 мл/кг, что составляет для взрослого около 150 мл, то есть примерно одну треть дыхательного объема. Оставшаяся часть дыхательного объема, реально участвующая в газообмене, умноженная на частоту дыхания, позволяет рассчитать объем альвеолярной вентиляции (VA, приблизительно 5000 мл/мин). Функциональная остаточная емкость легких (ФОЕ) представляет собой тот объем воздуха, который остается в легких после спокойного выдоха.
Слайд 17

Функциональная остаточная емкость снижается в положении на спине, при ожирении, беременности, анестезии, но не меняется с возрастом. Для анестезиологов показатель ФОЕ представляет особый интерес: во время апноэ ФОЕ является «резервуаром», в котором запасен кислород, поступающий в кровь; при снижении ФОЕ изменяется распределение газа в легких, что сопровождается нарушением соотношения вентиляции и легочной перфузии; если ФОЕ снижается ниже определенного значения («емкость закрытия»), возникает спадение (закрытие) дыхательных путей, что ведет к шунтированию.
Слайд 18

Слайд 19
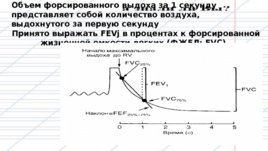
Объем форсированного выдоха за 1 секунду представляет собой количество воздуха, выдохнутого за первую секунду
Принято выражать FEVj в процентах к форсированной жизненной емкости легких (ФЖЕЛ; FVC).
Слайд 20

Типичные спирограммы. (А) Здоровый человек. (Б) Больной обструктивной болезнью ВП. (В) Больной рестриктивной болезнью легких. FEV,/FVC % понижено при обструкции и сохранено при рестрикции При обструктивных расстройствах ведущем патофизиологической аномалией является увеличенное сопротивление ВП , легочная паренхима нормальна, посужены ВП. Следовательно, FVC может быть сохранена, но воздушный поток снизится и FEVi/FVC % уменьшится. Как видно из рис. наклон спирограммы выдоха заметно снижен по сравнению с нормой и FEV,/FVC % уменьшено. Рестриктивные расстройства характеризуются ограничением наполнения грудной клетки воздухом: легочная паренхима изменена таким образом, что легкие становятся жесткими и с трудом расправляются Функция ВП обычно остается нормальной и, следовательно, скорость воздушного потока не претерпевает изменений. Хотя FVC и FEVi снижаются, отношение FEVi/FVC% остается нормальным
Слайд 21

Слайд 22

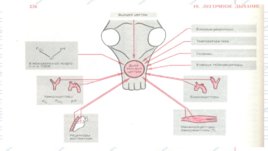
область центральной регуляции, афферентный путь, эфферентный путь. Системы физиологической нейрогенной регуляции
обычно принято разделять на следующие три составляющие:
Область центральной регуляции дыхания, известная как дыхательный центр, расположена в нижней части ствола мозга — в продолговатом мозге (medulla oblongata). Это образование включает «инспираторные нейроны», которые активны только во время вдоха, и «экспираторные нейроны», активирующиеся только в фазу выдоха. афферентные пути Центральные хеморецепторы Хеморецепторы — это клетки, способные реагиро- вать на химические стимулы. Они располагаются на дне четвертого желудочка (в стволе мозга) и, реагируя на кислотность спинномозговой жидкости Периферические хеморецепторы Каротидные и аортальные Эфферентные пути Эфферентные нервные волокна, исходящие из дыхательного центра, идут в составе спинного мозга к диафрагме, межреберным мышцам и вспомогательным дыхательным мышцам шеи. Диафрагма иннервируется диафрагмальным нервом, который образуется на шее при слиянии ветвей спинальных нервов от сегментов C3–C5. Межреберные мышцы иннервируются сегментарными межреберными нервами, покидающими спинной мозг на уровне от T1 до T12. Иннервация вспомогательных мышц шеи обеспечивается нервами шейного сплетения.
Слайд 23

Дыхательный центр Дыхательный центр - совокупность нейронных ансамблей разных этажей центральной нервной системы, обеспечивающих управление внешним дыханием Автоматический дыхательный центр - совокупность нейронов специфических (дыхательных) ядер продолговатого мозга, способных генерировать дыхательный ритм Функции дыхательного центра: - моторная или двигательная - гомеостатическая
Слайд 24
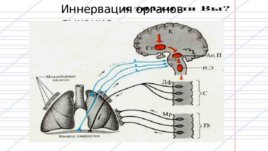
Иннервация органов дыхания
Слайд 25

Основной дыхательный центр располагается на дне четвертого желудочка и состоит из двух групп нейронов: инспираторных (дорсальная) и экспираторных (вентральная). Нейроны вдоха генерируют импульс автоматически, а экспираторные вовлекаются в процесс только при форсированном выдохе. К важным центральным образованиям относят еще два центра: апнойный (усиливает вдох) и пневмотаксический центр (греч. pneumon — легкое, taxis — строй, порядок.), прерывающий вдох путем подавления дорсальной группы нейронов.
Слайд 26
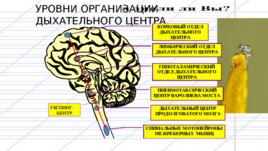
УРОВНИ ОРГАНИЗАЦИИ ДЫХАТЕЛЬНОГО ЦЕНТРА ГАСПИНГ- ЦЕНТР
Слайд 27

Дыхательный центр Бульбарный отдел – главное представительство. Обеспечивает автоматическую саморегуляцию дыхания. Включает инспираторный (ранние и поздние нейроны) и экспираторный отделы Спинальный уровень – включает мотонейроны передних рогов, иннервирующие дыхательные мышцы (3-5 шейные сегменты-диафрагму; 1-6 грудные сегменты-межреберные мышцы) Область моста- пневмотаксический центр- регулирует продолжительность вдоха и выдоха (ритм дыхания) Средний мост, мозжечок – регуляция тонуса дыхательных мышц Гипоталамус –интеграция дыхания с другими функциями и внешней средой Кора больших полушарий – произвольная и условно-рефлекторная регуляция дыхания
Слайд 28
Слайд 29

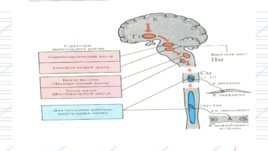
Хеморецепторы, регулирующие процесс дыхания, располагаются как на периферии, так и центрально. В норме регуляция осуществляется центральными рецепторами продолговатого мозга, чувствительными к концентрации ионов водорода в ликворе. концентрация H (p H) будет определяться парциальным давлением CO2, который свободно проникает через гематоэнцефалический барьер из артериальной крови (в интерстициальную жидкость ткани мозга существуют периферические хеморецепторы, которые располагаются в каротидном синусе и аортальных тельцах. Большая часть этих периферических образований чувствительна к снижению парциального давления O2 крови, но некоторые также реагируют на рост Pa CO2. Ответ этих рецепторов возникает лишь при тяжелой гипоксемии — снижении Pa O2 60 мм рт. ст. (8 к Па), например, при дыхании окружающим воздухом на большой высоте
Слайд 30
Слайд 31

У здоровых людей поступление в каротидные тельца крови с PO2 менее 80 мм рт. ст. (10,6 к Па) или PCO2 более 40 мм рт. ст. (5,3 к Па) вызывает немедленное и выраженное усиление вентиляции. каротидные тельца расположены в месте бифуркации общей сонной артерии на наружную и внутреннюю ветви в области шеи. Аортальные тельца расположены в дуге аорты. Информация от каротидных телец поступает в дыхательный центр по волокнам, входящим в состав языкоглоточного нерва (IX пара черепно-мозговых нервов), а от аортальных телец — по блуждающему нерву (X пара).
Слайд 32

Существует ответ на растяжение (наполнение легких): растяжение легких и грудной клетки ведет к завершению вдоха. Эта реакция обеспечивает безопасность и предупреждает избыточную нагрузку на органы дыхания. Напротив, при низком объеме легких действует противоположный рефлекс. Небольшое растяжение объема легких может стимулировать рецепторы растяжения с усилением и продолжением вдоха. Этот эффект иногда может наблюдаться в условиях анестезии у больных, которым введены опиоиды. Спонтанное дыхание у них отсутствует или частота его резко снижена, но при создании анестезиологом небольшого положительного давления в дыхательных путях (вспомогательный вдох) происходит стимуляция дыхания и пациент как бы «подхватывает» его, совершая глубокий вдох. Рецепторы, залегающие в стенке бронхов, отвечают на раздражающие вещества и вызывают кашель, задержку дыхания и чиханье. В эластических тканях легких и грудной клетки расположены рецепторы, реагирующие на растяжение. В стенке сосудов легочного русла также существуют рецепторы растяжения. При их стимуляции (усиление кровенаполнения, например, при сердечной недостаточности) развивается рефлекторная гипервентиляция. Информация от этих рецепторов передается в дыхательный центр по ветвям блуждающего нерва.
Слайд 33
Слайд 34

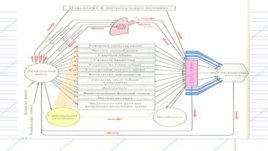
Сопротивление дыхательных путей характеризует препятствие потоку воздуха проводящими дыхательными путями. Наибольшая часть сопротивления создается дыхательными путями большого калибра (до 6–7-го порядка) и вкладом тканевого сопротивления Повышение сопротивления вследствие сужения дыхательных путей, например, при бронхоспазме, приводит к развитию обструктивных заболеваний легких. во время выдоха ближайшие к альвеолам дыхательные пути могут спадаться, что усугубляет обструкцию, не позволяет увеличить скорость экспираторного потока и служит причиной возникновения динамической гиперинфляции («воздушная ловушка») в дистальных дыхательных путях. Комплайнс (англ. compliance, C — податливость) характеризует растяжимость (способность к удлинению). В итоговое значение этого показателя вносит вклад как податливость ткани легких, так и грудной клетки, поэтому податливость измеряется как соотношение единицы объема к единице давления (V/P) — обычно в мл / см вод. ст.
Слайд 35

гистерезис При дыхании с высокой частотой требуется более высокая скорость потока, что повышает силы трения. Это явление проявляется на фоне хронических обструктивных заболеваний, когда пациенты стараются минимизировать работу дыхания за счет более редкого (медленного) дыхания при более высоком дыхательном объеме. Пациенты с рестриктивными поражениями легких (снижен комплайнс) по мере нарастания дыхательного объема быстро достигают неблагоприятной верхней части кривой комплайнса, при этом, уменьшая работу дыхания, они стремятся к быстрому и поверхностному дыханию.
Слайд 36

Если поверхность жидкости сферическая, то она в соответствии с законом Лапласа будет создавать определенное давление: P 2 х T / r, где Р — давление, T — поверхностное натяжение, r — радиус сферы. В случае с двумя свободными поверхностями жидкости (пузырь) это уравнение выглядит как P 4 Ч T / r. (В альвеолах лишь одна — внутренняя поверхность жидкости создает натяжение) Сурфактант сложное многокомпонентное вещество, вырабатываемое эпителиальными альвеолоцитами 2-го типа, и позволяет значительно снизить поверхностное натяжение пленки жидкости дыхательной поверхности альвеол, состоящий в основном из фосфолипидов (дипальмитоил лецитин), оказывает следующие важные эффекты : снижает утечки жидкости из легочных капилляров в альвеолы, поскольку силы поверхностного натяжения увеличивают градиент гидростатических давлений на разделе капилляров и альвеол; повышает (улучшает) суммарный легочной комплайнс; снижает склонность альвеол меньшего размера к опустошению путем передачи газа более крупным «соседям» и, таким образом, уменьшает риск коллабирования легочной ткани.
Слайд 37
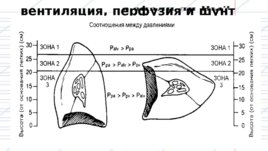
вентиляция, перфузия и шунт
Слайд 38

Распределение перфузии в легких главным образом определяется силой тяжести. Это значит, что в положении стоя перфузионное давление в базальных отделах легких будет равно сумме среднего давления в легочной артерии (15 мм рт. ст., или 20 см H2O) и гидростатического давления столба жидкости, высота которого определяется дистанцией от уровня легочного ствола до основания легкого (примерно 15 см H2O).
Слайд 39
Слайд 40

Слайд 41

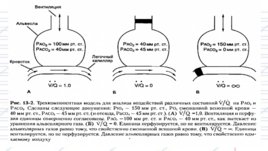
Нарушения соотношения V/Q очень часто возникают во время анестезии. Это обусловлено снижением ФОЕ, что в свою очередь изменяет положение легких относительно кривой комплайнса. Верхушки, таким образом, перемещаются в более благоприятные условия, в то время как базальные отделы занимают менее выгодную позицию в нижней части кривой. При полном прекращении альвеолярного кровотока в какой-либо зоне будет наблюдаться экстремальное нарушение V/Q, при этом соотношение V/Q будет стремиться к бесконечности ( ). Эта зона обозначается как альвеолярное мертвое пространство, которое вместе с анатомическим мертвым пространством составляет физиологическое мертвое пространство. в случае с шунтированием улучшить оксигенацию можно лишь путем восстановления вентиляции легких при помощи приемов респираторной физиотерапии, таких как санация дыхательных путей, рекрутмент легких, создание ПДКВ или неинвазивная вентиляция на фоне непрерывного положительного давления в дыхательных путях
Слайд 42

Существует физиологический механизм, уменьшающий выраженность гипоксемии вследствие низкого соотношения V/Q путем развития местной вазоконстрикции в зонах, получающих недостаточную вентиляцию, с перераспределением крови к прочим областям, вентиляция которых лучше. Этот феномен, известный под названием «гипоксическая легочная вазоконстрикция» Вместе с тем эффективность защитного эффекта ГЛВ может подавляться рядом препаратов, и в частности ингаляционными анестетиками.
Слайд 43

может участвовать ряд факторов, таких как: изменение давления наполнения левого сердца, сердечный выброс, частота сердечных сокращений, гематокрит и объем крови в легких. Однако наиболее важным патофизиологическим фактором является повышение легочного сосудистого сопротивления, локализованное, главным образом, в прекапиллярных артериях и артериолах. Развитие легочной гипертензии В отличие от гипоксемии, гиперкапния, по-видимому, способствует легочной гипертензии, вызывая ацидемию, а не прямую вазоконстрикцию. Задержка двуокиси углерода может быть самоподдерживающейся; гиперкапния снижает чувствительность дыхательного центра к С02 и способствует задержке бикарбоната почками Значительная ацидемия (р Н крови 7.2) вызывает легочную вазоконстрикцию. У человека ацидемия действует синергически с гипоксией. Значительная алкалемия (р Н крови 7.5) уменьшает сужение сосудов в ответ на гипоксию.
Слайд 44

Слайд 45
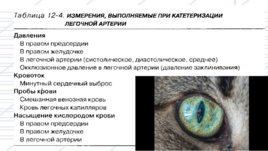
Слайд 46

недыхательные функции легких
Хотя главная функция легких состоит в обеспечении газообмена, они участвуют в ряде физиологических процессов, среди которых наиболее важными являются следующие: создание резервуара (депо) крови, которая при необходимости может поступать в системный кровоток, фильтрация микросгустков, активация ангиотензина-II за счет расщепления ангиотензина-I ангиотензинпревращающим ферментом (АПФ), инактивация ряда эндогенных веществ, таких как норадреналин и брадикинин, участие в иммунном ответе путем секреции с мокротой Ig A.
Слайд 47
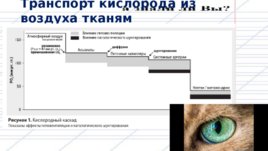
Транспорт кислорода из воздуха тканям
Слайд 48

из альвеол в кровь
Кровь, возвращающаяся к сердцу из тканей, имеет низкое РО2 (32 мм рт. ст., 4,3 к Па) и поступает к легким по легочным артериям. Легочные артерии ветвятся с образованием легочных капилляров, окружающих альвеолы. Кислород диффундирует из альвеол — зоны высокого РО2 (100 мм рт. ст., 13 к Па) в капилляры — зону низкого РО2 (32 мм рт. ст., 4,3 к Па). После оксигенации кровь поступает по легочным венам в левые отделы сердца и далее в ткани организма. В модели «идеального легкого» РО2 в крови легочных вен могло бы равняться РО2 в альвеолах (PAO2). Однако два ключевых фактора делают это невозможным и объясняют возникновение альвеолярно-артериального интервала (разности). Во-первых, свой вклад вносит несовершенство вентиляционно-перфузионных (V/Q) отношений (увеличение мертвого пространства или шунт), а во-вторых — ограниченная скорость диффузии через альвеолокапиллярную мембрану. Диффузия Кислород диффундирует из альвеол в капилляры до момента выравнивания РО2 в капиллярах (Pc O2) и PAO2. Этот процесс протекает быстро, занимая около 0,25 секунды, и в норме завершается, когда кровь проходит одну треть пути по легочному капилляру. Общее время прохождения крови по газообменному участку капилляра составляет 0,75 секунды. В интактных легких, даже если сердечный выброс и альвеолярный кровоток оказываются повышенными (нагрузка), время контакта крови с альвеолой достаточно для выравнивания парциальных давлений O2
Слайд 49

Каждый грамм гемоглобина при полном насыщении способен переносить 1,34 мл кислорода. Таким образом, каждый литр крови с концентрацией гемоглобина 150 г/л и при полном насыщении O2 (при Рa О2 100 мм рт. ст., или 13 к Па) может переносить около 200 мл кислорода. При этом Рa О2 (100 мм рт. ст.) в каждом литре плазмы будет растворено всего 3 мл кислорода! доставка кислорода При рассмотрении адекватности доставки кислоро- да тканям следует иметь в виду три фактора: концентрация гемоглобина, сердечный выброс и оксигенация. Количество кислорода, доступного организму за мину- ту, известно как доставка кислорода (DO2): DO2 СВ х Hb х 1,34 х Sa O2, где DO2 — доставка кислорода (мл/мин); СВ — сердечный выброс (л/мин); 1,34 — константа Гюффнера; Hb — концентрация гемоглобина (г/л); Sa O2 — насыщение (сатурация) артериальной крови кислородом (%). Например, 5000 мл крови/мин х 200 мл О2/1000 мл крови 1000 мл О2/мин.
Слайд 50

Потребление кислорода В покое и сознании человек каждую минуту потребляет около 250 мл кислорода (потребление кислорода в покое), таким образом, используется всего 25% от количества O2, содержащегося в артериальной крови. Гемоглобин смешанной венозной крови насыщен O2 примерно на 75% (от 95% до 25%). В покое клеткам предоставляется значительно больше кислорода, чем они могут использовать. При физической нагрузке потребление повышается, что обычно компенсируется путем повышения сердечного выброса
Слайд 51

Транспорт кислорода и анестезия
Гиповентиляция может возникать во время анестезии вследствие обструкции дыхательных путей, действия ингаляционных анестетиков, опиоидов и гипнотиков. Альвеолярное РО2 определяется балансом между поступлением кислорода при дыхании и его потреблением в процессе метаболизма. Гиповентиляция и снижение концентрация кислорода на вдохе ведет к снижению альвеолярного РО2. Повышенное потребление кислорода при возросших метаболических потребностях, например, на фоне послеоперационного озноба или гипертермии, также приводит к снижению РAО2. При снижении Ра О2 ниже 60 мм рт. ст. (8 к Па) хеморецепторы каротидного синуса и аорты вызывают гипервентиляцию и повышение сердечного выброса, что опосредовано симпатической стимуляцией. Во время операции эта компенсаторная реакция на гипоксию подавляется анестетиками, что какое-то время распространяется на послеоперационный период.
Слайд 52

Транспорт кислорода и анестезия После индукции в наркоз наблюдается быстрое снижение ФОЕ, главным образом обусловленное утратой тонуса респираторных мышц и грудной клетки. Происходит снижение ФОЕ ниже объема закрытия — экспираторного показателя емкости, при котором закрываются мелкие дыхательные пути. Эти области могут оставаться закрытыми на протяжении всего времени дыхательного цикла, что ведет к шунтированию. развитие нарушений V/Q вследствие закрытия дыхательных путей (шунт) будет повышать альвеолярно-артериальный градиент по O2. После индукции анестезии это «венозное примешивание» нарастает с 1% до 10% Это следует рассматривать как неизбежный побочный эффект анестезии и объясняет необходимость использования дополнительного O2 во время анестезии для поддержания нормальной оксигенации. Более того, ингаляционные анестетики подавляют гипоксическую легочную вазоконстрикцию, при этом перфузия плохо вентилируемых или коллабированных альвеол не будет снижаться в должной мере. Многие анестетики снижают сердечный выброс и доставку кислорода.
Слайд 53

Транспорт кислорода и анестезия Снижение доставки кислорода к тканям частично компенсируется за счет того, что анестезия снижает уровень метаболизма и, следовательно, потребности в кислороде на величину порядка 15%. Искусственная вентиляция устраняет работу дыхания и снижает потребности в кислороде еще на 6%. Анестетики не оказывают влияния на способность гемоглобина переносить кислород. Во время поддержания анестезии фракция вдыхаемого кислорода при имеющейся возможности должна всегда быть равной или превышать 30% для компенсации гиповентиляции и легочного шунта, сопровождающих анестезию. У пациентов с риском снижения доставки (анемия, снижение сердечного выброса) или повышенным потреблением кислорода (лихорадка) может потребоваться дальнейшее увеличение фракции вдыхаемого кислорода. Хотя нормальное значение Рa О2 при возросшем легочном шунтировании может быть восстановлено и поддерживаться за счет повышенной фракции вдыхаемого кислорода, приходится отметить, что при значениях легочного шунта более 30% эта мера перестает быть эффективной
Слайд 54

Транспорт кислорода и анестезия У пациентов с исходно низкой ФОЕ (новорожденные, беременные, полные пациенты) или низким содержанием гемоглобина и, следовательно, уменьшенным запасом кислорода десатурация протекает особенно быстро — преоксигенация у них имеет особую значимость и должна проводиться со всей тщательностью! Преоксигенация подразумевает дыхание 100% кислородом в течение трех минут через плотно прижатую к лицу маску, соединенную с дыхательным контуром наркозного аппарата. Это время необходимо для вытеснения азота из ФОЕ легких кислородом (денитрогенизация) в условиях спонтанной нормовентиляции. При возникновении любого внезапного нарушения течения анестезии первое, что требуется сделать еще до определения причины, — дать 100% кислород. Это один из ключевых подходов к неотложной терапии острых нарушений дыхания и кровообращения.
Слайд 55

После обширных оперативных вмешательств повышенное примешивание неоксигенированной, венозной крови (нарушения V/Q — шунт, и закрытие дыхательных путей), а также аномальный ответ на гипоксию сохраняются на протяжении периода длительностью до трех суток. Послеоперационная гиповентиляция — частое явление, которое может возникать вследствие остаточного действия средств общей анестезии, использования опиоидов, боли или обструкции дыхательных путей. Озноб в раннем послеоперационном периоде повышает потребление кислорода. Оксигенотерапия в послеоперационном периоде необходима всем пациентам, находящимся без сознания (в палате пробуждения), при ознобе, гиповентиляции и риске развития сердечно-сосудистых нарушений (ИБС).
Слайд 56

аноксические смеси газов Если по ошибке пациенту дана 100% закись азота, снижение Ра О2 происходит значительно быстрее, чем при апноэ. Снижение Рa О2 до критических значений произойдет быстрее чем за 10 секунд! Это происходит потому, что кислород, зарезервированный в легких и крови, быстро вымывается с каждым вдохом газовой смеси, не содержащей кислород. Таким образом, снижение Рa О2 произойдет быстрее, чем в случае, если бы он просто прекратил поступать и использовался на покрытие метаболических потребностей организма (250 мл/мин). Современные аппараты для анестезии имеют встроенные устройства, предупреждающие непреднамеренную подачу 100% N2O. диффузионная гипоксия Закись азота в 40 раз лучше растворяется в крови, чем азот. При прекращении подачи закиси азота в конце анестезии она в течение 2–3 минут в больших количествах продолжает диффундировать в альвеолы из крови. Если пациент дышит окружающим воздухом, присутствие в газовой смеси закиси азота и азота в альвеолах снижает Pa O2. Это явление называется диффузионной гипоксией и может быть устранено путем повышения концентрации O2 в альвеолах за счет подачи 100% кислорода на протяжении 2–3 минут после прекращения подачи закиси азота.
Слайд 57

транспорт углекислого газа
Углекислый газ образуется в митохондриях в результате клеточного метаболизма. В результате темп образования CO2 составляет в покое при смешанном питании около 200 мл/мин. Этот объем соответствует 80% поглощенного кислорода, что дает респираторный коэффициент, равный 0,8 (RQ — соотношение между темпом образования CO2 и темпом потребления кислорода). Углекислый газ переносится из тканей к легким с кровью тремя способами: 1) в растворенном виде, 2) в виде угольной кислоты (вода — буфер), 3) в связанном с белками виде (в частности, с гемоглобином). Приблизительно 75% CO2 транспортируется эритроцитами и 25% в плазме. Углекислый газ в 20 раз лучше растворяется в воде, чем кислород, что соответствует закону генри , гласящему, что количество молекул газа в растворе пропорционально его парциальному давлению на границе с жидкостью. При 37 С коэффициент растворимости CO2 составляет 0,0308 ммоль/литр/мм рт. ст. (или 0,231 ммоль/л/к Па).
Слайд 58

Растворимость повышается по мере снижения температуры: при 37 С растворимость будет составлять 0,5 мл/к Па в 100 мл крови. Парциальное давление CO2 в артериальной и смешанной венозной крови составляет соответственно 40 мм рт. ст. (5,3 к Па) и 46 мм рт. ст. (6,1 к Па). Таким образом, артериальная кровь будет содержать около 2,5 мл растворенного CO2 на 100 мл, а венозная крови — 3 мл на 100 мл. При сердечном выбросе 5 л/мин осуществляется транспорт 150 мл растворенного CO2 к легким, из которого 25 мл (около 16%) будет удаляться с выдохом.
Слайд 59

Угольная кислота Углекислый газ взаимодействует с водой с образованием угольной кислоты; эта реакция ускоряется ферментом карбоангидраза. Затем угольная кислота может свободно диссоциировать Карбоангидраза присутствует во многих органах, включая глазное яблоко, почки и головной мозг.
Слайд 60

Углекислый газ и вода свободно диффундируют в эритроциты и конвертируются в угольную кислоту, которая затем диссоциирует с образованием ионов водорода и бикарбоната. Ионы водорода не проходят через клеточные мембраны, но диффузия CO2 не ограничена. Однако мембрана эритроцита обеспечивает диффузию ионов бикарбоната в плазму в обмен на ионы хлора — феномен, известный как хлоридный сдвиг (равновесие Гиббса—Доннана (Gibbs—Donnan) или эффект Гамбургера (Hamburger)).
Слайд 61

Связывание CО 2 гемоглобином и прочими белками Углекислый газ быстро присоединяется к нейтральной терминальной аминогруппе (R–NH2) с образованием карбаминовых соединений : R–NH2 CO2 RNH–CO2 H . Восстановленный гемоглобин является единственным белком, который может эффективно связывать ионы водорода при физиологическом значении p H, что объясняется высоким содержанием в его составе аминокислоты гистидина , с имидазольной группой которой связываются ионы H . Около 30% CO2, покидающего организм с выдыхаемой газовой смесью, поступает в легкие в связанном с гемоглобином виде.
Слайд 62

Транспорт углекислого газа в Тканях
При взаимодействии CO2 с водой образуется угольная кислота,протекает очень медленно в плазме, но быстро в эритроцитах в связи с наличием там фермента карбоангидразы. Угольная кислота (H2CO3) диссоциирует с образованием ионов H и HCO3–, что ведет к повышению концентрации этих ионов в эритроцитах. ионы бикарбоната могут покидать эритроциты, а ионы водорода не способны С целью поддержания электронейтральности место ионов бикарбоната занимают ионы хлорида (Cl–), поступающие из плазмы.
Слайд 63

При повышении кислотности связь между гемоглобином и кислородом ослабляется, при этом восстановление гемоглобина обеспечивает защелачивание имидазольной группы. На уровне тканей окисленные имидазольные группы ослабляют сродство к кислороду, тогда как ионы водорода нейтрализуются гемоглобином, который начинает проявлять более щелочные свойства. Транспорт углекислого газа в легких Связывание кислорода с гемоглобином облегчается при защелачивании гистидиновых групп: аффинитет гема к кислороду повышается по мере освобождения CO2 , что является одной из причин эффекта Бора (Bohr): O2 Hb H HCO3– Hb O2 H2O CO2. Освобождение гемоглобина сдвигает равновесие реакции в пользу образования и выведения CO2. Концентрация HCO3– снижается по мере накопления и элиминации CO2
Слайд 64

Слайд 65

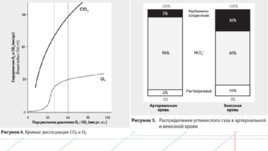
Кривая диссоциации углекислого газа устанавливает связь между Pa CO2 и количеством углекислого газа, переносимого с кровью (мл) Количество растворенного CO2 и бикарбоната будет варьировать в зависимости от PCO2, но не зависит от состояния гемоглобина. Однако количество карбаминогемоглобина в значительной мере определяется оксигенацией гемоглобина и в меньшей степени PCO2. Парциальное давление CO2 в смешанной венозной крови составляет 46 мм рт. ст. (6,1 к Па), в артериальной крови 40 мм рт. ст. (5,3 к Па). Общее содержание CO2 в венозной и артериальной крови составляет соответственно 520 и 480 мл/л.
Слайд 66

Высокое содержание CO2 в венозной капиллярной крови снижает аффинитет гемоглобина к кислороду, приводя к его высвобождению в тканях. При этом происходит сдвиг кривой диссоциации оксигемоглобина вправо ( эффект Бора) , а деоксигенированный гемоглобин связывает большее количество CO2 по сравнению с оксигенированным ( эффект Хэлдэйна ). Высвобождение кислорода в капиллярном русле приводит к усилению щелочных свойств молекулы гемоглобина (становится более сильным акцептором протонов). Таким образом, гемоглобин повышает количество CO2, переносимого с венозной кровью : Hb O2 CO2 H2O Hb H HCO3– O2. Каждая молекула CO2, поступающая в эритроцит, повышает внутриклеточное осмотическое давление посредством роста концентрации ионов HCO3– или Cl–. Как следствие, происходит увеличение объема эритроцитов, что объясняет более высокое значение гематокрита венозной крови, которое на 3% выше, чем артериальной. При сравнении с артериальной, венозную кровь также отличают более высокая концентрация HCO3– и сниженная концентрация хлоридов. различия между артериальной и венозной кровью
Слайд 67
Слайд 68

значение p H Эритроцито в Полное восстановление гемоглобина ведет к повышению p H крови на 0,03. При снижении сатурации на 25% p H повышается на 0,007 (при постоянном PCO2). Если PCO2 повышается на 6 мм рт. ст. (0,8 к Па), что соответствует артериовенозной разности, происходит снижение значения p H на 0,04. Конечный эффект этих изменений — падение p H на 0,033 (с 7,4 до 7,36). При Прохождении через легкие В легочных капиллярах эритроциты высвобождают CO2, что сопровождается повышением сродства гемоглобина к кислороду. Оксигенированный гемоглобин связывает меньшее количество ионов водорода, что ведет к «закислению» молекулы, но снижение PCO2 и сдвиг ионов хлорида и бикарбоната компенсируют эти изменения, «защелачивая» молекулу гемоглобина. Выведение воды уменьшает средний корпускулярный объем (MCV), что сопровождается снижением гематокрита. Кривая диссоциации оксигемоглобина сдвигается влево ( эффект Бора ). В плазме артериальной крови концентрация ионов хлора выше, а бикарбоната ниже, чем в венозной. роль углекислого газа в элиминации кислот Каждую минуту из организма удаляется с дыханием около 200 мл углекислого газа, что является эквивалентным выведению 12–13 молей ионов водорода за сутки. В то же время p H мочи колеблется в интервале 4,5–8,0. Даже при p H 4,0 с мочой может быть выведено не более 10–4 моль/л ионов H . Таким образом, при образовании 3 литров мочи за сутки этот путь вносит относительно небольшой вклад в элиминацию ионов водорода. Тем не менее, с мочой могут быть удалены ионы фосфата и сульфата, которые не могут быть конвертированы в CO2.
Слайд 69

Общее содержание CO2 в организме, включая ионы бикарбоната, составляет около 120 литров, что в 100 раз превышает содержание кислорода. При наступлении апноэ и полной задержке CO2 темп нарастания PCO2 будет составлять 3–6 мм рт. ст./мин (0,4–0,8 к Па/мин). Произойдет быстрое выравнивание PCO2 в альвеолярном газе и венозной крови: альвеолярное PCO2 поднимется с 40 до 46 мм рт. ст., а PO2 за минуту снизится со 105 мм рт. ст. до 40 мм рт. ст. Как следствие, у пациента быстро развивается гипоксемия. Если выполнена преоксигенация 100% кислородом, PO2 в альвеолах будет оставаться на уровне 100 мм рт. ст. с поддержанием сатурации на уровне 100% в течение нескольких минут. Каждую минуту из альвеолярного пространства будет поглощаться около 250 мл O2 c одновременным стабильным повышением Pa CO2. Спустя 5 минут в состоянии апноэ его значение будет приближаться к 75 мм рт. ст. (10 к Па), что будет сопровождаться соответствующим падением p H. Эффекты апноэ
Слайд 70
Слайд 71
Слайд 72

Слайд 73

^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
