Презентация - Гетероциклические соединения
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 93%
- Слайдов: 54
- Просмотров: 6415
- Скачиваний: 2821
- Размер: 2.58 MB
- Онлайн: Да
- Формат: ppt / pptx
Слайды и текст этой онлайн презентации
Слайд 1
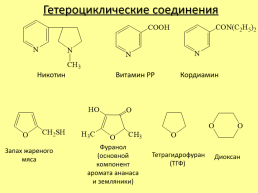
Гетероциклические соединения
Никотин
Витамин РР
Кордиамин
Фуранол (основной компонент аромата ананаса и земляники)
Запах жареного мяса
Тетрагидрофуран (ТГФ)
Диоксан
Никотин
Витамин РР
Кордиамин
Фуранол (основной компонент аромата ананаса и земляники)
Запах жареного мяса
Тетрагидрофуран (ТГФ)
Диоксан
Слайд 2
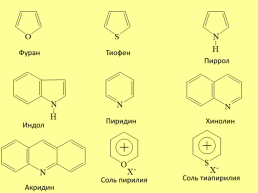
Фуран
Тиофен
Пиррол
Пиридин
Хинолин
Индол
Соль тиапирилия
Соль пирилия
Акридин
Слайд 3
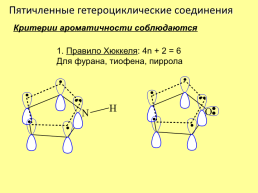
Пятичленные гетероциклические соединения
Критерии ароматичности соблюдаются
1. Правило Хюккеля: 4n + 2 = 6 Для фурана, тиофена, пиррола
Критерии ароматичности соблюдаются
1. Правило Хюккеля: 4n + 2 = 6 Для фурана, тиофена, пиррола
Слайд 4
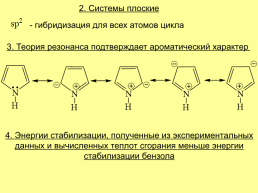
2. Системы плоские
- гибридизация для всех атомов цикла
3. Теория резонанса подтверждает ароматический характер
4. Энергии стабилизации, полученные из экспериментальных данных и вычисленных теплот сгорания меньше энергии стабилизации бензола
- гибридизация для всех атомов цикла
3. Теория резонанса подтверждает ароматический характер
4. Энергии стабилизации, полученные из экспериментальных данных и вычисленных теплот сгорания меньше энергии стабилизации бензола
Слайд 5

5. Легкость протекания реакций электрофильного замещения (электроноизбыточные системы)
Фуран менее ароматичен, т.к. электроотрицательность кислорода максимальна, то есть диеновый характер более выражен
Фуран менее ароматичен, т.к. электроотрицательность кислорода максимальна, то есть диеновый характер более выражен
Слайд 6
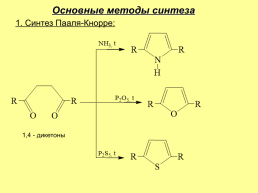
Основные методы синтеза
1. Синтез Пааля-Кнорре:
1,4 - дикетоны
1. Синтез Пааля-Кнорре:
1,4 - дикетоны
Слайд 7
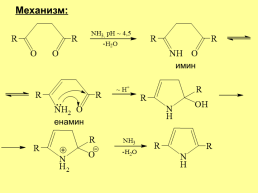
Механизм:
имин
енамин
имин
енамин
Слайд 8
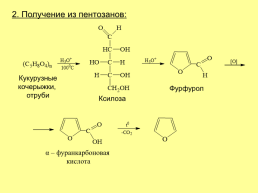
2. Получение из пентозанов:
Кукурузные кочерыжки, отруби
Фурфурол
Ксилоза
α – фуранкарбоновая кислота
Кукурузные кочерыжки, отруби
Фурфурол
Ксилоза
α – фуранкарбоновая кислота
Слайд 9
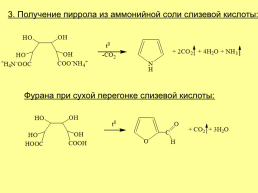
3. Получение пиррола из аммонийной соли слизевой кислоты:
Фурана при сухой перегонке слизевой кислоты:
Фурана при сухой перегонке слизевой кислоты:
Слайд 10
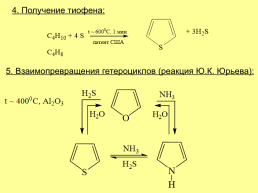
4. Получение тиофена:
5. Взаимопревращения гетероциклов (реакция Ю.К. Юрьева):
5. Взаимопревращения гетероциклов (реакция Ю.К. Юрьева):
Слайд 11
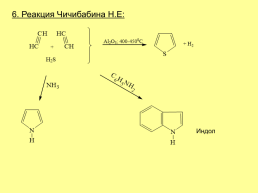
6. Реакция Чичибабина Н.Е:
Индол
Индол
Слайд 12
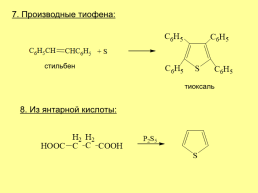
7. Производные тиофена:
стильбен
тиоксаль
8. Из янтарной кислоты:
стильбен
тиоксаль
8. Из янтарной кислоты:
Слайд 13
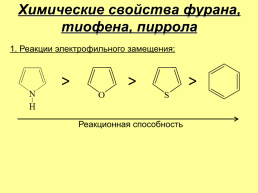
Химические свойства фурана, тиофена, пиррола
1. Реакции электрофильного замещения:
>
>
>
Реакционная способность
1. Реакции электрофильного замещения:
>
>
>
Реакционная способность
Слайд 14
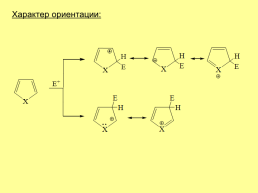
Характер ориентации:
Слайд 15
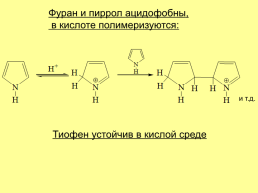
Фуран и пиррол ацидофобны,
в кислоте полимеризуются:
и т.д.
Тиофен устойчив в кислой среде
и т.д.
Тиофен устойчив в кислой среде
Слайд 16
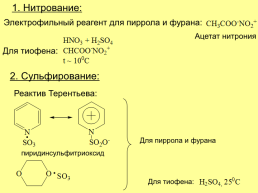
1. Нитрование:
Электрофильный реагент для пиррола и фурана:
Ацетат нитрония
Для тиофена:
2. Сульфирование:
Реактив Терентьева:
Для пиррола и фурана
пиридинсульфитриоксид
Для тиофена:
Электрофильный реагент для пиррола и фурана:
Ацетат нитрония
Для тиофена:
2. Сульфирование:
Реактив Терентьева:
Для пиррола и фурана
пиридинсульфитриоксид
Для тиофена:
Слайд 17
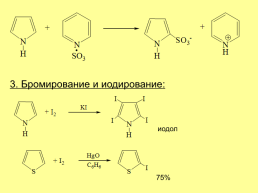
3. Бромирование и иодирование:
иодол
75%
Слайд 18
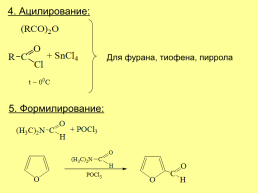
4. Ацилирование:
Для фурана, тиофена, пиррола
5. Формилирование:
Для фурана, тиофена, пиррола
5. Формилирование:
Слайд 19
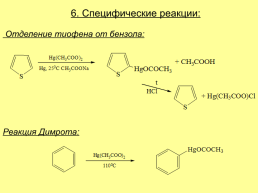
6. Специфические реакции:
Отделение тиофена от бензола:
Реакция Димрота:
Отделение тиофена от бензола:
Реакция Димрота:
Слайд 20
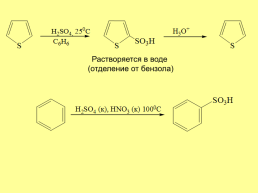
Растворяется в воде (отделение от бензола)
Слайд 21
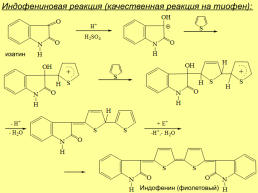
Индофениновая реакция (качественная реакция на тиофен):
изатин
Индофенин (фиолетовый)
изатин
Индофенин (фиолетовый)
Слайд 22
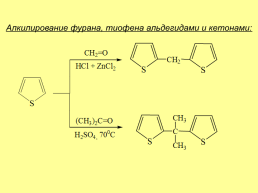
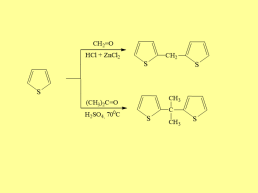
Алкилирование фурана, тиофена альдегидами и кетонами:
Слайд 23
Слайд 24
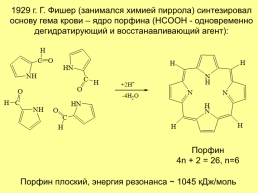
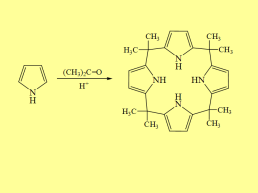
1929 г. Г. Фишер (занимался химией пиррола) синтезировал основу гема крови – ядро порфина (HCOOH - одновременно дегидратирующий и восстанавливающий агент):
Порфин 4n + 2 = 26, n=6
Порфин плоский, энергия резонанса ~ 1045 кДж/моль
Порфин 4n + 2 = 26, n=6
Порфин плоский, энергия резонанса ~ 1045 кДж/моль
Слайд 25
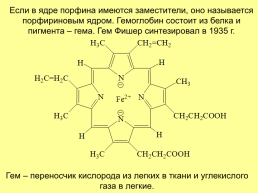
Если в ядре порфина имеются заместители, оно называется порфириновым ядром. Гемоглобин состоит из белка и пигмента – гема. Гем Фишер синтезировал в 1935 г.
Гем – переносчик кислорода из легких в ткани и углекислого газа в легкие.
Гем – переносчик кислорода из легких в ткани и углекислого газа в легкие.
Слайд 26
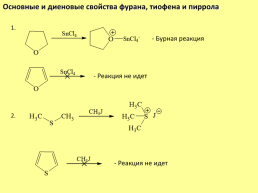
Основные и диеновые свойства фурана, тиофена и пиррола
1.
- Бурная реакция
- Реакция не идет
2.
- Реакция не идет
1.
- Бурная реакция
- Реакция не идет
2.
- Реакция не идет
Слайд 27
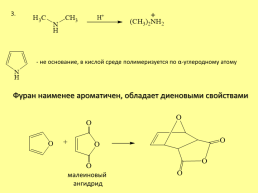
3.
- не основание, в кислой среде полимеризуется по α-углеродному атому
Фуран наименее ароматичен, обладает диеновыми свойствами
малеиновый ангидрид
- не основание, в кислой среде полимеризуется по α-углеродному атому
Фуран наименее ароматичен, обладает диеновыми свойствами
малеиновый ангидрид
Слайд 28
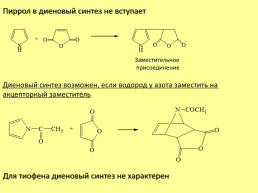
Пиррол в диеновый синтез не вступает
Заместительное присоединение
Диеновый синтез возможен, если водород у азота заместить на акцепторный заместитель
Для тиофена диеновый синтез не характерен
Заместительное присоединение
Диеновый синтез возможен, если водород у азота заместить на акцепторный заместитель
Для тиофена диеновый синтез не характерен
Слайд 29
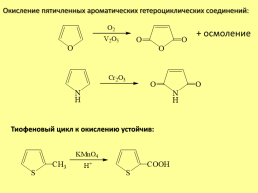
Окисление пятичленных ароматических гетероциклических соединений:
+ осмоление
Тиофеновый цикл к окислению устойчив:
+ осмоление
Тиофеновый цикл к окислению устойчив:
Слайд 30
Слайд 31
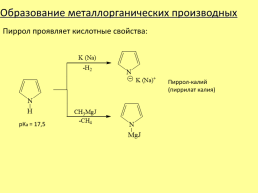
Образование металлорганических производных
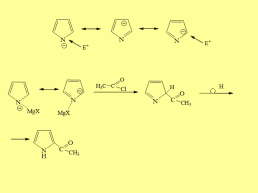
Пиррол проявляет кислотные свойства:
Пиррол-калий (пиррилат калия)
рКа = 17,5
Пиррол проявляет кислотные свойства:
Пиррол-калий (пиррилат калия)
рКа = 17,5
Слайд 32
Слайд 33
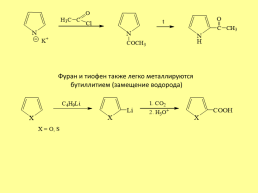
Фуран и тиофен также легко металлируются бутиллитием (замещение водорода)
Слайд 34
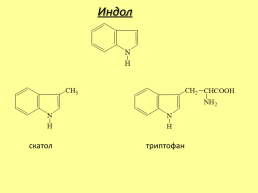
Индол
скатол
триптофан
скатол
триптофан
Слайд 35
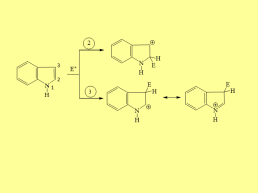
Слайд 36
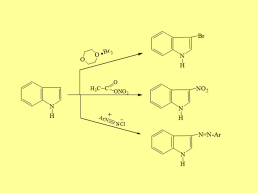
Слайд 37
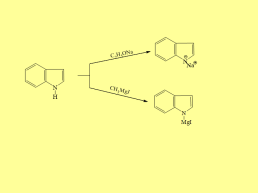
Слайд 38
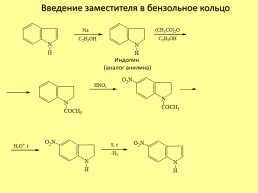
Введение заместителя в бензольное кольцо
Индолин (аналог анилина)
Индолин (аналог анилина)
Слайд 39
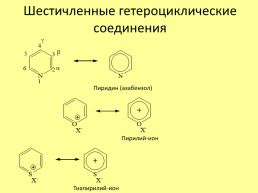
Шестичленные гетероциклические соединения
Пиридин (азабензол)
Пирилий-ион
Тиапирилий-ион
Пиридин (азабензол)
Пирилий-ион
Тиапирилий-ион
Слайд 40
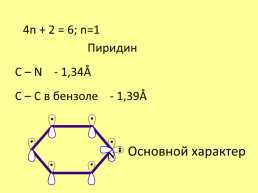
4n + 2 = 6; n=1
Пиридин
С – N - 1,34Å
С – C в бензоле - 1,39Å
Основной характер
Пиридин
С – N - 1,34Å
С – C в бензоле - 1,39Å
Основной характер
Слайд 41
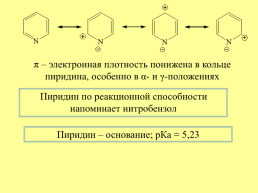
π – электронная плотность понижена в кольце пиридина, особенно в α- и γ-положениях
Пиридин по реакционной способности напоминает нитробензол
Пиридин – основание; рКа = 5,23
Слайд 42
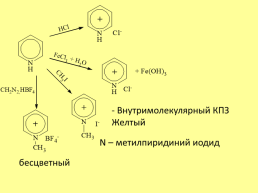
- Внутримолекулярный КПЗ Желтый
N – метилпиридиний иодид
бесцветный
Слайд 43
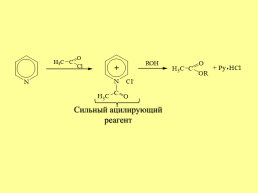
Сильный ацилирующий реагент
Слайд 44
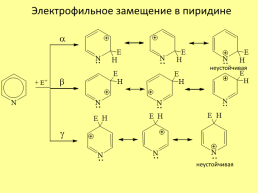
Электрофильное замещение в пиридине
неустойчивая
неустойчивая
неустойчивая
неустойчивая
Слайд 45
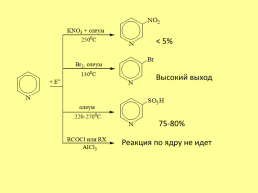
< 5%
Высокий выход
75-80%
Реакция по ядру не идет
Слайд 46
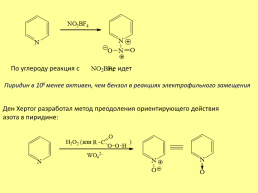
По углероду реакция с не идет
Пиридин в 106 менее активен, чем бензол в реакциях электрофильного замещения
Ден Хертог разработал метод преодоления ориентирующего действия азота в пиридине:
Слайд 47
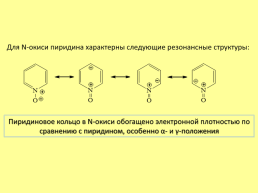
Для N-окиси пиридина характерны следующие резонансные структуры:
Пиридиновое кольцо в N-окиси обогащено электронной плотностью по сравнению с пиридином, особенно α- и γ-положения
Пиридиновое кольцо в N-окиси обогащено электронной плотностью по сравнению с пиридином, особенно α- и γ-положения
Слайд 48
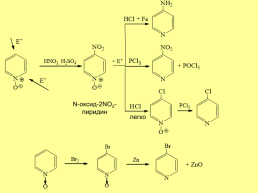
N-оксид-2NO2-пиридин
легко
Слайд 49
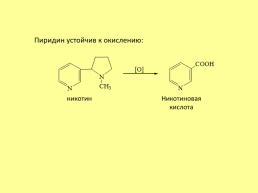
Пиридин устойчив к окислению:
никотин
Никотиновая кислота
никотин
Никотиновая кислота
Слайд 50
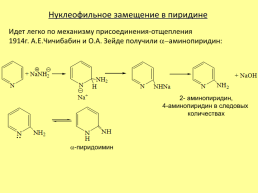
Нуклеофильное замещение в пиридине
Идет легко по механизму присоединения-отщепления 1914г. А.Е.Чичибабин и О.А. Зейде получили a-аминопиридин:
2- аминопиридин, 4-аминопиридин в следовых количествах
a-пиридоимин
Идет легко по механизму присоединения-отщепления 1914г. А.Е.Чичибабин и О.А. Зейде получили a-аминопиридин:
2- аминопиридин, 4-аминопиридин в следовых количествах
a-пиридоимин
Слайд 51
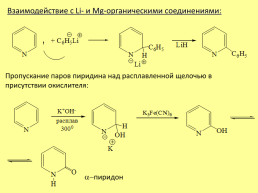
Взаимодействие с Li- и Mg-органическими соединениями:
Пропускание паров пиридина над расплавленной щелочью в присутствии окислителя:
a-пиридон
Пропускание паров пиридина над расплавленной щелочью в присутствии окислителя:
a-пиридон
Слайд 52
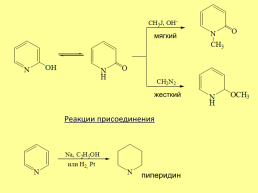
мягкий
жесткий
Реакции присоединения
пиперидин
Слайд 53
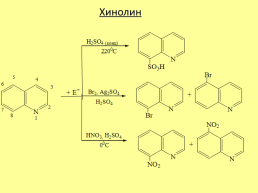
Хинолин
Слайд 54
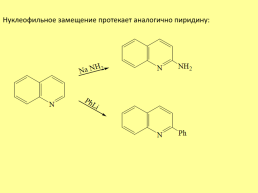
Нуклеофильное замещение протекает аналогично пиридину:
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.