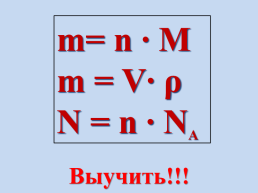Слайды и текст этой онлайн презентации
Слайд 1
Тема урока:
Количество вещества. Моль.
Слайд 2
Какие физические величины можно использовать для определения меры веществ? В каких единицах измеряются эти физические величины?
Слайд 4
1 карат = 0,2 г
1 баррель нефти
=158,988 л
Слайд 6
Можно ли найти число частиц в порции вещества?
?
Слайд 7
Моль
от французского слова «moles»-
множество
1 Моль – это количество вещества,
в котором содержится
6,02 ∙1023 частиц
Слайд 8
Число частиц
в одном моль вещества
называется
числом Авогадро (NА)
NА = 6,02 ∙1023 1/моль
Слайд 9
Количество вещества
Обозначение:
ν (ню), или n
Единица измерения: моль
Слайд 10
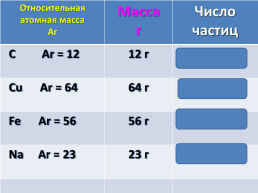
Относительная
атомная масса
Аr.Масса
г.Число частиц
C Ar = 12.12 г.6,02 ∙1023
Cu Ar = 64.64 г.6,02 ∙1023
Fe Ar = 56.56 г.6,02 ∙1023
Na Аr = 23.23 г.6,02 ∙1023
..
Слайд 11
1 моль вещества – 6,02∙1023частиц
Сколько частиц содержат
3 моль вещества?
3 ∙ 6,02∙1023 = 18,06∙1023
Сколько частиц содержат
0,5 моль вещества?
0,5 ∙ 6,02∙1023 = 3,01∙1023
Слайд 12
В общем виде:
N = n ∙ NA
N – число частиц
n – количество вещества
NA – число Авогадро
Слайд 13
Молярная масса (М) – это суммарная масса всех частиц, входящих в 1 моль вещества.
[ Mr = M ]
Mr(H2O)= 18
M(H2O)= 18 г/моль
Слайд 14
Можно ли найти массу, зная количество вещества?
Слайд 15
n = m/M
m = n ∙ M
Слайд 16
Задача.
Найти массу 3 моль атомов серы
Дано
n (S) = 3моль
M(S) = 32 г/моль
Найти m(S)
Решение
m = n ∙ M
m = 3 ∙ 32 = 96 (г)
Ответ: m(S) = 96 г
Слайд 17
Равные массы, но разные объемы, потому что ....
m = V∙ ρ
Слайд 18
m= n ∙ M
m = V∙ ρ
N = n ∙ NA
Выучить!!!
Слайд 19
Сколько ложек сахарного песка
вы кладете в чашку чая?
Рассчитайте:
какое количество сахарозы
вы выпиваете с чаем;
2) сколько молекул сахарозы (C12H22O11)
содержится в этом количестве, если
в 1 чайной ложке
примерно 5 г сахарозы.
Слайд 20
Домашнее задание:
 Правила обращения с веществами и лабораторным оборудованием
Правила обращения с веществами и лабораторным оборудованием Окружающий мир 3 класс «Из чего состоит вещество?»
Окружающий мир 3 класс «Из чего состоит вещество?» Тест: «Строение вещества»
Тест: «Строение вещества» Простые вещества - металлы
Простые вещества - металлы Теория строения органических веществ А.М. Бутлерова (10 класс)
Теория строения органических веществ А.М. Бутлерова (10 класс) Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел.
Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел. Транспорт веществ в организме животных
Транспорт веществ в организме животных