Слайды и текст этой онлайн презентации
Слайд 1
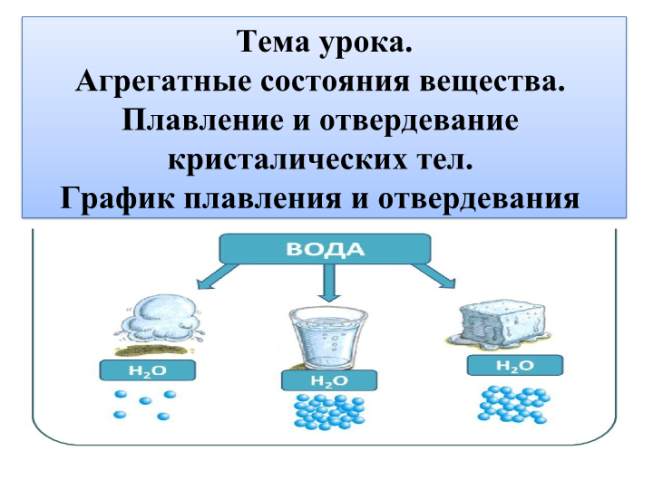
Тема урока.
Агрегатные состояния вещества.
Плавление и отвердевание
кристалических тел.
График плавления и отвердевания
кристаллических тел.
Слайд 2
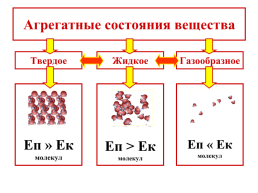
Агрегатные состояния вещества
Твердое
Жидкое
Газообразное
Еп » Ек
молекул
Еп > Ек
молекул
Еп « Ек
молекул
Слайд 4
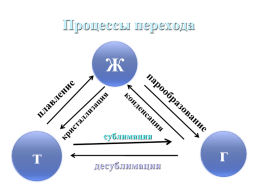
Процессы перехода
плавление
парообразование
конденсация
кристаллизация
сублимация
десублимация
Слайд 5
Изменения агрегатного состояния вещества
Плавление - переход вещества из твердого состояния в жидкое.
Парообразование - переход вещества из жидкого состояния в газообразное.
Сублимация - переход вещества из твердого состояния в газообразное
Кристаллизация - переход вещества из жидкого состояния в твердое.
Конденсация - переход вещества из газообразного состояния в жидкое.
Десублимация - переход вещества из газообразного состояния в твердое.
Слайд 6
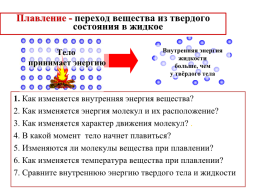
Плавление - переход вещества из твердого состояния в жидкое
Внутренняя энергия жидкости
больше, чем
у твёрдого тела
Тело
принимает энергию
1. Как изменяется внутренняя энергия вещества?
2. Как изменяется энергия молекул и их расположение?
3. Как изменяется характер движения молекул? .
4. В какой момент тело начнет плавиться?
5. Изменяются ли молекулы вещества при плавлении?
6. Как изменяется температура вещества при плавлении?
7. Сравните внутреннюю энергию твердого тела и жидкости
Слайд 7
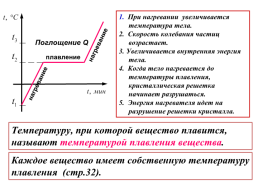
1. При нагревании увеличивается температура тела.
2. Скорость колебания частиц возрастает.
3. Увеличивается внутренняя энергия тела.
4. Когда тело нагревается до температуры плавления, кристаллическая решетка начинает разрушаться.
5. Энергия нагревателя идет на разрушение решетки кристалла.
Поглощение Q
нагревание
плавление
нагревание
Температуру, при которой вещество плавится, называют температурой плавления вещества.
Каждое вещество имеет собственную температуру плавления (стр.32).
Слайд 8
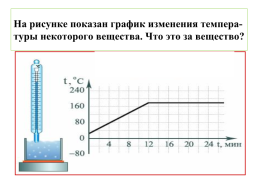
На рисунке показан график изменения темпера-туры некоторого вещества. Что это за вещество?
Слайд 9
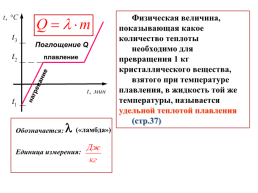
Физическая величина, показывающая какое количество теплоты
необходимо для превращения 1 кг кристаллического вещества,
взятого при температуре плавления, в жидкость той же температуры, называется удельной теплотой плавления
(стр.37)
Поглощение Q
плавление
нагревание
(«ламбда»)
Обозначается:
Единица измерения:
Слайд 10
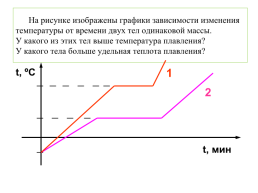
На рисунке изображены графики зависимости изменения температуры от времени двух тел одинаковой массы. У какого из этих тел выше температура плавления? У какого тела больше удельная теплота плавления?
t, ºC
t, мин
Слайд 11
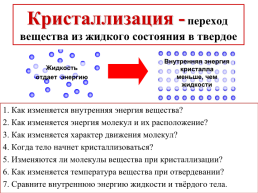
Кристаллизация - переход вещества из жидкого состояния в твердое
Внутренняя энергия кристалла
меньше, чем
жидкости
Жидкость
отдает энергию
1. Как изменяется внутренняя энергия вещества?
2. Как изменяется энергия молекул и их расположение?
3. Как изменяется характер движения молекул?
4. Когда тело начнет кристаллизоваться?
5. Изменяются ли молекулы вещества при кристаллизации?
6. Как изменяется температура вещества при отвердевании?
7. Сравните внутреннюю энергию жидкости и твёрдого тела.
Слайд 12
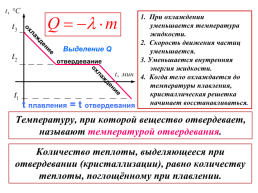
1. При охлаждении уменьшается температура жидкости.
2. Скорость движения частиц уменьшается.
3. Уменьшается внутренняя энергия жидкости.
4. Когда тело охлаждается до температуры плавления, кристаллическая решетка начинает восстанавливаться.
охлаждение
Выделение Q
отвердевание
охлаждение
t плавления = t отвердевания
Температуру, при которой вещество отвердевает, называют температурой отвердевания.
Количество теплоты, выделяющееся при отвердевании (кристаллизации), равно количеству теплоты, поглощённому при плавлении.
Слайд 13
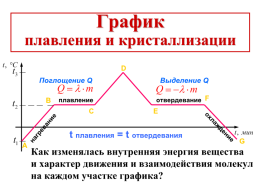
График
плавления и кристаллизации
D
Поглощение Q
Выделение Q
F
B
плавление
отвердевание
C
E
охлаждение
нагревание
t плавления = t отвердевания
G
А
Как изменялась внутренняя энергия вещества
и характер движения и взаимодействия молекул
на каждом участке графика?
Слайд 14
Запомни:
При плавлении происходит разрушение кристаллической решётки. Расстояние между частицами вещества увеличивается. Соответственно увеличивается потенциальная энергия частиц.
При отвердевании вещества происходит образование кристаллической решетки, потенциальная энергия частиц уменьшается.
Слайд 15
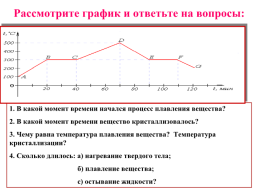
Рассмотрите график и ответьте на вопросы:
1. В какой момент времени начался процесс плавления вещества?
2. В какой момент времени вещество кристаллизовалось?
3. Чему равна температура плавления вещества? Температура кристаллизации?
4. Сколько длилось: а) нагревание твердого тела;
б) плавление вещества;
с) остывание жидкости?
Слайд 16
Вопросы
Переход из твердого состояния в жидкое состояние называется...
Переход из жидкого состояния в твердое состояние называется...
Удельная теплота плавления …..
Количество теплоты, необходимое для плавления ….
Количество теплоты, выделяющееся при кристаллизации ….
Слайд 17
Качественные задачи
Могут ли быть в жидком состоянии кислород и водород?
Могут ли быть в газообразном состоянии железо и золото?
Кусок свинца нагрели и он перешёл в жидкое состояние. Как при этом изменилась скорость движения молекул, их расположение, внутренняяя энергия вещества?
Слайд 18
3. Можно ли в алюминиевом котле расплавить медь? Цинк?
4. Какие металлы можно расплавить в медном сосуде?
5. В каком состоянии находятся серебро и вольфрам при температуре 1000 0С ?
6. Температура газовой горелки 5000 С. Посудой из каких металлов можно пользоваться?
7. Какой металл расплавится на ладони?
Слайд 19
Количество теплоты, необходимое для плавления Q = m = Q / m m = Q /
Слайд 20
Количество теплоты, выделяющееся при кристаллизации: Q = - m
Слайд 21
Задачи
Алюминиевый и медный бруски массой 1 кг каждый нагреты до температуры их плавления. Для плавления какого тела потребуется больше количества теплоты? На сколько больше?
На сколько при плавлении увеличится внутренняя энергия ртути, свинца, меди массами по 1 кг, взятых при их температурах плавления?
Слайд 22
3. Сколько энергии нужно затратить, чтобы расплавить лед массой 4 кг при температуре 00С ?
4. Сколько энергии требуется затратить, чтобы расплавить свинец массой 20 кг при температуре плавления? Сколько энергии понадобится для этого, если начальная температура свинца 270С?
Слайд 23
Домашнее задание:
§ 12 – 15 прочитать, отвечать на вопросы (у)
Упр.8 № 1 - 3
Спасибо за урок!
Желаю успехов!
 Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел
Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел Изменение агрегатных состояний вещества. Плавление и отвердевание кристаллических тел
Изменение агрегатных состояний вещества. Плавление и отвердевание кристаллических тел Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах
Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах Плавление и отвердевание. График плавления и отвердевания. Удельная теплота плавления
Плавление и отвердевание. График плавления и отвердевания. Удельная теплота плавления Изменение агрегатного состояния вещества
Изменение агрегатного состояния вещества Агрегатные состояния вещества
Агрегатные состояния вещества Обобщение материала по теме Агрегатные состояния вещества
Обобщение материала по теме Агрегатные состояния вещества