Слайды и текст этой онлайн презентации
Слайд 1
Изменение агрегатных состояний вещества
Плавление и отвердевание кристаллических тел
8 класс
Слайд 2
Вспомни!
Из чего состоит вещество?
Какую энергию называют внутренней энергией тела?
От чего зависит внутренняя энергия тела?
Как можно изменить внутреннюю энергию?
В каких агрегатных состояниях может находиться вещество?
Слайд 3
Что же отличает одно состояние вещества от другого?
Каковы особенности молекулярного строения газов, жидкостей и твердых тел?
Слайд 4
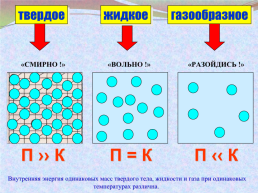
твердое
жидкое
газообразное
«СМИРНО !»
«ВОЛЬНО !»
«РАЗОЙДИСЬ !»
П ›› К
П = К
П ‹‹ К
Внутренняя энергия одинаковых масс твердого тела, жидкости и газа при одинаковых температурах различна.
Слайд 5
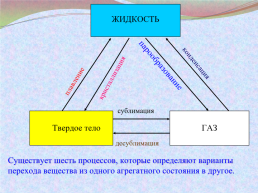
ЖИДКОСТЬ
конденсация
плавление
парообразование
кристаллизация
сублимация
Твердое тело
ГАЗ
десублимация
Существует шесть процессов, которые определяют варианты перехода вещества из одного агрегатного состояния в другое.
Слайд 6
Примеры процессов, при которых происходят агрегатные превращения вещества
Плавление - таяние льда
Слайд 7
Кристаллизация- замерзание воды
Слайд 8
Испарение воды, выбрасываемой гейзером
Слайд 9
Конденсация – образование облаков
Слайд 10
Сублимация
Графит можно нагреть до тысячи градусов, и тем не менее в жидкость он не превратится.
Слайд 11
Десублимация - узоры на окнах
Слайд 12
Некоторые процессы сопровождаются поглощением тепла. Другие – отдачей тепла.
Слайд 13
Плавление
По мере возрастания температуры энергия колебательного
движения атомов в твёрдом теле возрастает и, наконец,
наступает такой момент, когда связи между атомами
начинают разрываться. При этом твердое тело переходит в
жидкое состояние. Такой переход называется плавлением.
Плавление происходит при строго определённой температуре.
Слайд 16
Запомни!
Температура, при которой происходит переход твердого вещества в жидкое называется температурой плавления.
Во время процесса плавления температура остается постоянной, хотя телу передается количество теплоты, т.е. внутренняя энергия увеличивается.
Вещество отвердевает при той же температуре, при которой плавится.
tпл = tкр
Слайд 17
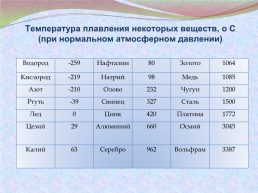
Температура плавления некоторых веществ, о С (при нормальном атмосферном давлении)
Водород.-259.Нафталин.80.Золото.1064
Кислород.-219.Натрий.98.Медь.1085
Азот.-210.Олово.232.Чугун.1200
Ртуть.-39.Свинец.327.Сталь.1500
Лед.0.Цинк.420.Платина.1772
Цезий.29.Алюминий.660.Осмий.3045
Калий.63.Серебро.962.Вольфрам.3387
Слайд 18
Проверь себя!
1.Какой из металлов, приведенных в таблице, самый легкоплавкий?
2. Какой из металлов самый тугоплавкий?
3.Какой из двух металлов алюминий или медь, вы бы выбрали, чтобы изготовить посуду годную для расплавления в ней другого металла?
4.Какой из кусков стальной или вольфрамовый останется твердым, если будет брошен в расплавленное железо?
5.Будет ли плавиться чугунная деталь, брошенная в расплавленную медь?
6.Олово переведено из одного состояния в другое. Так что внутренняя энергия уменьшилась. Затвердело оно или расплавилось?
Слайд 19
Запомни!
При охлаждении расплавленного твёрдого тела происходит обратный процесс, называемый кристаллизацией.
Образование кристалла также происходит при постоянной температуре, равной температуре плавления.
tпл = tкр
При кристаллизации жидкости выделяется такое же количество теплоты, какое поглощается при плавлении вещества той же массы.
Слайд 21
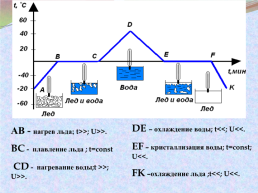
DE – охлаждение воды; t<<; U<<.
EF – кристаллизация воды; t=const; U<<.
FK –охлаждение льда ;t<<; U<<.
АВ - нагрев льда; t>>; U>>.
BC - плавление льда ; t=const
CD - нагревание воды;t >>; U>>.
Слайд 22
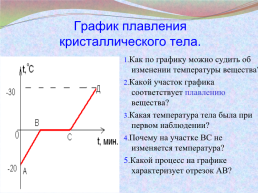
График плавления кристаллического тела.
1.Как по графику можно судить об изменении температуры вещества?
2.Какой участок графика соответствует плавлению вещества?
3.Какая температура тела была при первом наблюдении?
4.Почему на участке ВС не изменяется температура?
5.Какой процесс на графике характеризует отрезок АВ?
Слайд 23
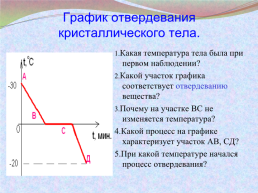
График отвердевания кристаллического тела.
1.Какая температура тела была при первом наблюдении?
2.Какой участок графика соответствует отвердеванию вещества?
3.Почему на участке ВС не изменяется температура?
4.Какой процесс на графике характеризует участок АВ, СД?
5.При какой температуре начался процесс отвердевания?
Слайд 24
Вычисление количества теплоты при плавлении
Q=λm
λ – удельная теплота плавления.
Физический смысл коэффициента λ
- физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1кг, чтобы при температуре плавления полностью перевести его в жидкое состояние.
Слайд 25
Вычисление количества теплоты при отвердевании
При кристаллизации вещества выделяется такое же
количество теплоты, которое было затрачено на
образование расплава.
Знак «-» показывает, что количество вещества выделяется.
Q= - λm
Слайд 26
Вещество.Удельная теплота плавления (кДж/кг)
Алюминий.390
Железо.270
Золото.67
Лёд.330
Медь.210
Нафталин.150
Олово.59
Платина.110
Ртуть.10
Свинец.25
Серебро.100
Цинк.120
Чугун (белый).14
Чугун (серый).100
У различных веществ удельная теплота плавления разная.
Слайд 27
Домашнее задание
§37 (повторить)
§ §38,39 (учить)
 Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел.
Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел. Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел
Агрегатные состояния вещества. Плавление и отвердевание кристалических тел. График плавления и отвердевания кристаллических тел Изменение агрегатного состояния вещества
Изменение агрегатного состояния вещества Тепловые явления. Изменение агрегатных состояний веществ
Тепловые явления. Изменение агрегатных состояний веществ Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах
Твердое состояние вещества. Плавление. Кристаллическое и аморфное состояние вещества. Типы связи в кристаллах Тепловые явления. Изменение агрегатных состояний вещества (11 класс)
Тепловые явления. Изменение агрегатных состояний вещества (11 класс) Агрегатные состояния вещества
Агрегатные состояния вещества