Презентация - Урок в 11 классе «Основные способы получения металлов»
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 97%
- Слайдов: 26
- Просмотров: 4313
- Скачиваний: 1672
- Размер: 0.9 MB
- Класс: 11
- Формат: ppt / pptx
Примеры похожих презентаций
 Материалы уроков русского языка в 6 классе «Основные способы словообразования» (закрепление изученного)
Материалы уроков русского языка в 6 классе «Основные способы словообразования» (закрепление изученного) Урок русского языка 5 класс «Тема текста - Основная мысль текста»
Урок русского языка 5 класс «Тема текста - Основная мысль текста» Диагностика и контроль образовательных достижений на уроках русского языка в 5-9 классах: развитие творческих и исследовательских способностей
Диагностика и контроль образовательных достижений на уроках русского языка в 5-9 классах: развитие творческих и исследовательских способностей Способы получения металлов и их сплавов -Важнейшие месторождения металлов и их соединений в Казахстане
Способы получения металлов и их сплавов -Важнейшие месторождения металлов и их соединений в Казахстане Способы получения металлов
Способы получения металлов Личностно-ориентированный подход к формированию творческих способностей на уроках русского языка в начальных классах
Личностно-ориентированный подход к формированию творческих способностей на уроках русского языка в начальных классах К уроку химии по теме «металлы» 11 класс
К уроку химии по теме «металлы» 11 класс
Слайды и текст этой онлайн презентации
Слайд 1

Основные способы получения металлов
Урок в 11 классе
Урок в 11 классе
Слайд 2

Способы получения металлов
обычно разделяют на три типа: пирометаллургические - восстановление при высоких температурах; гидрометаллургические - восстановление из солей в растворах; электрометаллургические - электролиз раствора или расплава.
обычно разделяют на три типа: пирометаллургические - восстановление при высоких температурах; гидрометаллургические - восстановление из солей в растворах; электрометаллургические - электролиз раствора или расплава.
Слайд 3

Пирометал-лургически
получают: чугун, сталь, медь, свинец, никель, хром и другие металлы.
Доменный процесс – получение стали и чугуна
Доменный процесс – получение стали и чугуна
Слайд 4

Гидрометаллургически получают: золото, цинк, никель и некоторые другие металлы.
Получаемые металлы: Cd, Ag, Au, Cu, Zn, Mo и др.
Получаемые металлы: Cd, Ag, Au, Cu, Zn, Mo и др.
Слайд 5

Электрометал-лургически получают: щелочные и щёлочноземель-ные металлы, алюминий, магний и другие металлы.
Слайд 6

Общие способы получения металлов
1. Восстановление металлов из оксидов углем или угарным газом MеxOy + C = CO2 + Me, MеxOy + C = CO + Me, MеxOy + CO = CO2 + Me получают: Fe, Cu, Pb, Sn, Cd, Zn
Например, 1. ZnOy+ C t= CO + Zn 2. Fe3O4+ 4CO t= 4CO2 + 3Fe 3. MgO + C t= Mg + CO Не подходит для металлов, образующих карбиды с углём.
1. Восстановление металлов из оксидов углем или угарным газом MеxOy + C = CO2 + Me, MеxOy + C = CO + Me, MеxOy + CO = CO2 + Me получают: Fe, Cu, Pb, Sn, Cd, Zn
Например, 1. ZnOy+ C t= CO + Zn 2. Fe3O4+ 4CO t= 4CO2 + 3Fe 3. MgO + C t= Mg + CO Не подходит для металлов, образующих карбиды с углём.
Слайд 7

Общие способы получения металлов
2. Обжиг сульфидов с последующим восстановлением (если металл находится в руде в виде соли или основания, то последние предварительно переводят в оксид) 1 стадия – MеxSy+O2 = MеxOy+SO2 2 стадия – MеxOy + C = CO2 + Me или MеxOy + CO = CO2 + Me
Например, 1. 2ZnS + 3O2 t= 2ZnO + 2SO2↑ 2. MgCO3 t= MgO + CO2↑
2. Обжиг сульфидов с последующим восстановлением (если металл находится в руде в виде соли или основания, то последние предварительно переводят в оксид) 1 стадия – MеxSy+O2 = MеxOy+SO2 2 стадия – MеxOy + C = CO2 + Me или MеxOy + CO = CO2 + Me
Например, 1. 2ZnS + 3O2 t= 2ZnO + 2SO2↑ 2. MgCO3 t= MgO + CO2↑
Слайд 8

Общие способы получения металлов
3 Алюмотермия (в тех случаях, когда нельзя восстановить углём или угарным газом из-за образования карбида или гидрида) MеxOy + Al = Al2O3 + Me получают: Mn, Cr, Ti, Mo, W, V и др
Например, 1. 4SrO + 2Al t= Sr(AlO2)2 + 3Sr 2. 3MnO2 + 4Al t= 3Mn + 2Al2O3 3. 2Al + 3BaO t= 3Ba + Al2O3 (получают барий высокой чистоты)
3 Алюмотермия (в тех случаях, когда нельзя восстановить углём или угарным газом из-за образования карбида или гидрида) MеxOy + Al = Al2O3 + Me получают: Mn, Cr, Ti, Mo, W, V и др
Например, 1. 4SrO + 2Al t= Sr(AlO2)2 + 3Sr 2. 3MnO2 + 4Al t= 3Mn + 2Al2O3 3. 2Al + 3BaO t= 3Ba + Al2O3 (получают барий высокой чистоты)
Слайд 9

Общие способы получения металлов
4. Водородотермия - для получения металлов особой чистоты MеxOy + H2 = H2O + Me Получают металлы большей чистоты: Cu, Ni, W, Fe, Mo, Cd, Pb
Например, 1. WO3 + 3H2 t= W + 3H2O↑ 2. MoO3 + 3H2 t= Mo + 3H2O↑
4. Водородотермия - для получения металлов особой чистоты MеxOy + H2 = H2O + Me Получают металлы большей чистоты: Cu, Ni, W, Fe, Mo, Cd, Pb
Например, 1. WO3 + 3H2 t= W + 3H2O↑ 2. MoO3 + 3H2 t= Mo + 3H2O↑
Слайд 10

Восстановление металлов электрическим током (электролиз)
А) Щелочные и щелочноземельные металлы получают в промышленности электролизом расплавов солей (хлоридов): 2NaCl расплав, электр. ток. 2 Na + Cl2↑ CaCl2 расплав, электр. ток. Ca + Cl2↑ расплавов гидроксидов: 4NaOH расплав, электр. ток. 4Na + O2↑ + 2H2O (!!! используют изредка для Na)
А) Щелочные и щелочноземельные металлы получают в промышленности электролизом расплавов солей (хлоридов): 2NaCl расплав, электр. ток. 2 Na + Cl2↑ CaCl2 расплав, электр. ток. Ca + Cl2↑ расплавов гидроксидов: 4NaOH расплав, электр. ток. 4Na + O2↑ + 2H2O (!!! используют изредка для Na)
Слайд 11

Восстановление металлов электрическим током (электролиз)
Б) Алюминий в промышленности получают в результате электролиза расплава оксида алюминия в криолите Na3AlF6 (из бокситов): 2Al2O3 расплав в криолите, электр. ток. 4Al + 3 O2↑ В) Электролиз водных растворов солей используют для получения металлов средней активности и неактивных: 2CuSO4+2H2O раствор, электр. ток. 2Cu + O2 + 2H2SO4
Б) Алюминий в промышленности получают в результате электролиза расплава оксида алюминия в криолите Na3AlF6 (из бокситов): 2Al2O3 расплав в криолите, электр. ток. 4Al + 3 O2↑ В) Электролиз водных растворов солей используют для получения металлов средней активности и неактивных: 2CuSO4+2H2O раствор, электр. ток. 2Cu + O2 + 2H2SO4
Слайд 12
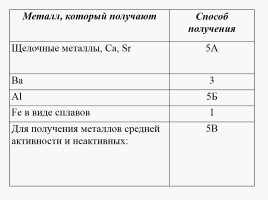
Металл, который получают Способ получения
Щелочные металлы, Ca, Sr 5А
Ba 3
Al 5Б
Fe в виде сплавов 1
Для получения металлов средней активности и неактивных: 5В
Щелочные металлы, Ca, Sr 5А
Ba 3
Al 5Б
Fe в виде сплавов 1
Для получения металлов средней активности и неактивных: 5В
Слайд 13

Примеры заданий по теме: «Общие способы получение металлов»
Задания с выбором ответа ( А10, А24, А29). А1. Реакция возможна между 1) Ag и K2SO4 (р-р) 2) Zn и KCl (р-р) 3) Mg и SnCl2 (р-р) 4) Ag и CuSO4 (р-р) А2. Какой из металлов вытесняет железо из сульфата железа (II)? 1) Cu 2) Zn 3) Sn 4) Hg
Задания с выбором ответа ( А10, А24, А29). А1. Реакция возможна между 1) Ag и K2SO4 (р-р) 2) Zn и KCl (р-р) 3) Mg и SnCl2 (р-р) 4) Ag и CuSO4 (р-р) А2. Какой из металлов вытесняет железо из сульфата железа (II)? 1) Cu 2) Zn 3) Sn 4) Hg
Слайд 14

A3. Какой из металлов вытесняет медь из сульфата меди (II)?
1) Zn 2) Ag 3) Hg 4) Au
A4. Формула вещества, восстанавливающего оксид меди (II) - это
1) CO2 2) H2 3) HNO3 4) Cl2
A5. Формула вещества, не восстанавливающего оксид железа (III) -
1) HCl 2) Al 3) H2 4) C
Слайд 15

А6. Для осуществления превращений в соответствии со схемой:
Al(OH)3 → AlCl3 → Al необходимо последовательно использовать
1) хлор и водород
2) хлорид натрия и водород
3) хлороводород и цинк
4) соляную кислоту и калий
А7. Пирометаллургический метод получения металлов отражает реакция:
1) HgS + O2 → Hg + SO2
2) CuSO4 + Fe → FeSO4 + Cu
3) 2NaCl (ток)→ 2Na + Cl2
4) CuSO4 + Zn → ZnSO4 + Cu
Слайд 16

А8. Гидрометаллургический метод получения металлов отражает реакция:
1) HgS + O2 → Hg + SO2
2) CuSO4 + Fe → FeSO4 + Cu
3) 2NaCl (ток)→ 2Na + Cl2
4) AlCl3 + 3K → Al + 3KCl
А9. В качестве восстановителя при выплавке железа в промышленности
наиболее часто используют
1) водород
2) алюминий
3) натрий
4) кокс
Слайд 17

А10. Оксид углерода (II) проявляет восстановительные свойства при нагревании с
1) N2 2) H2S 3) Fe 4) Fe2O3
Задания с кратким ответом (В3)
В1. При электролизе раствора AgNO3 на катоде выделяется
1) серебро
2) водород
3) серебро и водород
4) кислород и водород
Слайд 18

В2. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА
ВОДНОГО РАСТВОРА
А) AgF 1) Ag, F2
Б) NaNO3 2) Ag, O2, HF
B) Pb(NO3)2 3) H2, O2
Г) NaF 4) Pb, O2, HNO3
5) H2, NO2, O2
6) NaOH, H2, F2
Слайд 19

В3. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА ВОДНОГО РАСТВОРА ВОДНОГО РАСТВОРА
А) HgCl2 1) металл, хлор
Б) AlCl3 2) водород, хлор, гидроксид
В) Hg(ClO4)2 металла
Г) Na2SO3 3) водород, кислород
4) металл, кислород, кислота
5) металл, сернистый газ
6) водород, сернистый газ
Слайд 20

В4. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА
ВОДНОГО РАСТВОРА
А) нитрат цинка 1) цинк, кислород, азотная кислота
Б) бромид цинка 2) водород, кислород
В) бромид калия 3) водород, оксид азота (IV)
Г) нитрат калия 4) цинк, бром
5) водород, бром, гидроксид калия
6) калий, бром
7) калий, оксид азота (IV)
Слайд 21

В5. Установите соответствие между формулой вещества и продуктом электролиза его водного раствора, образующимся на като-де
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА
ВОДНОГО РАСТВОРА
А) Li2SO4 1) H2
Б) Ba(OH)2 2) O2
В) MgCl2 3) Cl2
Г) SnCl2 4) Li
5) Ba
6) Mg
7) Sn
Слайд 22

В6. Верны ли следующие суждения о промышленных способах получения металлов?
А. В основе пирометаллургии лежит процесс восстановления металлов из руд при высоких температурах.
Б. В промышленности в качестве восстановителей используют оксид углерода (II) и кокс.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Слайд 23

В7. Установите соответствие между металлом и способом его
электролитического получения.
МЕТАЛЛ ЭЛЕКТРОЛИЗ
А) натрий 1) водного раствора солей
Б) алюминий 2) водного раствора гидроксида
В) серебро 3) расплава поваренной соли
Г) медь 4) расплавленного оксида
5) раствора оксида в расплав-
ленном криолите
6) расплавленного нитрата
Слайд 24

В8. Установите соответствие между металлом и способом его электролитического получения.
МЕТАЛЛ ЭЛЕКТРОЛИЗ
А) калий 1) расплавленного нитрата
Б) магний 2) водного раствора гидроксида
В) медь 3) расплава хлорида
Г) свинец 4) расплавленного оксида
5) раствора оксида в расплавленном криолите
6) водного раствора солей
Слайд 25

В9. Установите соответствие между металлом и способом его электролитического получения.
МЕТАЛЛ ЭЛЕКТРОЛИЗ
А) хром 1) водного раствора солей
Б) алюминий 2) водного раствора гидроксида
В) литий 3) расплава соли
Г) барий 4) расплавленного оксида
5) раствора оксида в расплав-
ленном криолите
6) расплавленного нитрата
Слайд 26

Задания с развёрнутым ответом (С2)
С1. Напишите уравнения реакций, с помощью которых можно осуществить превращения:
Cu → Cu(NO3)2 → Cu(OH)2 → Х → Сu → CuSO4
Укажите условия протекания реакций.
C2. Даны вещества: алюминий, оксид марганца (IV), водный раствор сульфата меди и концентрированная соляная кислота.
Напишите уравнения четырёх возможных реакции между этими веществами.
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
