Слайды и текст этой онлайн презентации
Слайд 1
Периодическая система элементов
Слайд 2
Первые попытки систематизации элементов
1829 г. закон триад немецкий химик Иоганн Вольфганг Дёберейнер
В 1843 г. Леопольд Гмелин привёл таблицу химически сходных элементов, расставленных по группам в порядке возрастания "соединительных масс".
В 1850 г. немецкий врач Макс фон Петтенкоферт высказал предположение, что элементы, возможно, являются сложными образованиям и каких-то субэлементарных частиц
в 1862 г. предложил винтовой график элементов, расположенных в порядке возрастания атомных весов – т. н. "земная спираль"
Слайд 3
1864 г. закон октав Ньюлендса. в ряду элементов, размещённых в порядке возрастания атомных весов, свойства восьмого элемента сходны со свойствами первого
Слайд 4
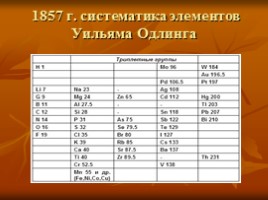
1857 г. систематика элементов Уильяма Одлинга
Слайд 5
:
в 1869 году Дмитрий Иванович Менделеев представил Русскому химическому обществу периодический закон химических элементов, изложенный в нескольких основных положениях, на основе которых он составил периодическую систему химических элементов
Основные положения
1. Элементы, расположенные по возрастанию их атомного веса, представляют явственную периодичность свойств;
2. Сходные по свойствам элементы имеют или близкие атомные веса (Os, Ir, Pt), или последовательно и однообразно увеличивающиеся (K, Rb, Cs);
3. Сопоставление элементов или их групп по величине атомного веса отвечает их т.н. валентности;
4. Элементы с малыми атомными весами имеют наиболее резко выраженные свойства, поэтому они являются типическими элементами;
5. Величина атомного веса элемента может быть иногда исправлена, если знать аналоги данного элемента;
6. Следует ожидать открытия ещё многих неизвестных элементов, например, сходных с Al или Si, с паем (атомной массой) 65-75.
Слайд 6
Первая таблица Менделеева
Слайд 7
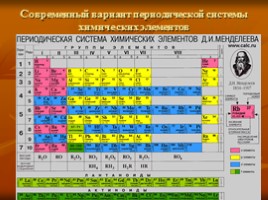
Современный вариант периодической системы химических элементов
Слайд 8
Все графические изображения взяты с поисковой системы Yandex
 Периодический закон и периодическая химических система элементов (ПСХЭ) Д.И. Менделеева
Периодический закон и периодическая химических система элементов (ПСХЭ) Д.И. Менделеева Характеристика элемента по его положению в периодической системе химических элементов Д.И. Менделеева
Характеристика элемента по его положению в периодической системе химических элементов Д.И. Менделеева Периодический закон Менделеева и периодическая система химических элементов
Периодический закон Менделеева и периодическая система химических элементов Совместимость элементов системы «человек - среда». Компьютерная безопасность
Совместимость элементов системы «человек - среда». Компьютерная безопасность Периодическая система Д.И.Менделеева (иследовательская работа)
Периодическая система Д.И.Менделеева (иследовательская работа) Обобщение и систематизация знаний по теме «Глагол»
Обобщение и систематизация знаний по теме «Глагол» Система уроков по синтаксису сложного предложения в 9 классах «Тире и двоеточие в бессоюзном предложении»
Система уроков по синтаксису сложного предложения в 9 классах «Тире и двоеточие в бессоюзном предложении»