Слайды и текст этой онлайн презентации
Слайд 1
Как часто вы обретали какое-то знание?
Как часто вам удавалось его передать кому-то другому?
На самом деле, истинное знание невозможно передать — его можно только постичь самостоятельно.
Слайд 2
1. Группа 1. Свойство простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины зарядов ядер их атомов.
2. Номер периода 2. Вертикальный столбец химических элементов.
3. Изотопы 3. Горизонтальный ряд химических элементов начинается со щелочного металла и заканчивается инертным элементом.
4. Период 4. Разновидности атомов одного и того же элемента, имеющие одинаковое число протонов в ядре, но разную массу.
5.Формулировка периодического закона 5. Число электронов на внешнем уровне.
6. Номер группы 6. Число электронных слоев в атоме
Слайд 3
1. Группа 2. Вертикальный столбец химических элементов.
2. Номер периода 6. Число электронных слоев в атоме
3. Изотопы 4. Разновидности атомов одного и того же элемента, имеющие одинаковое число протонов в ядре, но разную массу.
4. Период 3. Горизонтальный ряд химических элементов начинается со щелочного металла и заканчивается инертным элементом.
5.Формулировка периодического закона 1. Свойство простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины зарядов ядер их атомов.
6. Номер группы 5. Число электронов на внешнем уровне.
Слайд 4
Каким образом атомы
удерживаются возле друг друга в молекулах простых и сложных веществ ?
О₂, Н₂, Н₂О, HCl
Слайд 5
Ковалентная связь атомов при образовнии молекул простых веществ
Слайд 6
Цели урока
Сформировать понятие о ковалентной связи в молекулах простых веществ
Изучить механизм образования ковалентной связи в молекулах простых веществ
Слайд 7
Запишите электронное строение атома хлора.
Слайд 8
Как, не записывая электронное строение атома, определить число неспаренных электронов?
Число неспаренных электронов =
8 - №группы
Слайд 9
Группа Валентные
электроны Неспаренные электроны
V
VI
VII
Слайд 10
Группа Валентные
электроны Неспаренные электроны
V 5 3
VI 6 2
VII 7 1
Слайд 11
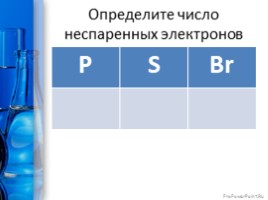
Определите число неспаренных электронов
P S Br
Слайд 12
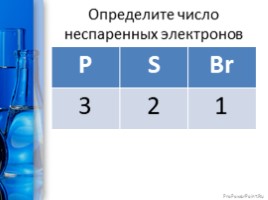
Определите число неспаренных электронов
P S Br
3 2 1
Слайд 13
Механизм образования ковалентной связи в молекулах простых веществ
Слайд 15
Химическая связь, осуществляемая общими электронными парами, называется ковалентной
Слайд 16
Задание.
Пользуясь алгоритмом, составить cхемы образования ковалентных связей в молекулах водорода, кислорода и азота.
Слайд 17
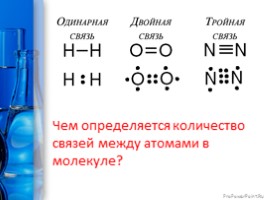
Чем определяется количество связей между атомами в молекуле?
Слайд 18
Цели урока
Сформировать понятие о ковалентной связи в молекулах простых веществ
Изучить механизм образования ковалентной связи в молекулах простых веществ
Слайд 19
Домашнее задание
§ 45
Ответить на вопросы после текста параграфа (устно)
Заполнить таблицу на листочках
«Ковалентная связь»
 Ковалентная связь
Ковалентная связь Строение ароматических углеводородов - Ароматическая связь
Строение ароматических углеводородов - Ароматическая связь Ионная связь
Ионная связь Урок русского языка в 3 классе «Связь частей речи в словосочетаниях»
Урок русского языка в 3 классе «Связь частей речи в словосочетаниях» Взаимосвязь органов и систем органов как основа гомеостаза
Взаимосвязь органов и систем органов как основа гомеостаза Взаимосвязь русского языка и экологии
Взаимосвязь русского языка и экологии Урок математики 1 класс «Связь сложения и вычитания - Вычитание вида 8-, 9-, 10-»
Урок математики 1 класс «Связь сложения и вычитания - Вычитание вида 8-, 9-, 10-»