Презентация - Создание коллаборативной среды (8 класс)
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 97%
- Слайдов: 44
- Просмотров: 2942
- Скачиваний: 1043
- Размер: 1 MB
- Класс: 8
- Формат: ppt / pptx
Примеры похожих презентаций
 Создание игры с применением игровой среды unity и языка программирования c#»
Создание игры с применением игровой среды unity и языка программирования c#» Создание современной здоровьесберегающей образовательной среды для детей ДОУ и детей с ОВЗ
Создание современной здоровьесберегающей образовательной среды для детей ДОУ и детей с ОВЗ Обучающий мастер-класс по созданию пасхального украшения «Пасхальный венок»
Обучающий мастер-класс по созданию пасхального украшения «Пасхальный венок» Создание безопасной и психологически комфортной образовательной среды в дошкольном образовательном учреждении
Создание безопасной и психологически комфортной образовательной среды в дошкольном образовательном учреждении Для 9 класса "Создание web - сайта"
Для 9 класса "Создание web - сайта" Создание развивающей образовательной среды для изучения математики: геометрический материал.
Создание развивающей образовательной среды для изучения математики: геометрический материал. Роль логопеда в создании здоровьесберегающей среды
Роль логопеда в создании здоровьесберегающей среды
Слайды и текст этой онлайн презентации
Слайд 1

Создание коллаборативной среды
Игра «Молекулы и атомы»
Слайд 2

Над этим вопросом люди задумывались ещё в древности.
В первом веке до н.э. римский поэт и философ Лукреций Кар, изложил учение Эпикура в поэме "О природе вещей", благодаря которой оно и сохранилось для следующих поколений.
,,…На морском берегу, разбивающем волны,
Платье сыреет всегда, а на солнце, вися, высыхает,
Значит, дробится вода на такие мельчайшие части,
Что недоступны они совершенно для нашего взора.”
Мозговой шторм Вопрос на размышление
Мозговой шторм Вопрос на размышление
Слайд 3

Ещё 2500 лет назад древнегреческий философ Демокрит полагал, что любой предмет состоит из мельчайших частиц –атомов.
Группу греческих философов, придерживающихся того взгляда, что существуют подобные крошечные неделимые частицы, называли атомистами
Слайд 4

Тема урока
Состав и строение атома. Изотопы
Учитель химии НИШ ХБН г.Атырау Ким Е.Г.
Учитель химии НИШ ХБН г.Атырау Ким Е.Г.
Слайд 5

Цель урока:
знать названия, размер и расположение протона, нейтрона и электрона в атоме.
знать подробную структуру атома в отношении протонов, нейтронов и электронов (только первых 20 элементов); знать значение числа протонов и числа нуклонов.
уметь объяснить полное описание ядра для названия элемента и определения количества фундаментальных частиц.
Слайд 6

Цели обучения
описывать строение атома знать понятие изотоп определять состав атомного ядра нуклидов первых 20 элементов описывать элемент по названию и по количеству частиц, содержащихся в его атоме
описывать строение атома знать понятие изотоп определять состав атомного ядра нуклидов первых 20 элементов описывать элемент по названию и по количеству частиц, содержащихся в его атоме
Слайд 7

Ожидаемый результат
Знает названия субатомных частиц атома, структуру расположения и их заряд. Знает что атомный номер совпадает числами протонов и электронов. Умеет находить число нейтронов использовав атомный номер и массовый номер. Может определить атомное и массовое число с помощью субатомных частиц каждого элемента. Может определить число субатомных частиц используя полное описание ядра.
Знает названия субатомных частиц атома, структуру расположения и их заряд. Знает что атомный номер совпадает числами протонов и электронов. Умеет находить число нейтронов использовав атомный номер и массовый номер. Может определить атомное и массовое число с помощью субатомных частиц каждого элемента. Может определить число субатомных частиц используя полное описание ядра.
Слайд 8
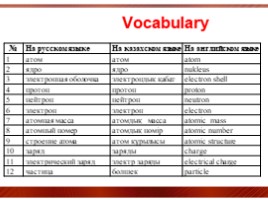
Vocabulary
№ На русском языке На казахском языке На английском языке
1 атом атом atom
2 ядро ядро nukleus
3 электронная оболочка электрондық қабат electron shell
4 протон протон proton
5 нейтрон нейтрон neutron
6 электрон электрон electron
7 атомная масса атомдық масса atomic mass
8 атомный номер атомдық нөмір atomic number
9 строение атома атом құрылысы atomic structure
10 заряд заряды charge
11 электрический заряд электр заряды electrical charge
12 частица бөлшек particle
Слайд 9

Ответьте на вопросы
1.Что означает "атом" в переводе с древнегреческого ?("неделимый"). 2.Опишите строение атома, используя предложенную терминологию на английском и казахском языках.
1.Что означает "атом" в переводе с древнегреческого ?("неделимый"). 2.Опишите строение атома, используя предложенную терминологию на английском и казахском языках.
Слайд 10
Просмотр видео
https://www.youtube.com/watch?v=OCInhp3wHdI
https://www.youtube.com/watch?v=OCInhp3wHdI
Слайд 11

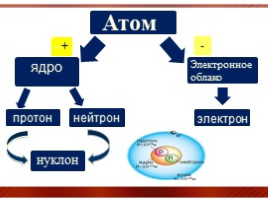
Атом-это электронейтральная система взаимодействия элементарных частиц, состоящая из ядра и электронной оболочки.
XIX в было доказано, что атом делим, что он состоит из более мелких или элементарных частиц.
XIX в было доказано, что атом делим, что он состоит из более мелких или элементарных частиц.
Слайд 12
Слайд 13
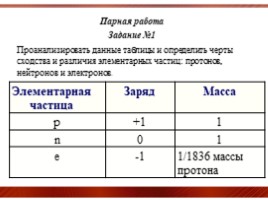
Парная работа Задание №1 Проанализировать данные таблицы и определить черты сходства и различия элементарных частиц: протонов, нейтронов и электронов. Таблица элементарных частиц
Элементарная частица Заряд Масса
p +1 1
n 0 1
e -1 1/1836 массы протона
Слайд 14

Запомните!
Заряд ядра определятся только количеством протонов и
равен атомному номеру элемента и обозначается Z .
Количество электронов равно количеству протонов.
Общее число нуклонов в ядре называется массовым числом и обозначается А
Количество нейтронов можно узнать по разности между массой атома количеством протонов (N=A-Z).
Слайд 15

Состав атома углерода.
Z=+6
P+= 6
e−=6
N=A-Z
N=12-6=6
Слайд 16
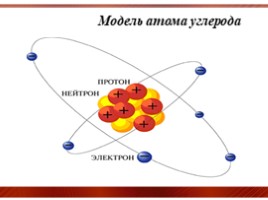
Модель атома углерода
Слайд 17

Задание №2
Подпишите под рисунками химические знаки и названия частиц.
химический знак- ____________ . ____________
1.химический знак- _______________ ______________ 4. ______________
химический знак- ____________ . ____________
1.химический знак- _______________ ______________ 4. ______________
Слайд 18

Задание №2
Подпишите под рисунками химические знаки и названия частиц.
химический знак-Н - электрон. -протон
1.химический знак- -электрон - протон 4. -нейтрон
химический знак-Н - электрон. -протон
1.химический знак- -электрон - протон 4. -нейтрон
Слайд 19

Групповая работа
Прием «Карусель»
Слайд 20
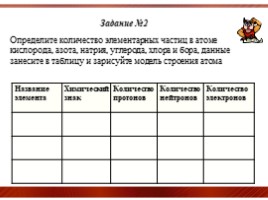
Задание №2
Определите количество элементарных частиц в атоме кислорода, азота, натрия, углерода, хлора и бора, данные занесите в таблицу и зарисуйте модель строения атома
Название элемента Химический знак Количество протонов Количество нейтронов Количество электронов
Определите количество элементарных частиц в атоме кислорода, азота, натрия, углерода, хлора и бора, данные занесите в таблицу и зарисуйте модель строения атома
Название элемента Химический знак Количество протонов Количество нейтронов Количество электронов
Слайд 21

Отгадайте, о какой элементарной частице идет речь?
1) Очень положительный С массою внушительной, А таких, как он, отряд Создает в ядре заряд. Лучший друг его – нейтрон. Догадались? Он-….!
2) Зарядом я похвастать не могу, А потому сижу в ядре и ни гу-гу. А то еще подумают: шпион, А я нейтральный и зовусь…!
3) Он бежит по проводам, Он бывает тут и там, Свет зажег, нагрел утюг …. – наш лучший друг. Если в атом он попал – То считай почти пропал: Он с утра и до утра Носится вокруг ядра.
Разминка
Разминка
Слайд 22

1.Какие частицы определяют заряд ядра? А. Нейтроны В. Электроны С. Протоны D. Нуклоны
Тест У вас на столах лежат жетоны разных цветов с буквами (A,B,C, D) По команде поднимите карточку с буквой соответствующей правильному ответу.
Слайд 23

1.Какие частицы определяют заряд ядра? А. Нейтроны В. Электроны С. Протоны D. Нуклоны
Тест У вас на столах лежат жетоны разных цветов с буквами (A,B,C, D) По команде поднимите карточку с буквой соответствующей правильному ответу.
Слайд 24

2.Заряд ядра:
А. отрицательный В. положительный
С. частичный D.нейтральный
Слайд 25

2.Заряд ядра:
А. отрицательный В. положительный
С. частичный D.нейтральный
Слайд 26

3.Атомный номер элемента соответствует:
А.числу нейтронов В. атомной массе
С.числу протонов D.числу протонов и электронов
Слайд 27

3.Атомный номер элемента соответствует:
А.числу нейтронов В. атомной массе
С.числу протонов D.числу протонов и электронов
Слайд 28

4.Какие субатомные частицы входят в состав ядра?
А. Электрон С. Электрон и протон
В. Электрон и нейтрон D. Протон и нейтрон
Слайд 29

4.Какие субатомные частицы входят в состав ядра?
А. Электрон С. Электрон и протон
В. Электрон и нейтрон D. Протон и нейтрон
Слайд 30

5.Какие субатомные частицы находятся в составе атома вне ядра?
А. Нейтроны В. Протоны
С. Электроны D. Нуклоны
Слайд 31

5.Какие субатомные частицы находятся в составе атома вне ядра?
А. Нейтроны В. Протоны
С. Электроны D. Нуклоны
Слайд 32

6.Атом является электронейтральной частицей, так как:
А.Число протонов равно числу нейтронов
В. Число электронов и протонов равны друг другу
С. Число нейтронов и электронов равны
D. Атом является заряженной частицей
Слайд 33

6.Атом является элнектронейтральной частицей, так как:
А.Число протонов равно числу нейтронов
В. Число электронов и протонов равны друг другу
С. Число нейтронов и электронов равны
D. Атом является заряженной частицей
Слайд 34

7. Массой каких частиц определяется масса атома?
А. Электронов В. Электронов и нейтронов
С. Электронов и протонов D. Протонов и нейтронов
Слайд 35

7. Массой каких частиц определяется масса атома?
А. Электронов В. Электронов и нейтронов
С. Электронов и протонов D. Протонов и нейтронов
Слайд 36

8. Как определяется число нейтронов в атоме?
А. Равно числу протонов
В. Равно числу электронов
С. Разность между массовым номером и числом протонов
D. Разность между атомной массой и числом электронов
Слайд 37

8. Как определяется число нейтронов в атоме?
А. Равно числу протонов
В. Равно числу электронов
С. Разность между массовым номером и числом протонов
D. Разность между атомной массой и числом электронов
Слайд 38

9. Условный заряд одного протона равен:
А. +1 В. – 1 С. 0 D. +2
Слайд 39

9. Условный заряд одного протона равен:
А. +1 В. – 1 С. 0 D. +2
Слайд 40

10. Условный заряд одного электрона равен:
А. +1 В. – 1 С. 0 D. +2
Слайд 41

10. Условный заряд одного электрона равен:
А. +1 В. – 1 С. 0 D. +2
Слайд 42

Рефлексия
Представьте, что наш класс – это атом. Вы являетесь элементарными частицами. Как Вы оцениваете свою работу? Для этого у вас на столах лежат жетоны разных цветов. Красный жетон ( протоны) – это значит, что я понял(а) все хорошо, могу объяснить другому. Зеленый жетон ( нейтроны) –по данной теме у меня есть вопросы. Синий жетон(электроны) – недостаточно понял(а) эту тему. Итак вопрос, как вы оцениваете свою работу?
Представьте, что наш класс – это атом. Вы являетесь элементарными частицами. Как Вы оцениваете свою работу? Для этого у вас на столах лежат жетоны разных цветов. Красный жетон ( протоны) – это значит, что я понял(а) все хорошо, могу объяснить другому. Зеленый жетон ( нейтроны) –по данной теме у меня есть вопросы. Синий жетон(электроны) – недостаточно понял(а) эту тему. Итак вопрос, как вы оцениваете свою работу?
Слайд 43

Все в наших руках
Рефлексия «Ладонь»
1.Знаю названия субатомных частиц атома, структуру расположения и их заряд.
2.Знаю что атомный номер совпадает числами протонов и электронов.
3.Умею находить число нейтронов использовав атомный номер и массовый номер.
4.Могу определить атомное и массовое число с помощью субатомных частиц каждого элемента.
5.Могу определить число субатомных частиц используя полное описание ядра.
Слайд 44

Задание на дом
Учащиеся выбирают один уровень по своему желанию Уровень А (средний) изготовить модель строения атома одного из 20 первых элементов Уровень В (творческий) изготовить 2 модели строения атома одного из 20 первых элементов
Уровень С (креативный) создать видео о модели строения атома одного из 20 первых элементов
Учащиеся выбирают один уровень по своему желанию Уровень А (средний) изготовить модель строения атома одного из 20 первых элементов Уровень В (творческий) изготовить 2 модели строения атома одного из 20 первых элементов
Уровень С (креативный) создать видео о модели строения атома одного из 20 первых элементов
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
