Презентация - Классификация белков
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 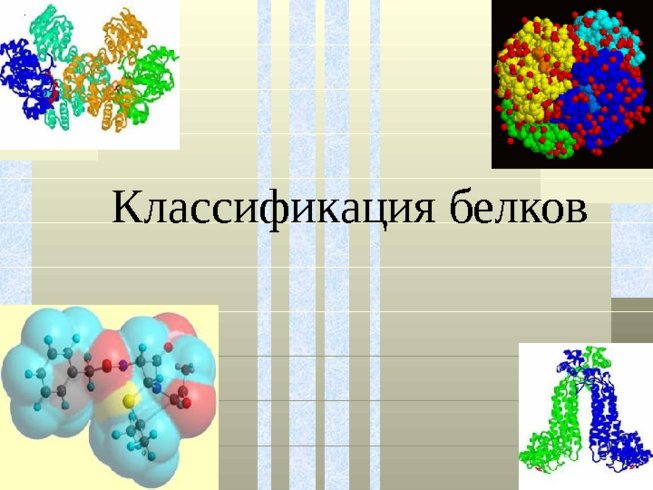
|
Распечатать
- Уникальность: 95%
- Слайдов: 83
- Просмотров: 5612
- Скачиваний: 2211
- Размер: 7.47 MB
- Онлайн: Да
- Формат: ppt / pptx
Примеры похожих презентаций
 Классификация технологий
Классификация технологий Опасные и чрезвычайные ситуации: классификация, общие понятия и определения
Опасные и чрезвычайные ситуации: классификация, общие понятия и определения Биосинтез белка - Функции белков
Биосинтез белка - Функции белков Наркомания и наркотические вещества - Их действие на человека и классификация
Наркомания и наркотические вещества - Их действие на человека и классификация Трасология основные понятия классификация следов
Трасология основные понятия классификация следов Соли их классификация и свойства
Соли их классификация и свойства Классификация углеводородов
Классификация углеводородов
Слайды и текст этой онлайн презентации
Слайд 1
Классификация белков
Слайд 2

По химическому составу
различают простые белки, сложные белки.
Слайд 3

Классификация простых белков альбумины, глобулины, гистоны, протамины, протеиноиды.
Слайд 4

Альбумины глобулярные белки, молекулярная масса 70 000, растворимы в воде, ИЭТ 5, высаливаются 100% сульфатом аммония, синтез в печени.
Слайд 5

Функции альбуминов депо белка в организме, осморегуляция, неспецифическая защита, транспорт лекарств, металлов, холестерина, билирубина, желчных пигментов, гормонов.
Слайд 6

Глобулины глобулярные белки, молекулярная масса 150 000 дальтон, растворимы в солевых растворах, ИЭТ 7, имеют ряд фракций, высаливаются 50% сульфатом аммония, синтезируются в печени и В-лимфоцитах .
Слайд 7

Функции глобулинов ферменты, транспорт витаминов, гормонов, металлов, защита (иммунитет), γ -глобулины являются антителами.
Слайд 8
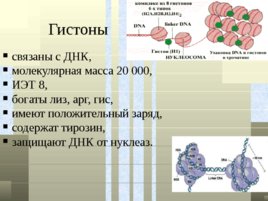
Гистоны связаны с ДНК, молекулярная масса 20 000, ИЭТ 8, богаты лиз, арг, гис, имеют положительный заряд, содержат тирозин, защищают ДНК от нуклеаз.
Слайд 9
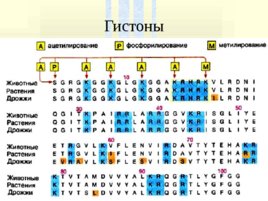
Гистоны
Слайд 10

Протамины молекулярная масса 5000, ИЭТ 11, содержат много арг, лиз, имеют положительный заряд, не содержат тирозин, являются белковым компонентом нуклеопротеинов.
Слайд 11

Проламины и глютелины белки растительного происхождения, содержатся в семенах злаков, растворимы в 60-80% водном растворе, а другие простые белки выпадают в осадок, проламины содержат 20-25% глу и 10-15% пролина.
Слайд 12
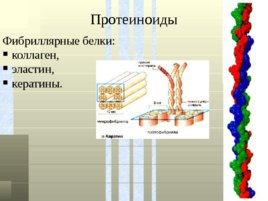
Протеиноиды Фибриллярные белки: коллаген, эластин, кератины.
Слайд 13

Коллаген Треть общего белка организма приходится на коллаген – основной белок соединительной ткани. молекулярная масса коллагена 300 000, Содержится в: коже, роговице, костях.
Слайд 14
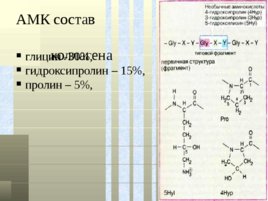
АМК состав коллагена глицин -30%, гидроксипролин – 15%, пролин – 5%,
Слайд 15

Строение коллагена молекула коллагена состоит из 3 пептидных цепей, в каждой примерно 1000 АМК, вторичная структура коллагена – 3 спирали перевиты друг с другом, образуя плотный жгут (тропоколлаген), все 3 цепи параллельны, то есть на одном конце коллагена N -концы цепей, а на другом С-концы. Молекулы коллагена, соединяясь, образуют микрофибриллы, из них образуются пучки волокон. Тройная спираль коллагена стабилизируется межцепочечными сшивками между лизиновыми и гидроксилизиновыми остатками. Гидроксипролин стабилизирует тройную спираль коллагена по отношению к действию протеиназ и действию протеолитических ферментов.
Слайд 16
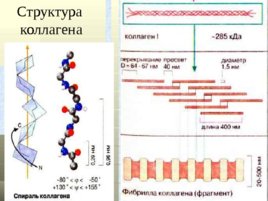
Структура
коллагена
Слайд 17

Уникальная особенность метаболизма гидроксипролина эта АМК, входящая в состав белков пищи, не включается в коллаген, пищевой пролин является предшественником гидроксипролина в составе коллагена. На каждый моль гидроксилированного пролина декарбоксилируется 1 моль α -кетоглутарата с образованием сукцината. В результате реакции один атом кислорода поступает в сукцинат, а другой в пролин.
Слайд 18

Известно 19 типов коллагена. Определённую роль в синтезе коллагена играют белки-шапероны, обеспечивающие «контроль качества» коллагена. Ряд заболеваний связан с нарушением синтеза коллагена. Основная причина - мутации.
Слайд 19

Заболевания, связанные с нарушением синтеза коллагена
несовершенный остеогенез, хондродисплазии, семейная аневризма аорты.
Слайд 20

По мере старения фибриллы коллагена становятся более жёсткими и хрупкими, меняются свойства хрящей, сухожилий, роговицы.
Слайд 21

Эластин гликопротеин с множеством гидрофобных АМК, сеть полипептидных цепей, поперечно-связанных остатками десмозина, фибриллы эластина хорошо растягиваются, эластичность возникает за счёт наличия гибкой случайной конформации молекул эластина и большого количества эластичных сшивок, молекулярная масса 72 000 дальтон, основной структурный компонент эластических волокон, входит в состав кровеносных сосудов, связок, артерий.
Слайд 22

α -кератины образуют волосы, шерсть, перья, рога, когти, чешую, наружный слой кожи.
Слайд 23
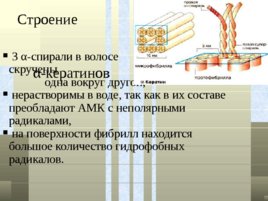
Строение α -кератинов 3 α -спирали в волосе скручены одна вокруг другой, нерастворимы в воде, так как в их составе преобладают АМК с неполярными радикалами, на поверхности фибрилл находится большое количество гидрофобных радикалов.
Слайд 24
.
Слайд 25

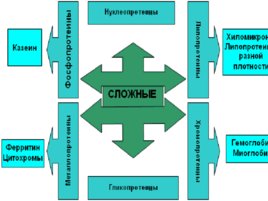
Сложные белки помимо белковой части содержат небелковый компонент.
хромопротеины состоят из простого белка и связанного с ним окрашенного компонента, гемопротеины: железосодержащие - красные, магнийсодержащие -зелёные, медьсодержащие – голубые, жёлтые флавопротеины.
Слайд 26
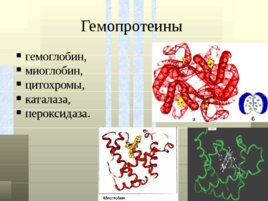
Гемопротеины гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза.
Слайд 27
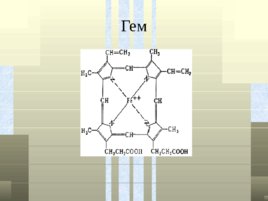
Гем
Слайд 28
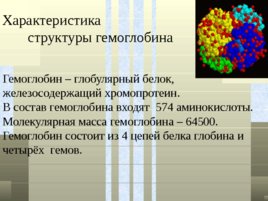
Характеристика структуры гемоглобина Гемоглобин – глобулярный белок, железосодержащий хромопротеин. В состав гемоглобина входят 574 аминокислоты. Молекулярная масса гемоглобина – 64500. Гемоглобин состоит из 4 цепей белка глобина и четырёх гемов.
Слайд 29
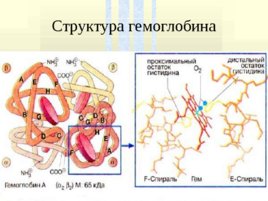
Структура гемоглобина
Слайд 30
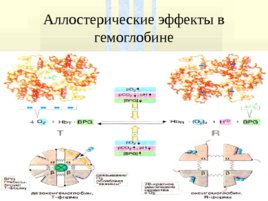
Аллостерические эффекты в гемоглобине
Слайд 31

Гем Гем - это соединение циклического тетрапиррола – порфирина с железом. Атом железа имеет 6 связей: четыре – с атомами азота пиррольных колец, пятая – с гистидином, шестая – для связывания с кислородом.
Слайд 32

Глобин - белок типа альбуминов синтезируется в нормобластах состоит из четырёх полипептидных цепей: 2α -цепи по 141 АМК, 2β -цепи по 146 АМК. содержит много гистидина. Первичная структура – последовательность АМК, соединённых пептидной связью. Вторичная структура – α -спираль. Спирализованные неподвижные участки (70%) прерываются подвижными неспирализованными. Третичная структура – глобулярный белок. Четвертичная структура – белок состоит из 4х полипептидных цепей, уложенных относительно друг друга. С каждой цепью связан один гем.
Слайд 33

Миоглобин находится в красных мышцах, участвует в запасании кислорода, молекулярная масса 17 000, включает 153 АМК, α -спираль уложена в глобулу.
Слайд 34
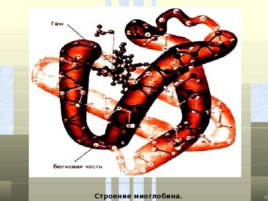
Строение миоглобина.
Слайд 35
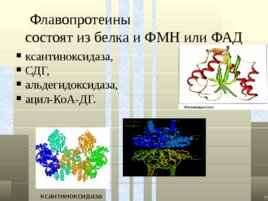
Флавопротеины состоят из белка и ФМН или ФАД ксантиноксидаза, СДГ, альдегидоксидаза, ацил-Ко А-ДГ. ксантиноксидаза
Слайд 36
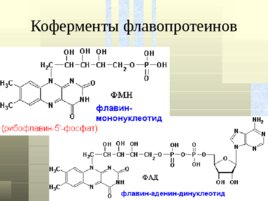
Коферменты флавопротеинов
Слайд 37

Металлопротеины Белки содержащие негеминовое железо ферритин – депо железа в организме, в составе этого белка находится 20% железа организма, образуется в печени и селезёнке, трансферрин.
Слайд 38

Белки-ферменты - металлопротеины С u -содержащие: цитохромоксидаза, церулоплазмин, тирозиназа, Mn- содержащие: аргиназа, Zn -содержащие: карбоангидраза, алкоголь ДГ.
Слайд 39

Фосфопротеины состоят из белка и фосфорной кислоты, фосфорная кислота присоединяется через ОН-группу серина.
Слайд 40

Фосфопротеины казеиноген в молоке, овальбумин и фосвитин в яйцах, ихтулин в икре рыбы, в большом количестве содержатся в клетках ЦНС.
Слайд 41

Биологическая роль фосфопротеинов входят в состав мозга, в растущем организме фосфор – пластический материал, способны отдавать фосфорную кислоту для макроэргов и ферментов.
Слайд 42
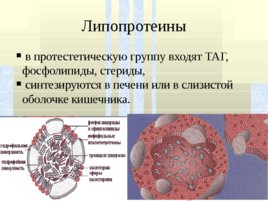
Липопротеины в протестетическую группу входят ТАГ, фосфолипиды, стериды, синтезируются в печени или в слизистой оболочке кишечника.
Слайд 43

Биологическая роль
липопротеинов входят в состав плазматических мембран (20-80%), содержатся в нервной ткани, находятся в плазме крови ХМ, ЛПНП, ЛПВП, ЛПОНП.
Слайд 44

Гликопротеины (гликоконъюгаты) белки, содержащие олигосахаридные цепи, ковалентно присоединённые к полипептидной основе, углеводные компоненты ковалентно соединены с азотом аспарагина молекулы белка, при развитии ряда болезней (рак, астма, иммунодефицит, ревматоидный артрит) изменяются структуры гликоконъюгатов.
Слайд 45

Углеводный компонент галактоза, глюкоза, манноза, N -ацетилгалактозамин, N -ацетилглюкозамин, N -ацетилненйраминовая кислота, фукоза.
Слайд 46

Функции гликопротеинов структурная (находятся в плазматических мембранах), смазочная и защитная (муцины, слизь), транспорт витаминов, липидов, микроэлементов (все белки плазмы крови, кроме альбуминов, гликопротеины), иммунологическая (иммуноглобулины, антигены гистосовместимости, комплемент, интерферон), гормоны (хорионический гонадотропин, ТТГ), ферменты (протеазы, нуклеазы, гликозидазы, гидролазы, факторы свёртывания), места клеточных контактов распознавания, гормональные рецепторы, лектины влияют на эмбриональное развитие и дифференцировку, могут влиять на выбор мест метастазирования раковых клеток.
Слайд 47
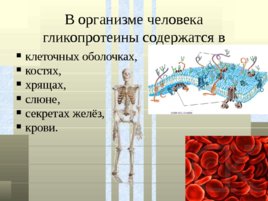
В организме человека гликопротеины содержатся в клеточных оболочках, костях, хрящах, слюне, секретах желёз, крови.
Слайд 48

Интерфероны образуются в клетке в ответ на внедрение вирусной НК, ограничивая вирусную агрессию, сложные белки, молекулярная масса от 25 000 до 40 000.
Слайд 49
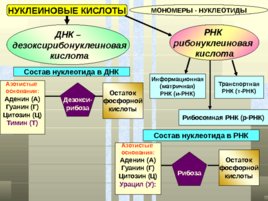
НУКЛЕИНОВЫЕ КИСЛОТЫ МОНОМЕРЫ - НУКЛЕОТИДЫ ДНК – дезоксирибонуклеиновая кислота РНК рибонуклеиновая кислота Состав нуклеотида в ДНК Состав нуклеотида в РНК Азотистые основания: Аденин (А) Гуанин (Г) Цитозин (Ц) Урацил (У): Рибоза Остаток фосфорной кислоты Азотистые основания: Аденин (А) Гуанин (Г) Цитозин (Ц) Тимин (Т) Дезокси- рибоза Остаток фосфорной кислоты Информационная (матричная) РНК (и-РНК) Транспортная РНК (т-РНК) Рибосомная РНК (р-РНК)
Слайд 50
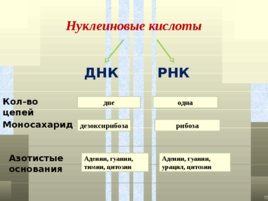
Нуклеиновые кислоты ДНК РНК Моносахарид дезоксирибоза рибоза Азотистые основания Аденин, гуанин, тимин, цитозин Аденин, гуанин, урацил, цитозин Кол-во цепей две одна
Слайд 51

Нуклеопротеины
состоят из белка и нуклеиновой кислоты белок – гистоны, протамины, НК – ДНК, РНК – полинуклеотиды, состоящие из мононуклеотидов.
Слайд 52
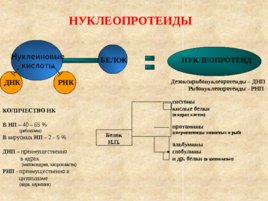
гистоны кислые белки (в ядрах клеток) протамины (сперматозоиды животных и рыб) альбумины глобулины и др. белки (в цитоплазме) Белок Н. П. КОЛИЧЕСТВО НК В НП – 40 – 65 % (рибосомы) В вирусных НП – 2 - 5 % ДНП – преимущественно в ядрах (митохондрии, хлоропласты) РНП - преимущественно в цитоплазме (ядра, ядрышки) Нуклеиновые кислоты ДНК РНК БЕЛОК НУКЛЕОПРОТЕИД Дезоксирибонуклеоротеиды – ДНП Рибонуклеопротеиды - РНП НУКЛЕОПРОТЕИДЫ
Слайд 53
Значение нуклеотидов синтез НК, энергетическая роль, коферменты, транспортная функция.
Слайд 54
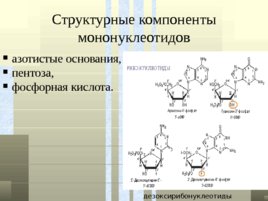
Структурные компоненты мононуклеотидов азотистые основания, пентоза, фосфорная кислота. дезоксирибонуклеотиды
Слайд 55
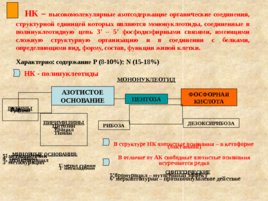
НК – высокомолекулярные азотсодержащие органические соединения, структурной единицей которых являются мононуклеотиды, соединенные в полинуклеотидную цепь 3 – 5 фосфодиэфирными связями, имеющими сложную структурную организацию и в соединении с белками, определяющими вид, форму, состав, функции живой клетки. Характерно: содержание Р (8-10%); N (15-18%) НК - полинуклеотиды МОНОНУКЛЕОТИД ФОСФОРНАЯ КИСЛОТА АЗОТИСТОЕ ОСНОВАНИЕ ПУРИНЫ Аденин Гуанин ПИРИМИДИНЫ Цитозин Урацил Тимин ПЕНТОЗА РИБОЗА ДЕЗОКСИРИБОЗА В структуре НК азотистые основания – в кетоформе (лактамной) МИНОРНЫЕ ОСНОВАНИЯ: 5 метилцитозин 4 тиоурацил дегидроурацил 3 метилурацил 1 метил гуанин 1 метиладенин В отличие от АК свободные азотистые основания встречаются редко СИНТЕТИЧЕСКИЕ 5 бромурацил – мутагенный эффект 6 меркаптопурин – противоопухолевое действие
Слайд 56
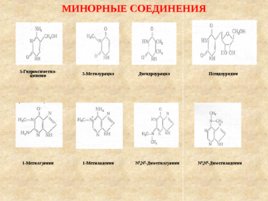
МИНОРНЫЕ СОЕДИНЕНИЯ 5-Гидроксиметил- цитозин Дигидроурацил 3-Метилурацил Псевдоуридин 1-Метилгуанин 1-Метиладенин N 2 ,N 2 - Диметилгуанин N 6 , N 6 - Диметиладенин
Слайд 57
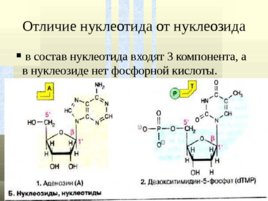
Отличие нуклеотида от нуклеозида в состав нуклеотида входят 3 компонента, а в нуклеозиде нет фосфорной кислоты.
Слайд 58
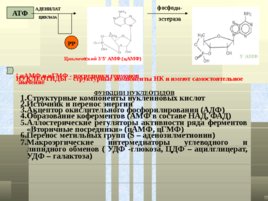
ФУНКЦИИ НУКЛЕОТИДОВ Структурные компоненты нуклеиновых кислот Источник и перенос энергии Акцептор окислительного фосфорилирования (АДФ) Образование коферментов (АМФ в составе НАД, ФАД) Аллостерические регуляторы активности ряда ферментов «Вторичные посредники» (ц АМФ, ц ГМФ) Перенос метильных групп ( S – аденозилметионин) Макроэргические интермедиаторы углеводного и липидного обменов ( УДФ -глюкоза, ЦДФ – ацилглицерат, УДФ – галактоза) ! ц АМФ и ц ГМФ - посредники гормонов НУКЛЕОТИДЫ – структурные компоненты НК и имеют самостоятельное значение АТФ АДЕНИЛАТ ЦИКЛАЗА РР фосфоди- эстераза Циклический 3 5 АМФ (ц АМФ) 5 АМФ
Слайд 59
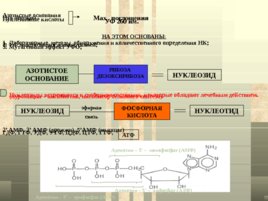
Азотистые основания Нуклеотиды Нуклеиновые кислоты Мах . поглощения УФ 260 нм. НА ЭТОМ ОСНОВАНЫ: Лабораторные методы обнаружения и количественного определения НК; УФ микроскопия живых тканей; Мутагенный эффект УФО; АЗОТИСТОЕ ОСНОВАНИЕ РИБОЗА ДЕЗОКСИРИБОЗА НУКЛЕОЗИД Нуклеозиды встречаются в свободном состоянии, некоторые обладают лечебным действием. (пуромицин – антибиотик, ингибитор белкового синтеза) НУКЛЕОЗИД ФОСФОРНАЯ КИСЛОТА НУКЛЕОТИД эфирная связь 2 АМФ, 3 АМФ ( дрожжи), 5 АМФ (мышцы) ГДФ, ГТФ, УДФ, УТФ, ЦДФ, ЦТФ, ТТФ, АТФ Аденозин – 5 – трифосфат (АТФ) Аденозин – 5 – монофосфат (АМФ) Аденозин – 5 – дифосфат (АДФ)
Слайд 60
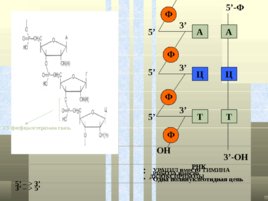
РНК УРАЦИЛ вместо ТИМИНА РИБОЗА вместо ДЕЗОКСИРИБОЗЫ Одна полинуклеотидная цепь 5 – 3 3 – 5 3 5 фосфодиэстеразная связь 3 -OH 5 - Ф А Т Ц Ц А Т OH 5 5 5 3 3 3 Ф Ф Ф Ф
Слайд 61

Правила Чаргаффа молярная доля пуринов равна молярной доле пиримидинов А Г Ц Т, количество аденина и цитозина равно количеству гуанина и тимина А Ц Т Г, количество аденина равно количеству тимина, количество гуанина равно количеству цитозина А Т, Г Ц, существенным для характеристики вида является коэффициент специфичности. У человека К 1.
Слайд 62

Комплементарность - это способность нуклеотидов к избирательному соединению в пары
Слайд 63
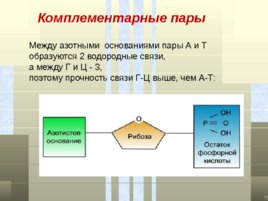
Между азотными основаниями пары А и Т образуются 2 водородные связи, а между Г и Ц - 3, поэтому прочность связи Г-Ц выше, чем А-Т: Комплементарные пары
Слайд 64
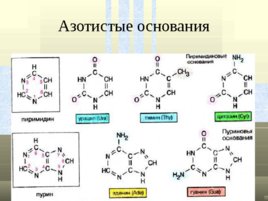
Азотистые основания
Слайд 65
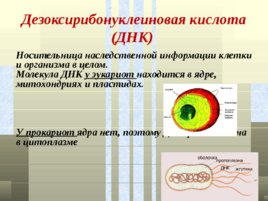
Дезоксирибонуклеиновая кислота (ДНК) Носительница наследственной информации клетки и организма в целом. Молекула ДНК у эукариот находится в ядре, митохондриях и пластидах. У прокариот ядра нет, поэтому ДНК расположена в цитоплазме
Слайд 66
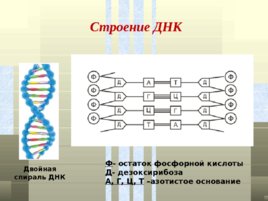
Строение ДНК Ф - остаток фосфорной кислоты Д - дезоксирибоза А, Г, Ц, Т –азотистое основание Двойная спираль ДНК
Слайд 67

Рибонуклеиновая кислота (РНК) Молекулы РНК находятся в цитоплазме, ядре и некоторых органоидах клетки. Типы РНК и РНК р РНК т РНК Содержат информацию о первичной структуре белка Переносят аминокислоты к месту синтеза белка Содержатся в рибосомах Участвуют в синтезе белка
Слайд 68
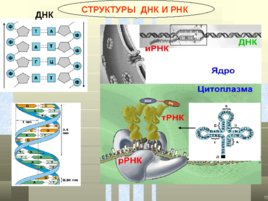
СТРУКТУРЫ ДНК И РНК ДНК
Слайд 69
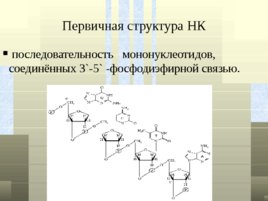
Первичная структура НК последовательность мононуклеотидов, соединённых 3 -5 -фосфодиэфирной связью.
Слайд 70
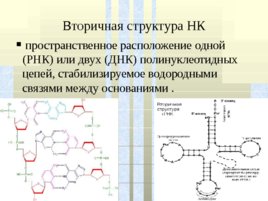
Вторичная структура НК пространственное расположение одной (РНК) или двух (ДНК) полинуклеотидных цепей, стабилизируемое водородными связями между основаниями .
Слайд 71

ВТОРИЧНАЯ СТРУКТУРА ДНК ПРАВИЛА ЧАРГАФА (1949) А Т Молярная доля ПУРИНОВ молярной доле ПИРИМИДИНОВ А Г Ц Т или 1 Содержание А содержанию Т (А Т, А / Т 1) Содержание Г содержанию Ц (Г Ц, Г / Ц 1) Изменчива только сумма А Т; Г Ц А Г Ц Т Г Ц - КОЭФФИЦИЕНТ СПЕЦИФИЧНОСТИ Модель -формы ДНК Спираль Уотсона – Крика (1952 ) 2 1 1 Малая бороздка 2 Большая бороздка
Слайд 72
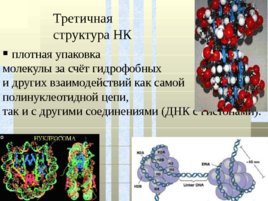
Третичная
структура НК плотная упаковка молекулы за счёт гидрофобных и других взаимодействий как самой полинуклеотидной цепи, так и с другими соединениями (ДНК с гистонами).
Слайд 73

ТРЕТИЧНАЯ СТРУКТУРА ДНК - СУПЕРСПИРАЛЬ СТРУКТУРНАЯ ОРГАНИЗАЦИЯ ДНК В ХРОМОСОМАХ В каждой хромосоме – одна гигантская молекула ДНК (1 10 ) ХРОМАТИН – надмолекулярная структура (ДНК белок РНК неорганические вещества) 11 КОМПОНЕНТ СОДЕРЖАНИЕ ДНК 30-35% ГИСТОНЫ 30-50% Негистоновые БЕЛКИ 4-33% РНК 1,5-10% Соотношение компонентов хроматина: Структурная организация хроматина позволяет использовать одну и ту же генетическую информацию ДНК, присущую данному организму, по-разному в специализированных клетках.
Слайд 74

БИОЛОГИЧЕСКАЯ РОЛЬ ДНК - Хранение наследственной информации Функциональная единица ДНК - ГЕН ГЕН – определенная последовательность нуклеотидов (500-2000 н.е.), с помощью которой закодирован определенный признак. СТРУКТУРНЫЙ ГЕН – закодирован признак РЕГУЛЯТОРНЫЙ ГЕН: ген оператор (ГО) ген регулятор (ГР) О П Е Р О Н ОПЕРОН – функциональная надструктура генетического аппарата КОДИРОВАНИЕ ИНФОРМАЦИИ ДНК Сколько признаков – столько оперонов Для кодирования всех признаков достаточно 2% ДНК, 98% - молчащая ДНК Кодон триплет 3 нуклеотида – буква генетического алфавита 4 64 кодона 3 ГЕНЕТИЧЕСКИЙ КОД Триплетен Универсален Вырожден АЛА – 3, ЛЕЙ – 6 Неперекрываем ЦЦА, ГАГ, ТЦГ ЦЦА, ГАГ, ТЦГ
Слайд 75

ТЕХНИКА РЕКОМБИНАНТНЫХ ДНК (ГЕННАЯ ИНЖЕНЕРИЯ) ! ЭНДОНУКЛЕАЗЫ РЕСТРИКЦИИ – РЕСТРИКТАЗЫ ГЕННАЯ ИНЖЕНЕРИЯ – направление молекулярной биологии по разработке методов конструирования нужных генов, внедрения их в клетку – хозяина с целью изменения ее генетических свойств. (1972) ПРИНЦИПИАЛЬНАЯ СХЕМА ПРОВЕДЕНИЯ РАБОТ ПО ГЕННОЙ ИНЖЕНЕРИИ рестриктазы расщепление Включение фрагмента чужеродной ДНК в плазмидную ДНК Проникновение плазмиды в бактериальную клетку хозяина Плазмидная ДНК Размножение бактерий
Слайд 76
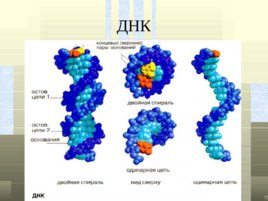
ДНК
Слайд 77

РНК, ВИДЫ, СТРУКТУРА И ФУНКЦИИ . РНК – одинарная полинуклеотидная цепочка м РНК. Mr – дес. тысяч – млн. нуклеотидов. 2-10% всей РНК, перенос информации от ДНК в цитозоль к рибосомам транскрипция АТГЦЦГ ТАЦГГЦ ДНК АУГЦЦГ РНК Первичная структура – полинуклеотид Вторичная структура – изогнутая полинуклеотидная цепь Третичная структура – полинуклеотидная нить «намотанная на катушку» - белок информофер (транспортный белок) р РНК Mr – млн., 80% всей РНК, СКЕЛЕТ рибосомы, образование полисом ВТОРИЧНАЯ СТРУКТУРА – спирализованные участки, соединенные изогнутой одно-цепочечной нитью нуклеотидов. ТРЕТИЧНАЯ – скелет рибосомы (палочка или клубок) на него «нанизываются» белки рибосом- ПОЛИСОМА. т РНК Mr – 20 тыс. (75 нуклеотидов) Активация и транспорт АК и рибосом для сборки полипептида ВТОРИЧНАЯ СТРУКТУРА – «лист клевера» образуется путем внутрецепочечного взаимодействия комплементарных нуклеотидов. ТРЕТИЧНАЯ СТРУКТУРА – имеет форму локтевого сгиба, образуется в трехмерном пространстве путем наложения петель на тело молекулы.
Слайд 78

МОДЕЛИ ВТОРИЧНОЙ И ТРЕТИЧНОЙ СТРУКТУРЫ РНК ВТОРИЧНАЯ СТРУКТУРА т РНК ТРЕТИЧНАЯ СТРУКТУРА т РНК АНТИКОДОН ДОБ. ПЕТЛЯ АКЦЕПТОРНЫЙ КОНЕЦ АНТИКОДОНОВАЯ ПЕТЛЯ D -ПЕТЛЯ T - ПЕТЛЯ
Слайд 79
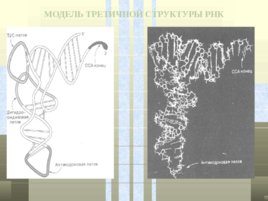
МОДЕЛЬ ТРЕТИЧНОЙ СТРУКТУРЫ РНК
Слайд 80
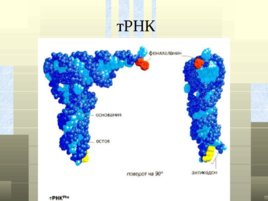
т РНК
Слайд 81

Сравнительная характеристика ДНК и РНК ДНК Биологический полимер Мономер – нуклеотид 4 типа азотистых оснований : аденин, тимин, гуанин, цитозин. Комплементарные пары: аденин-тимин, гуанин-цитозин Местонахождение - ядро Функции – хранение наследственной информации Сахар - дезоксирибоза РНК Биологический полимер Мономер – нуклеотид 4 типа азотистых оснований : аденин, гуанин, цитозин, урацил Комплементарные пары: аденин-урацил, гуанин-цитозин Местонахождение – ядро, цитоплазма Функции –перенос, передача наследственной информации. Сахар - рибоза
Слайд 82
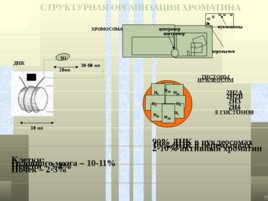
90% ДНК в нуклеосомах 10% ДНК в перемычках 2-10% активный хроматин Клетки: Головного мозга – 10-11% Печени – 3-4% Почек – 2-3% СТРУКТУРНАЯ ОРГАНИЗАЦИЯ ХРОМАТИНА Н1 20нп 10 нп 30-60 нп ДНК центромер ХРОМОСОМА нуклеосомы перемычки центромер 2Н2А 2Н2В 2Н3 2Н4 8 ГИСТОНОВ Н 2 b Н 3 Н 2 a Н 2 Н 2 a Н 2 Н 2 b Н 3 ГИСТОНЫ НУКЛЕОСОМ
Слайд 83
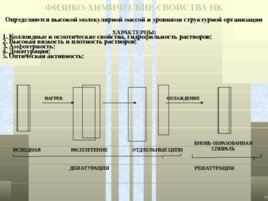
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА НК Определяются высокой молекулярной массой и уровнями структурной организации ХАРАКТЕРНЫ: Коллоидные и осмотические свойства, гидрофильность растворов; Высокая вязкость и плотность растворов; Амфотерность; Денатурация; Оптическая активность; НАГРЕВ ОХЛАЖДЕНИЕ ИСХОДНАЯ РАСПЛЕТЕНИЕ ОТДЛЕЛЬНЫЕ ЦЕПИ ВНОВЬ ОБРАЗОВАННАЯ СПИРАЛЬ ДЕНАТУРАЦИЯ РЕНАТУРАЦИЯ
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
