Презентация - Aminokislotalar. Oqsillar.
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 82%
- Слайдов: 32
- Просмотров: 9711
- Скачиваний: 2854
- Размер: 0.56 MB
- Онлайн: Да
- Формат: ppt / pptx
Слайды и текст этой онлайн презентации
Слайд 1

Aminokislotalar. Oqsillar.
Слайд 2

Слайд 3

Aminokislotalar. Oqsillar. Reja: 1. Aminokislotalar. Aminokislotalarning tuzilishi, izomeriyasi (α, β, γ - aminokislotalar). 2. Aminokislotalarning xossalari: karboksil guruhiga xos reaksiyalar, α -, β – va γ – aminokislotalarning qizdirishga munosabati. 3. Polipeptidlar. Laktamlar. α – aminokapron kislota. Kaprolaktam. Kapron tola. 4. Oqsillar. Oqsil molekulalarining tuzilishi. Oqsillarning klassifikatsiyasi. Oqsillarning sifat reaksiyalari. Ularning tabiatdagi ahamiyati va sanoatda ishlatilishi.
Слайд 4

Карбоксил ва аминогуруҳи сақловчи органик бирикмаларга аминокислоталар дейилади. Оқсиллар аминокислоталар қолдиғидан ташкил топганлиги сабабли, аминокислоталар жуда катта аҳамиятга эгадирлар. Аминокислоталарнинг гомологик қатори аминосирка кислотадан бошланади. Аминочумоли кислота мавжуд эмас. Аминокислоталар ни номлашда эмперик ва систематик номенклатурадан фойдаланилади. Эмперик номенклатура бўйича номлашда аминокислоталар номи тегишли кислота номи олдига амино сўзи қўшиб ҳосил қилинади. Карбоксил ва аминогуруҳларнинг ҳолати -, -, γ- каби ҳ арфлар билан ифодаланилади.
Слайд 5

Aminokislotalar - molekulasi tarkibida ham amino -(NH 2 ) , ham karboksil -(COOH) guruhi bo lgan moddalardir. Oqsillar esa turli xil -amino - kislotalarning qoldiqlaridan tashkil topgan yuqorimolekulyar polipeptid birikmalardir. Oqsillar tirik hayotning asosi bo lib murakkab tuzilishga egadir. Aminokislotalar tarkibidagi 2 ta funksional guruhning bir-biriga nisbatan joylashishiga qarab -, - va -aminokislotalar bo ladi .
Слайд 6

1. α -aminomoy kislota, 2- aminobutan kislota 2. β -aminomoy kislota, 3- aminobutan kislota 3. γ -aminomoy kislota, 4- aminobutan kislota (1) (2) (3)
Слайд 7

Aminokislotalar tarkibida asimmetrik uglerod atomi bo lganligi uchun ularga ham optik izomeriya xosdir. Ular ham qutblangan nurni o ngga ( ) yoki chapga (-) buradi. D va L qatorlarga bo linadi. Oqsil tarkibiga kiruvchi -aminokislotalar o ziga xos nomlarga ega. M-n: NH 2 -CH 2 -COOH glikokol, glitsin
Слайд 8

Aminokislotalar ham aminlar ning, ham karbon kislotalar ning xossalariga ega. Ular odatda, ichki tuz shaklida bo ladi va shuning uchun suvda eruvchan, kristall moddalardir. Oqsillar tarkibiga 20 taga yaqin -amino - kislotalar kiradi. Bu aminokislotalarning bir qismi organizmda sintez bo ladi, bir qismi esa tayyor holda ovqat bilan organizmga kirishi kerak. Organizm uchun zarur bo lgan, ammo organizmda sintez bo lmaydigan -amino - kislotalar almashtirib bo lmaydigan amino - kislotalar deyiladi. Ular quyidagilardir:
Слайд 9
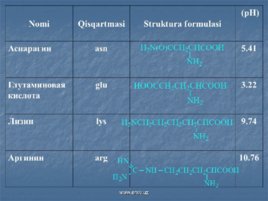
Слайд 10
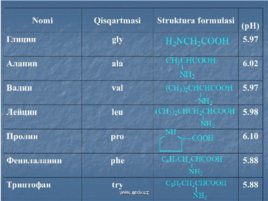
Слайд 11
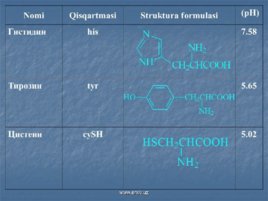
Слайд 12
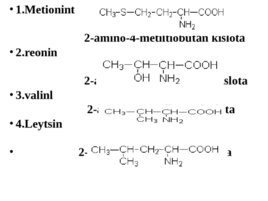
1. Metionint 2-amino-4-metiltiobutan kislota 2. reonin 2-amino-3-gidroksibutan kislota 3. valinl 2-amino-3-metilbutan kislota 4. L eytsin 2-amino-4-metilpentan kislota
Слайд 13
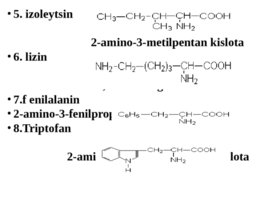
5. izoleytsin 2-amino-3-metilpentan kislota 6. lizin 2,6-diaminogeksan kislota 7.f enilalanin 2-amino-3-fenilpropan kislota 8. Triptofan 2-amino-3-(3-indolil) propan kislota
Слайд 14

Aminokislotalarni olish usullari ham aminobirikmalar va karbon kislotalarni olish usullariga o xshash. M-n: -aminokislotalarni -galogenkislotalardan va aldegidlardan quyidagi reaksiyalar yordamida olish mumkin:
Слайд 15
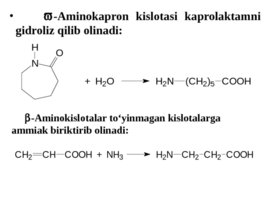
-Aminokapron kislotasi kaprolaktamni gidroliz qilib olinadi: -Aminokislotalar to yinmagan kislotalarga ammiak biriktirib olinadi:
Слайд 16
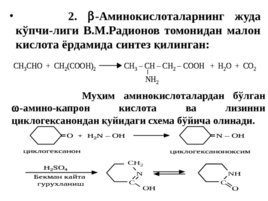
2. -Аминокислоталарнинг жуда кўпчи - лиги В. М. Радионов томонидан малон кислота ёрдамида синтез қилинган: Муҳим аминокислоталардан бўлган -амино - капрон кислота ва лизинни циклогексанондан қуйидаги схема бўйича олинади.
Слайд 17

Капролактам полимерланганда ёки аминокапрон кислота поликонденсатланиш реакциясига учратилганда капрон ҳосил бўлади. Физикавий хоссалари. Аминокислоталар юқори ҳароратда суюқланадиган, сувда яхши эрийдиган рангсиз кристалл моддалардир. Уларнинг суюқланиш ҳароратлари бир-биридан кам фарқ қилади.
Слайд 18

Бир асосли аминокислоталарнинг сувдаги эритмалари нейтрал характерга эга. Аминокислоталар ички туз (биполяр ион) NH 3 – CH 2 COO – кўринишида мавжуд бўладилар. Уларнинг бундай тузилишга эга бўлишлиги физикавий текшириш усуллари ёрдамида аниқланилган. Биполяр ион кислотали муҳитда катион, ишқорий муҳитда эса анион сифатида мавжуд бўлади. Аминокислота эритмалари изоэлектрик нуқтада электр токини ўтазмайди.
Слайд 19
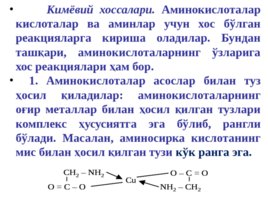
Кимёвий хоссалари. Аминокислоталар кислоталар ва аминлар учун хос бўлган реакцияларга кириша оладилар. Бундан ташқари, аминокислоталарнинг ўзларига хос реакциялари ҳам бор. 1. Аминокислоталар асослар билан туз ҳосил қиладилар: аминокислоталарнинг оғир металлар билан ҳосил қилган тузлари комплекс ҳусусиятга эга бўлиб, рангли бўлади. Масалан, аминосирка кислотанинг мис билан ҳосил қилган тузи кўк ранг а эга.
Слайд 20

2. Кислоталар каби аминокислоталар ҳам мураккаб эфирлар, галоген ангидридлар, амидлар ва бошқаларни ҳосил қиладилар. 3. Аминокислоталар аминогуруҳ ҳисоби - га кислота ҳусусиятига эга бўлган бирикмалар билан туз ҳосил қиладилар:
Слайд 21

4. Аминокислоталарга нитрит кислота билан таъсир этилганда оксикислоталарни ҳосил қиладилар: Аминокислоталарнинг эфирларига нитрит кислота билан таъсир этилганда барқарор диазидбирикмалар ҳосил бўлади:
Слайд 22
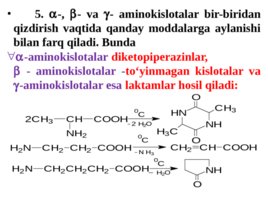
5. -, - va - aminokislotalar bir - biridan qizdirish vaqtida qanday moddalarga aylanishi bilan farq qiladi . Bunda -aminokislotalar diketopiperazinlar , - aminokislotalar - to yinmagan kislotalar va -aminokislotalar esa laktamlar hosil qiladi:
Слайд 23
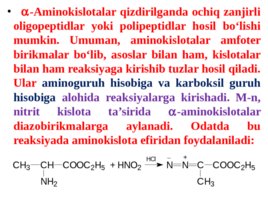
-Aminokislotalar qizdirilganda ochiq zanjirli oligopeptidlar yoki polipeptidlar hosil bo lishi mumkin. Umuman, aminokislotalar amfoter birikmalar bo lib, asoslar bilan ham, kislotalar bilan ham reaksiyaga kirishib tuzlar hosil qiladi. Ular aminoguruh hisobiga va karboksil guruh hisobiga alohida reaksiyalarga kirishadi . M-n, nitrit kislota ta sirida -aminokislotalar diazobirikmalar ga aylanadi. Odatda bu reaksiyada aminokislota efiridan foydalaniladi:
Слайд 24
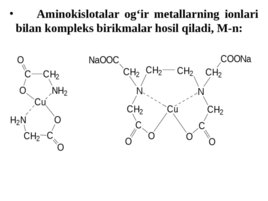
Aminokislotalar og ir metallarning ionlari bilan kompleks birikmalar hosil qiladi, M-n:
Слайд 25

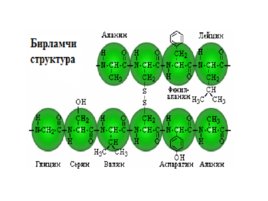
Suvda eruvchan komplekslar hosil qiluvchi aminokislotalar kompleksonlar deb ataladi. E eng muhim kompleksonlardan biri etilendiamintetrasirka kislota (trilon B)dir: Oqsillar ham amfoter xossaga ega bo lib birlamchi, ikkilamchi va uchlamchi tuzilishga egadir. Oqsillarning polipeptid molekulasidagi - aminokislota qoldiqlarining ketma - ketligi ularning birlamchi strukturasi deyiladi .
Слайд 26

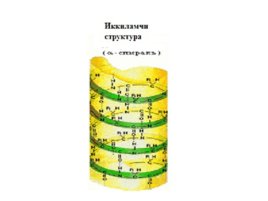
Oqsillarning ichki ( -) va molekulalararo ( -) vodorod bog lari hosil bo lishi tufayli spiralsimon tuzilishi ularning ikkilamchi strukturasi deb ataladi . Silindrsimon - spirallarning fazoda turlicha joylashishi va makromolekula turli qismlarida S - S disulfid ko priklarini hosil qilishiga oqsillarning uchlamchi strukturasi deb ataladi . Bir nechta polipeptid zanjirlarning vodorod bog lari , ion juftlari hosil qilib birlashishi oqsillarning to rtlamchi strukturasi deb ataladi . Oqsillarga biuret, ksantoprotein, Millon va ningidrin reaksiyalari xosdir. Oqsillar organizmda muhim hayotiy vazifani bajaradi.
Слайд 27

Алоҳида вакиллари. Аминосирка кислота (гликоколь, глицин) желатинани, фибро - инни гидролизлаб олинади. Хлорсирка кислотага аммиак таъсир эттириб олиниши мумкин. -Аминопропион кислота ( -аланин). ( )-аланин ҳамма оқсиллар таркибига киради. Циангидрин усули билан олинади. -Аминоизокапрон кислота (лейцин). ( )-лейцин кўпчилик оқсиллар, айниқса гемоглобин таркибига киради.
Слайд 28

Диаминокапрон кислота (лизин), ( )–лизин айрим балиқларнинг икрасидаги оқсил таркибига киради. Алмаштириб бўлмайдиган аминокислоталар қаторига мансуб.
Цистин Цистин қолдиғи шоҳ, жун, соч, тирноқ, оқсили таркибига киради.
Слайд 29
Слайд 30
Слайд 31

Слайд 32

^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.







