Презентация - Решение экспериментальных задач как условие развития познавательного интереса учащихся
Нужно больше вариантов? Смотреть похожие Нажмите для полного просмотра 
|
Распечатать
- Уникальность: 90%
- Слайдов: 35
- Просмотров: 753
- Скачиваний: 37
- Размер: 7.17 MB
- Класс: 11
- Формат: ppt / pptx
Примеры похожих презентаций
 Коллективно-проектная деятельность как условие познавательной активности учащихся
Коллективно-проектная деятельность как условие познавательной активности учащихся Когнитивная компетенция как средство развития одаренности обучающихся на уроках гуманитарного цикла в условиях ФГОС
Когнитивная компетенция как средство развития одаренности обучающихся на уроках гуманитарного цикла в условиях ФГОС Инновационные технологии как одно из средств активизации познавательной деятельности в условиях образовательной деятельности школы
Инновационные технологии как одно из средств активизации познавательной деятельности в условиях образовательной деятельности школы Образовательный терренкур и геокэшинг как средство развития познавательной активности дошкольников
Образовательный терренкур и геокэшинг как средство развития познавательной активности дошкольников Развитие технического творчества на уроках физики посредством решения открытых задач
Развитие технического творчества на уроках физики посредством решения открытых задач Развитие профессиональной компетентности педагога, как условие реализации требований ФГОС
Развитие профессиональной компетентности педагога, как условие реализации требований ФГОС Пути и способы развития интереса учащихся на уроках
Пути и способы развития интереса учащихся на уроках
Слайды и текст этой онлайн презентации
Слайд 1

Муниципальное казенное общеобразовательное учреждение
«Средняя школа №1 им. П.И. Николаенко»
Степновского муниципального района Ставропольского края, с. Степное
Решение экспериментальных задач, как условие развития познавательного интереса учащихся.
Учитель химии и биологии Матюшина Оксана Михайловна
2020 г.
Решение экспериментальных задач, как условие развития познавательного интереса учащихся.
Учитель химии и биологии Матюшина Оксана Михайловна
2020 г.
Слайд 2

В процессе обучения химии эксперимент является
своеобразным объектом обучения методом исследования источником и средством нового знания
своеобразным объектом обучения методом исследования источником и средством нового знания
Слайд 3

Основные функции:
Познавательная Воспитывающая Развивающая
Познавательная Воспитывающая Развивающая
Слайд 4

Требования к эксперименту.
Наглядность, выразительность опытов. Кратковременность опытов. Убедительность. Доступность, достоверность. Безопасность выполняемых опытов.
Наглядность, выразительность опытов. Кратковременность опытов. Убедительность. Доступность, достоверность. Безопасность выполняемых опытов.
Слайд 5

Экспериментальная химическая задача
Слайд 6
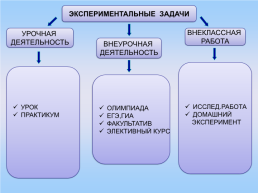
ЭКСПЕРИМЕНТАЛЬНЫЕ ЗАДАЧИ
УРОЧНАЯ ДЕЯТЕЛЬНОСТЬ
ВНЕКЛАССНАЯ РАБОТА
ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬ
ИССЛЕД.РАБОТА ДОМАШНИЙ ЭКСПЕРИМЕНТ
УРОК ПРАКТИКУМ
ОЛИМПИАДА ЕГЭ,ГИА ФАКУЛЬТАТИВ ЭЛЕКТИВНЫЙ КУРС
УРОЧНАЯ ДЕЯТЕЛЬНОСТЬ
ВНЕКЛАССНАЯ РАБОТА
ВНЕУРОЧНАЯ ДЕЯТЕЛЬНОСТЬ
ИССЛЕД.РАБОТА ДОМАШНИЙ ЭКСПЕРИМЕНТ
УРОК ПРАКТИКУМ
ОЛИМПИАДА ЕГЭ,ГИА ФАКУЛЬТАТИВ ЭЛЕКТИВНЫЙ КУРС
Слайд 7

В своей работе я использую следующие типы экспериментальных задач:
1. Задачи на получение веществ - Исходя из железа, получите гидроксид железа (+2). 2. Задачи на распознавание веществ - В трех пронумерованных пробирках находятся растворы хлорида, сульфата и карбоната натрия. Распознайте каждое вещество. 3. Задачи на доказательство качественного состава веществ - Докажите качественный состав сульфата бария. 4. Задачи на объяснение наблюдаемого явления - Испытайте лакмусом растворы карбоната калия, хлорида алюминия, хлорида натрия. Объясните результаты испытаний.
1. Задачи на получение веществ - Исходя из железа, получите гидроксид железа (+2). 2. Задачи на распознавание веществ - В трех пронумерованных пробирках находятся растворы хлорида, сульфата и карбоната натрия. Распознайте каждое вещество. 3. Задачи на доказательство качественного состава веществ - Докажите качественный состав сульфата бария. 4. Задачи на объяснение наблюдаемого явления - Испытайте лакмусом растворы карбоната калия, хлорида алюминия, хлорида натрия. Объясните результаты испытаний.
Слайд 8

Этапы решения экспериментальной задачи:
Постановка проблемы Построение гипотезы Проектирование опыта Составление плана эксперимента Осуществление эксперимента Оформление результатов эксперимента Формулирование выводов.
Постановка проблемы Построение гипотезы Проектирование опыта Составление плана эксперимента Осуществление эксперимента Оформление результатов эксперимента Формулирование выводов.
Слайд 9

«Исследование моющего действия растворов мыла и синтетического порошка» 10 класс
Выяснить, почему СМС обладает более сильным моющим действием, чем мыло. Причиной различного моющего действия исследуемых веществ является различие в их строении. Исследовать моющее действие мыла и СМС в жесткой воде, определить среду растворов.
Выяснить, почему СМС обладает более сильным моющим действием, чем мыло. Причиной различного моющего действия исследуемых веществ является различие в их строении. Исследовать моющее действие мыла и СМС в жесткой воде, определить среду растворов.
Слайд 10

«Исследование моющего действия растворов мыла и синтетического порошка» 10 класс
План эксперимента: а) определить моющее действие мыла и СМС в жесткой воде. б) с помощью индикатора фенолфталеина определить среду каждого раствора. 5. Осуществление эксперимента 6. Оформление результатов (в виде таблицы) Выводы: СМС обладают в 10 раз большей моющей способностью, чем мыла; не боятся жесткой воды, т.к. их кальциевые соли растворимы в воде; обладают более сильной щелочной средой, чем мыла.
План эксперимента: а) определить моющее действие мыла и СМС в жесткой воде. б) с помощью индикатора фенолфталеина определить среду каждого раствора. 5. Осуществление эксперимента 6. Оформление результатов (в виде таблицы) Выводы: СМС обладают в 10 раз большей моющей способностью, чем мыла; не боятся жесткой воды, т.к. их кальциевые соли растворимы в воде; обладают более сильной щелочной средой, чем мыла.
Слайд 11

По итогам проведенных опытов учащиеся заполнили таблицу.
Порядок выполнения работы.Химизм процесса
1. В две пробирки с водопроводной водой прилили: в одну – раствор мыла, в другую – раствор порошка. В первом случае приходится добавлять больше раствора для образования устойчивой пены, во второй пробирке пена образуется почти сразу.Мыло – это натриевые соли высших карбоновых кислот. В жесткой воде мыло не пенится, так как образуются нерастворимые соли: 2C17H35COONa+Ca(HCO3)2=(C17H35COO)2Ca+ 2NaHCO3 Стеарат кальция СМС – натриевые соли кислых сложных эфиров высших спиртов и серной кислоты. Их преимущество заключается в том, что их кальциевые соли растворимы в воде и они не утрачивают моющее действие в жесткой воде.
2. В пробирки с растворами мыла и порошка прилили фенолфталеин. Индикатор окрасился в малиновый цвет (во второй пробирке более интенсивное окрашивание), что свидетельствует о щелочной среде растворов..Натриевые соли карбоновых кислот, образованные сильными основаниями и слабыми кислотами, подвергаются гидролизу: C17H35COO - + Na+ + H2O C17H35COOH+ Na++OH -
Порядок выполнения работы.Химизм процесса
1. В две пробирки с водопроводной водой прилили: в одну – раствор мыла, в другую – раствор порошка. В первом случае приходится добавлять больше раствора для образования устойчивой пены, во второй пробирке пена образуется почти сразу.Мыло – это натриевые соли высших карбоновых кислот. В жесткой воде мыло не пенится, так как образуются нерастворимые соли: 2C17H35COONa+Ca(HCO3)2=(C17H35COO)2Ca+ 2NaHCO3 Стеарат кальция СМС – натриевые соли кислых сложных эфиров высших спиртов и серной кислоты. Их преимущество заключается в том, что их кальциевые соли растворимы в воде и они не утрачивают моющее действие в жесткой воде.
2. В пробирки с растворами мыла и порошка прилили фенолфталеин. Индикатор окрасился в малиновый цвет (во второй пробирке более интенсивное окрашивание), что свидетельствует о щелочной среде растворов..Натриевые соли карбоновых кислот, образованные сильными основаниями и слабыми кислотами, подвергаются гидролизу: C17H35COO - + Na+ + H2O C17H35COOH+ Na++OH -
Слайд 12

ПРАКТИКУМ
8 КЛАСС
9 КЛАСС
Практикум №1 «Простейшие операции с веществом» Практикум №2 «Свойства растворов электролитов».
Практикум №1 «Свойства металлов и их соединений» Практикум №2 «Свойства соединений неметаллов» Практикум №3 «Свойства органических веществ».
8 КЛАСС
9 КЛАСС
Практикум №1 «Простейшие операции с веществом» Практикум №2 «Свойства растворов электролитов».
Практикум №1 «Свойства металлов и их соединений» Практикум №2 «Свойства соединений неметаллов» Практикум №3 «Свойства органических веществ».
Слайд 13

Практикум
более высокая ступень развития ученического эксперимента, качественно новый этап повышения самостоятельности; учащиеся выполняют целую серию практических работ в конце большого раздела курса химии, благодаря чему, практикум носит повторительно-обобщающий характер.
более высокая ступень развития ученического эксперимента, качественно новый этап повышения самостоятельности; учащиеся выполняют целую серию практических работ в конце большого раздела курса химии, благодаря чему, практикум носит повторительно-обобщающий характер.
Слайд 14

Предпрофильное обучение химии
Факультативный курс «Химия для восьмиклассников» Элективные курсы в 9 классе: «Введение в неорганический синтез» «Экспериментальное решение задач по химии». Профильное обучение химии Элективные курсы : «Углубленное изучение органической химии через систему экспериментальных работ» 10 класс «Решение задач по химии» 11 класс «Химия в вопросах ЕГЭ» 11 класс
Факультативный курс «Химия для восьмиклассников» Элективные курсы в 9 классе: «Введение в неорганический синтез» «Экспериментальное решение задач по химии». Профильное обучение химии Элективные курсы : «Углубленное изучение органической химии через систему экспериментальных работ» 10 класс «Решение задач по химии» 11 класс «Химия в вопросах ЕГЭ» 11 класс
Слайд 15

Профильное обучение химии
«Распознавание лекарственных средств и их идентификация» 10 класс
«Распознавание лекарственных средств и их идентификация» 10 класс
Слайд 16

Профильное обучение химии
«Анализ пищевых продуктов» 10 класс
«Анализ пищевых продуктов» 10 класс
Слайд 17

Экспериментальные задачи в заданиях ЕГЭ
№7. В одну из пробирок с осадком гидроксида алюминия добавили сильную кислоту X, а в другую – раствор вещества Y. В результате в каждой из пробирок наблюдали растворение осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) бромоводородная кислота 2) гидросульфид натрия 3) сероводородная кислота 4) гидроксид калия 5) гидрат аммиака
№7. В одну из пробирок с осадком гидроксида алюминия добавили сильную кислоту X, а в другую – раствор вещества Y. В результате в каждой из пробирок наблюдали растворение осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) бромоводородная кислота 2) гидросульфид натрия 3) сероводородная кислота 4) гидроксид калия 5) гидрат аммиака
Слайд 18

Экспериментальные задачи в заданиях ЕГЭ
№25. Установите соответствие между двумя веществами, взятыми в виде водных растворов, и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. ВЕЩЕСТВА РЕАКТИВ А) H2SO4 (разб.) и HNO3 (разб.) 1) фенолфталеин Б) AlCl3 и KCl 2) CuCl2 В) HCl и HI 3) MgO Г) ZnCl2 и HgCl2 4) лакмус 5) Cu .
№25. Установите соответствие между двумя веществами, взятыми в виде водных растворов, и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. ВЕЩЕСТВА РЕАКТИВ А) H2SO4 (разб.) и HNO3 (разб.) 1) фенолфталеин Б) AlCl3 и KCl 2) CuCl2 В) HCl и HI 3) MgO Г) ZnCl2 и HgCl2 4) лакмус 5) Cu .
Слайд 19

Экспериментальные задачи в заданиях ЕГЭ
№30. Для выполнения задания используйте следующий перечень веществ: перманганат калия, гидрокарбонат натрия, сульфит натрия, сульфат бария, гидроксид калия, пероксид водорода. Допустимо использование водных растворов веществ. Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора. Выделение осадка или газа в ходе этой реакции не наблюдается. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
№30. Для выполнения задания используйте следующий перечень веществ: перманганат калия, гидрокарбонат натрия, сульфит натрия, сульфат бария, гидроксид калия, пероксид водорода. Допустимо использование водных растворов веществ. Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора. Выделение осадка или газа в ходе этой реакции не наблюдается. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Слайд 20

Экспериментальные задачи в заданиях ЕГЭ
№32. При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите уравнения четырёх описанных реакций.
№32. При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите уравнения четырёх описанных реакций.
Слайд 21

Экспериментальные задачи в заданиях ОГЭ
№13. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ А) CuCl2 и NaOH 1) выпадение белого осадка Б) BaCl2 и AgNO3 2) выпадение бурого осадка В) FeCl3 и Ba(OH)2 3) выпадение голубого осадка 4) выделение газа
№13. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ А) CuCl2 и NaOH 1) выпадение белого осадка Б) BaCl2 и AgNO3 2) выпадение бурого осадка В) FeCl3 и Ba(OH)2 3) выпадение голубого осадка 4) выделение газа
Слайд 22

Экспериментальные задачи в заданиях ОГЭ
№18. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. ВЕЩЕСТВА РЕАКТИВ А) K2CO3 и K2SiO3 1) CuCl2 Б) K2CO3 и Li2CO3 2) HCl В) Na2SO4 и NaOH 3) MgO 4) K3PO4
№18. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. ВЕЩЕСТВА РЕАКТИВ А) K2CO3 и K2SiO3 1) CuCl2 Б) K2CO3 и Li2CO3 2) HCl В) Na2SO4 и NaOH 3) MgO 4) K3PO4
Слайд 23

Экспериментальные задачи в заданиях ОГЭ
№23. Дан раствор сульфата магния, а также набор следующих реактивов: цинк; соляная кислота; растворы гидроксида натрия, хлорида бария и нитрата калия. Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания. Ознакомьтесь с инструкцией по выполнению задания, прилагаемой к заданиям КИМ. Подготовьте лабораторное оборудование, необходимое для проведения эксперимента.
№23. Дан раствор сульфата магния, а также набор следующих реактивов: цинк; соляная кислота; растворы гидроксида натрия, хлорида бария и нитрата калия. Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания. Ознакомьтесь с инструкцией по выполнению задания, прилагаемой к заданиям КИМ. Подготовьте лабораторное оборудование, необходимое для проведения эксперимента.
Слайд 24

Экспериментальные задачи в заданиях ОГЭ
№24. Проведите химические реакции между сульфатом магния и выбранными веществами в соответствии с составленными уравнениями реакции, соблюдая правила техники безопасности, приведённые в инструкции к заданию. Проверьте, правильно ли указаны в ответе на задание 23 признаки протекания реакций. При необходимости, дополните ответ или скорректируйте его.
№24. Проведите химические реакции между сульфатом магния и выбранными веществами в соответствии с составленными уравнениями реакции, соблюдая правила техники безопасности, приведённые в инструкции к заданию. Проверьте, правильно ли указаны в ответе на задание 23 признаки протекания реакций. При необходимости, дополните ответ или скорректируйте его.
Слайд 25
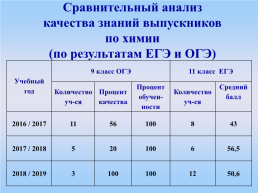
Сравнительный анализ качества знаний выпускников по химии (по результатам ЕГЭ и ОГЭ)
Учебный год.9 класс ОГЭ.11 класс ЕГЭ
Количество уч-ся.Процент качества.Процент обучен-ности.Количество уч-ся.Средний балл
2016 / 2017.11.56.100.8.43
2017 / 2018.5.20.100.6.56,5
2018 / 2019.3.100.100.12.50,6
Учебный год.9 класс ОГЭ.11 класс ЕГЭ
Количество уч-ся.Процент качества.Процент обучен-ности.Количество уч-ся.Средний балл
2016 / 2017.11.56.100.8.43
2017 / 2018.5.20.100.6.56,5
2018 / 2019.3.100.100.12.50,6
Слайд 26

Внеклассная работа «Вода – чудо природы» 8 класс
Слайд 27

Учебно-исследовательская деятельность
Основные этапы моей работы, как руководителя проекта.
Этап работы.Деятельность учителя
Разработка проектного задания.Помощь в выборе темы работы, разработка проектного задания, выявление проблемы, постановка цели и формулировка задач.
Разработка проекта.Консультации и координация работы: актуализация знаний, обсуждение вариантов исследования, продумывание плана способов деятельности, распределение обязанностей, организация проведения исследований, решение отдельных задач.
Оформление результатов.Помощь в оформлении письменного отчёта, анализе проделанной работы, обобщении результатов, корректировке выводов.
Презентация.Совместная подготовка устного сообщения, помощь при подготовке средств наглядности, консультации по выступлению перед публикой.
Рефлексия.Организация самоанализа успехов и ошибок.
Основные этапы моей работы, как руководителя проекта.
Этап работы.Деятельность учителя
Разработка проектного задания.Помощь в выборе темы работы, разработка проектного задания, выявление проблемы, постановка цели и формулировка задач.
Разработка проекта.Консультации и координация работы: актуализация знаний, обсуждение вариантов исследования, продумывание плана способов деятельности, распределение обязанностей, организация проведения исследований, решение отдельных задач.
Оформление результатов.Помощь в оформлении письменного отчёта, анализе проделанной работы, обобщении результатов, корректировке выводов.
Презентация.Совместная подготовка устного сообщения, помощь при подготовке средств наглядности, консультации по выступлению перед публикой.
Рефлексия.Организация самоанализа успехов и ошибок.
Слайд 28

«Определение физико-химических показателей молока» Самойлова Екатерина 10 класс
Слайд 29

«Исследование качества чипсов
и их влияние на организм» Сачко Валерия
10 класс
Слайд 30

«Природные индикаторы» Тагланова Мадина
9 класс
Слайд 31

«Исследование состава и качества шоколада» Тагланова Фатима
11 класс
Слайд 32

Домашний эксперимент
Слайд 33

Домашний эксперимент
Изучение скорости горения свечи. Определение щелочного характера мыльного раствора с помощью самодельных индикаторов (сока черной смородины или свекольного сока). Определение временной жесткости воды. Действие каталазы на пероксид водорода.
Изучение скорости горения свечи. Определение щелочного характера мыльного раствора с помощью самодельных индикаторов (сока черной смородины или свекольного сока). Определение временной жесткости воды. Действие каталазы на пероксид водорода.
Слайд 34

Целенаправленная и систематическая работа по формированию исследовательских умений учащихся способствует:
усилению мотивации учебной деятельности; изменению качества учебного процесса повышению интереса учащихся к химии; развитие самостоятельности в деятельности по приобретению знаний; интеллектуальному росту обучающихся.
усилению мотивации учебной деятельности; изменению качества учебного процесса повышению интереса учащихся к химии; развитие самостоятельности в деятельности по приобретению знаний; интеллектуальному росту обучающихся.
Слайд 35

Необходимо помнить, что решение экспериментальных задач — это не самоцель, а средство обучения, способствующее прочному усвоению знаний.
^ Наверх
X
Благодарим за оценку!
Мы будем признательны, если Вы так же поделитесь этой презентацией со своими друзьями и подписчиками.
