Слайды и текст этой онлайн презентации
Слайд 1
Тема: Типы химических связей .
Слайд 2
Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы
Слайд 3
Ионная химическая связь
это связь, образовавшаяся за счет электростатического притяжения
катионов к анионам
Слайд 4
Водородная связь
Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары (F, О, N и реже С и S) другой молекулы (или ее части)
O H…O H…O H…
H H H
Слайд 5
Металлическая связь
связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке
о п+
М — пе М
Схема образования металлической связи:
Задание:
Выпишите формулы веществ, в которых присутствует металлическая и водородная связи
Na, KF, NH3, C2H2, CH3-COOH, H2S, AL, NaCL.
Слайд 6
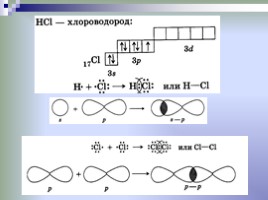
Ковалентная химическая связь
это связь, возникающая между атомами за счет образования общих электронных пар
Обменный
Донорно -акцепторный
Механизм образования связи:
Слайд 8
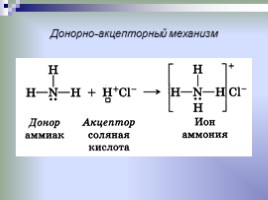
Донорно-акцепторный механизм
Слайд 9
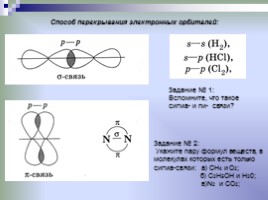
Способ перекрывания электронных орбиталей:
Задание № 1: Вспомните, что такое сигма- и пи- связи?
Задание № 2:
Укажите пару формул веществ, в молекулах которых есть только сигма-связи: а) СН4 и О2;
б) С2Н5ОН и Н20;
в)N2 и CO2;
Слайд 10
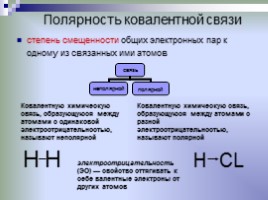
Полярность ковалентной связи
степень смещенности общих электронных пар к одному из связанных ими атомов
электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов
Ковалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной
Ковалентную химическую связь, образующуюся между атомами с разной электроотрицательностью, называют полярной
H H
H СL
Слайд 11
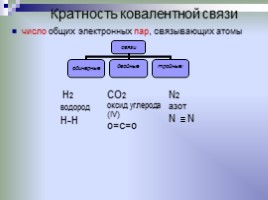
Кратность ковалентной связи
число общих электронных пар, связывающих атомы
CO2
оксид углерода (IV)
о=с=о
N2
азот
N N
H2
водород
H-H
 Типы химических реакций
Типы химических реакций Повторение «Типы химических реакций»
Повторение «Типы химических реакций» Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды Основные типы химических реакций (8 класс)
Основные типы химических реакций (8 класс) Типы и стили речи
Типы и стили речи Проект «Типы предприятий общественного питания на примере г. Каменска-Уральского»
Проект «Типы предприятий общественного питания на примере г. Каменска-Уральского» Амфотерность химических соединений
Амфотерность химических соединений