Слайды и текст этой онлайн презентации
Слайд 1
Урок химии 10 класс Арены. Бензол
Слайд 2
1)Углеводороды с общей формулой СnН2n+2
2) Частица с одним свободным электроном
3) Суффикс, который используется в названиях органических веществ для указания наличия в их молекуле двойной связи
4) Реакция взаимодействия органических веществ с азотной кислотой
А лканы
Р адикал
Е н
Нитрование
Ы
Слайд 4
Дано W(C) = 92,3 % D (CxHy/возд) = 2,69 Найти СхНу 1. W(H) = 100% - W(C) = 7,7% 2. Примем массу СхНу за 100 г, тогда m(C) = 92,3 г m(H) = 7,7 г 3. n(C) = 92,3 / 12 = 7,7 моль n(H) = 7,7 / 1 = 7,7 моль 4. х : у = n(C) : n(H) = 7,7 : 7,7 = 1 : 1 СН - простейшая формула 5. М(СН) = 13 г/моль М(СхНу) = D * M (воздуха) = 2,69 * 29 = 78 г/моль 78 / 13 = 6, умножаем индексы в простейшей формуле на 6. С6Н6 - бензол
Слайд 5
АРЕНЫ.
Представитель - С6Н6 бензол
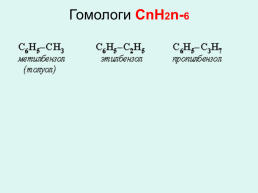
Общая формула - СnН2n-6
Слайд 6
История открытия
Впервые бензол описал немецкий химик Иоганн Глаубер, который получил это соединение в 1649 году в результате перегонки каменно-угольной смолы. Но ни названия вещество не получило, ни состав его не был известен.
Иоганн
Глаубер
Слайд 7
Своё второе рождение бензол получил благодаря работам Фарадея. Бензол был открыт в 1825 году английским физиком Майклом Фарадеем, который выделил его из жидкого конденсата светильного газа.
Майкл Фарадей
Слайд 8
В 1833 году немецкий физик и химик Эйльгард Мичерлих получил бензол при сухой перегонке кальциевой соли бензойной кислоты (именно от этого и произошло название бензол)
Эйльгард Мичерлих
Слайд 9
Структурная формула бензола
Была предложена немецким ученым А. Кекуле в 1865 году
Бензол не взаимодействует с бромной водой и
с раствором перманганата калия!
Н0
А.Кекуле
Слайд 10
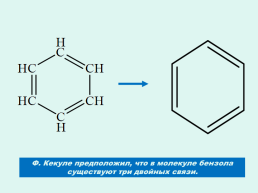
Ф. Кекуле предположил, что в молекуле бензола существуют три двойных связи.
Слайд 11
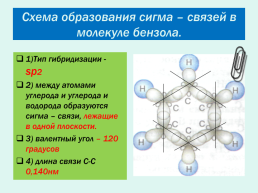
Схема образования сигма – связей в молекуле бензола.
1)Тип гибридизации - sр2
2) между атомами углерода и углерода и водорода образуются сигма – связи, лежащие в одной плоскости.
3) валентный угол – 120 градусов
4) длина связи С-С 0,140нм
Слайд 12
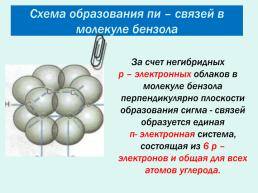
Схема образования пи – связей в молекуле бензола
За счет негибридных
р – электронных облаков в молекуле бензола перпендикулярно плоскости образования сигма - связей образуется единая
п- электронная система, состоящая из 6 р – электронов и общая для всех атомов углерода.
Слайд 13
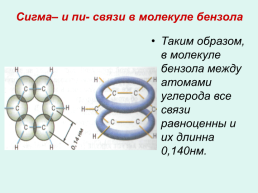
Сигма– и пи- связи в молекуле бензола
Таким образом, в молекуле бензола между атомами углерода все связи равноценны и их длинна 0,140нм.
Слайд 14
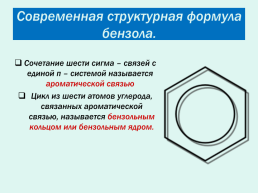
Современная структурная формула бензола.
Сочетание шести сигма – связей с единой п – системой называется ароматической связью
Цикл из шести атомов углерода, связанных ароматической связью, называется бензольным кольцом или бензольным ядром.
Слайд 15
Строение молекулы бензола
Слайд 17
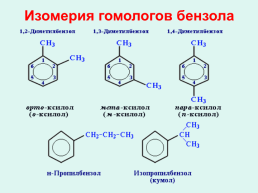
Изомерия гомологов бензола
Слайд 18
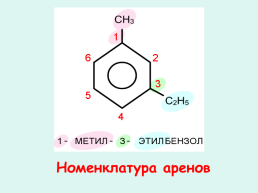
Номенклатура аренов
Слайд 19
Получение
Бензол получают из каменноугольной смолы, образующейся при коксовании угля.
В настоящее время бензол получают из нефти.
Бензол получают синтетическими методами.
Слайд 20
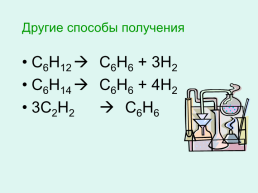
Другие способы получения
С6Н12 С6Н6 + 3Н2
С6Н14 С6Н6 + 4Н2
3С2Н2 С6Н6
Слайд 21
Физические свойства
Бензол – бесцветная, летучая, огнеопасная жидкость с неприятным запахом. Он легче воды ( =0,88 г/см3) и с ней не смешивается, но растворим в органических растворителях, и сам хорошо растворяет многие вещества. Бензол кипит при 80,1 С, при охлаждении легко застывает в белую кристаллическую массу. Бензол и его пары ядовиты. Систематическое вдыхание его паров вызывает анемию и лейкемию.
Слайд 22
Физические свойства бензола
Слайд 23
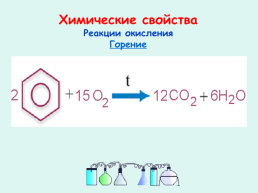
Химические свойства
Реакции окисления
Горение
Слайд 24
Химические свойства
Реакции окисления
Мягкое окисление
Бензол не обесцвечивает раствор перманганата калия
Слайд 25
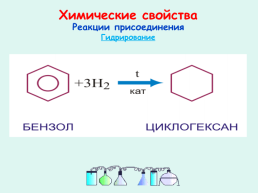
Химические свойства
Реакции присоединения
Гидрирование
Слайд 26
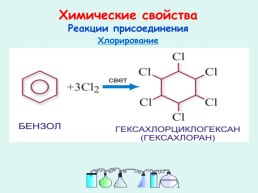
Химические свойства
Реакции присоединения
Хлорирование
Слайд 27
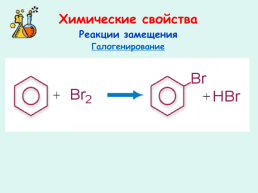
Химические свойства
Реакции замещения
Галогенирование
Слайд 28
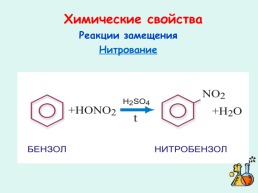
Химические свойства
Реакции замещения
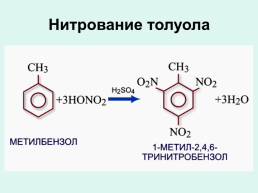
Нитрование
Слайд 29
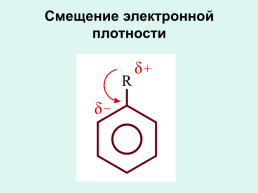
Смещение электронной плотности
Слайд 30
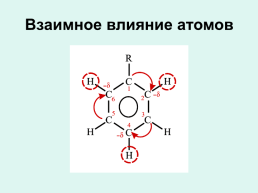
Взаимное влияние атомов
Слайд 31
Нитрование толуола
Слайд 32
Домашнее задание
§ 15,
упр.1-4, Презентация «Применение бензола»
 Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека»
Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека» Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс
Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс Урок химии в 10-м классе по теме «Аминокислоты»
Урок химии в 10-м классе по теме «Аминокислоты» К уроку химии по теме Моносахариды. Глюкоза, свойства, значение. 10-й класс
К уроку химии по теме Моносахариды. Глюкоза, свойства, значение. 10-й класс Урок химии в 10 классе «Сложные эфиры»
Урок химии в 10 классе «Сложные эфиры» Бурый дым ”Лисий хвост”.. Урок химии в 9-х классах
Бурый дым ”Лисий хвост”.. Урок химии в 9-х классах Открытый урок по химии 10 класс «Формулы и вещества»
Открытый урок по химии 10 класс «Формулы и вещества»