Слайды и текст этой онлайн презентации
Слайд 1
Урок в 10-м профильном классе по теме «ДИСАХАРИДЫ. САХАРОЗА»
Слайд 2
Цели:
создать условия для восприятия и первичного закрепления нового материала о строении и свойствах сахарозы как представителя дисахаридов;
показать практическую значимость изучаемого материала;
развивать навыки исследовательской работы, умение работать в группе;
поддерживать интерес к изучаемому предмету.
Слайд 3
Задание
Это вещество используют для получения искусственного меда. В сахарном тростнике содержится до 26% этого вещества. Оно является основным источником энергии для питания головного мозга. Известен его элементный состав: углерода – 42,11%, водорода – 6,43%, кислорода – 51,46%. Известно также, что молекула этого вещества тяжелее молекулы глюкозы в 1,9 раза. Выведите молекулярную формулу этого вещества.
Слайд 4
Определение
Дисахариды – это углеводы, которые гидролизуются с образованием двух молекул моносахаридов.
C12Н22О11 - молекулярная формула сахарозы
Слайд 5
Физические свойства
Бесцветное кристаллическое вещество, в большой массе белого цвета;
Хорошо растворимо в воде (особенно при температуре);
Сладкое на вкус;
При нагревании образуют карамель (тягучую, темно-бурую вязкую массу).
Слайд 6

Получение сахарозы из сахарной свеклы
Вначале свеклу хорошо отмывают, потом нарезают в виде мелких ломтиков или короткой лапши. Затем эту массу помещают в огромные котлы – диффузоры, в которых из свеклы горячая вода вымывает сахарозу (сахар). Вместе с ней из свеклы в водный раствор переходят и другие компоненты (различные органические кислоты, белки, красящие вещества и др.). Чтобы отделить эти продукты от сахарозы, раствор обрабатывают известковым молоком (гидроксидом кальция). Оно, реагируя с органическими кислотами, образует малорастворимые соли, которые выпадают в осадок. Сахароза образует с гидроксидом кальция растворимый сахарат кальция C12H22O11.CaO.2H2O. Этот продукт затем разлагается при пропускании через раствор углекислого газа. Выпавший в осадок карбонат кальция отфильтровывают, а раствор упаривают в вакууме. Начинается кристаллизация сахарозы, которую по мере образования отделяют центрифугированием. Оставшийся раствор – меласса – содержит до 50% сахарозы. Его используют для производства лимонной кислоты.
Выделенную сахарозу очищают и обесцвечивают. Для этого ее растворяют в воде и полученный раствор фильтруют через активированный уголь. Затем раствор снова упаривают и кристаллизуют.
Слайд 7
Химические свойства
Химические свойства невосстанавливающих дисахаридов определяются только спиртовыми (гидроксильными) группами. Возможна реакция этерификации:
C12H14O3(OH)8 + 8(CH3CO)2O
C12H14O3(CH3COO)8 + 8CH3COOH.
Слайд 8
Химические свойства
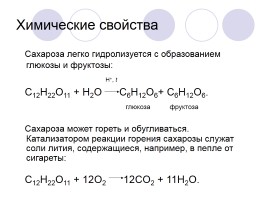
Сахароза легко гидролизуется с образованием глюкозы и фруктозы:
H+, t
C12H22O11 + H2O C6H12O6+ C6H12O6.
глюкоза фруктоза
Сахароза может гореть и обугливаться. Катализатором реакции горения сахарозы служат соли лития, содержащиеся, например, в пепле от сигареты:
C12H22O11 + 12O2 12CO2 + 11H2O.
Слайд 9
Химические свойства
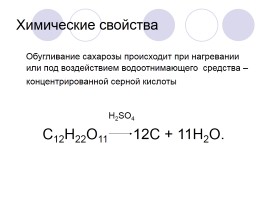
Обугливание сахарозы происходит при нагревании или под воздействием водоотнимающего средства – концентрированной серной кислоты
H2SO4
C12H22O11 12C + 11H2O.
Слайд 10
Применение сахарозы
Сахароза используется непосредственно как пищевой продукт или же в составе различных кондитерских изделий. В большой концентрации ее применяют в виде консерванта.
Помимо этого, сахарозу используют в химической промышленности для получения бутанола, глицерина, декстрана, этанола и лимонной кислоты.
Также сахароза является достаточно ценным сырьем в фармацевтической промышленности при изготовлении лекарственных препаратов.
В заключение хотелось бы отметить, что именно сахарный тростник является главным сырьем в производстве сахарозы. На его долю приходится две трети производимого во всем мире сахара.
 Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека»
Разработка урока по химии в 10 классе по теме «Лекарства и здоровье человека» Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс
Интегрированный урок по биологии и химии по теме Чудо фотосинтеза. 10-й класс Урок математики в 6 классе по теме «Пропорции»
Урок математики в 6 классе по теме «Пропорции» Повторительно- обобщающий урок по теме «причастие» 7 классе
Повторительно- обобщающий урок по теме «причастие» 7 классе К уроку в 7 классе по теме: «изготовление проектного изделия»
К уроку в 7 классе по теме: «изготовление проектного изделия» Урок алгебры в 9 классе по теме «Неравенства»
Урок алгебры в 9 классе по теме «Неравенства» Урок литературы в 10 классе по теме «Мыслящая поэзия»
Урок литературы в 10 классе по теме «Мыслящая поэзия»